Anexo
Instrumento
Encuesta
Estimado alumno: Te solicitamos responder las siguientes preguntas. Los resultados nos permitirán avanzar en el estudio de las dificultades que habitualmente se presentan en nuestros cursos y así poder realizar mejoras en la enseñanza de la materia. ¡Gracias por tu colaboración!
Parte 3. Opciones Múltiples
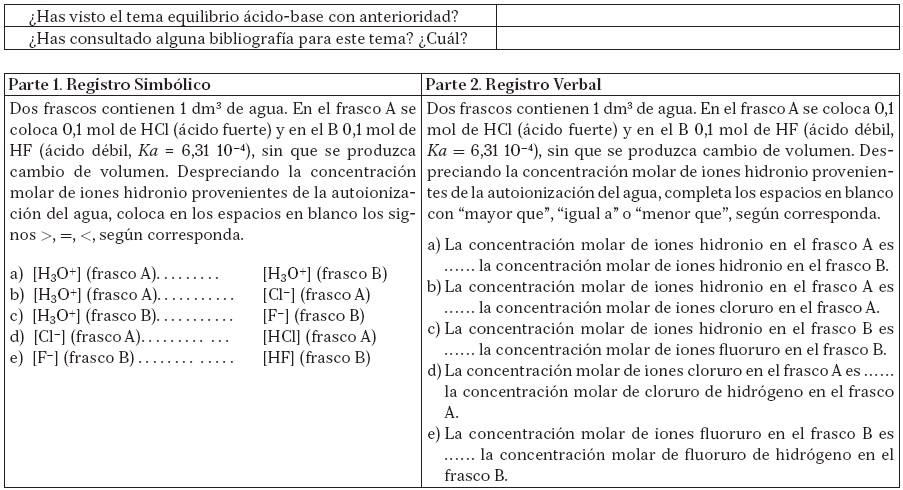
Dos frascos contienen 1 dm3 de agua. En el frasco A se coloca 0,1 mol de HCl (ácido fuerte) y en el B 0,1 mol de HF (ácido débil, Ka = 6,31 10−4), sin que se produzca cambio de volumen. Despreciando la concentración molar de iones hidronio provenientes de la autoionización del agua, indica si las siguientes afirmaciones son correctas (C) o incorrectas (I):
Frasco A
□ a- En este frasco no quedan moléculas de cloruro de hidrógeno disueltas, queda 0,1 mol de iones hidronio y 0,1 mol de iones cloruro disueltos en agua.
□ b- En este frasco queda 0,1 mol de moléculas de cloruro de hidrógeno disueltas, 0,1 mol de iones hidronio y 0,1 mol de iones cloruro disueltos en agua.
□ c- Este frasco contiene una solución de ácido clorhídrico 0,1 molar.
□ d- En este frasco no quedan moléculas de cloruro de hidrógeno disueltas.
□ e- Al tratarse de una solución de un ácido fuerte, en este frasco la concentración de iones hidronio es menor que 0,1 molar pues las uniones entre los átomos de hidrógeno y cloro son fuertes.
Frasco B
□ a- En este frasco queda disuelto igual número de moléculas de fluoruro de hidrógeno que de iones fluoruro porque en el equilibrio hay igual cantidad de reactivos que de productos.
□ b- Este frasco contiene una solución de ácido fluorhídrico 0,1 molar.
□ c- En este frasco no quedan moléculas de fluoruro de hidrógeno disueltas, queda 0,1 mol de iones hidronio y 0,1 mol de iones fluoruro disueltos en agua.
□ d- En este frasco quedan moléculas de fluoruro de hidrógeno disueltas pero en una cantidad menor que 0,1 mol.
□ e- En este frasco la concentración de iones hidronio es 0,1 molar porque se trata de una solución 0,1 molar del ácido.