Introducción
Las úlceras crónicas (UC), son alteraciones en la piel que toman más de seis semanas en cicatrizar [1]. El envejecimiento, la diabetes y la obesidad incrementan la prevalencia de las UC, por lo que son una de las principales causas de morbilidad y mortalidad [2]. Son más frecuentes en personas de la tercera edad con enfermedad vascular periférica [3] y se caracterizan por la presencia de dolor [4] e incapacidad para cicatrizar [5].
Aunque se han desarrollado tratamientos para este tipo de problemas, la mayoría de ellos no tiene efectos benéficos a corto plazo, lo que repercute sobre el gasto público de las instituciones de salud pública y sobre la calidad de vida de los pacientes [6]. Por otro lado, la medicina regenerativa y la ingeniería de tejidos ofrecen una alternativa en terapias celulares para el tratamiento de este tipo de lesiones [7] debido a que pueden reparar/reemplazar el tejido dañado [8]. Las células troncales mesenquimales (CTM) son las células más empleadas en medicina regenerativa debido a que son células progenitoras con capacidad de autoregenerarse y multipotentes, pueden aislarse de varios tejidos como: médula ósea [9], tejido adiposo [10], sangre de cordón umbilical [11], sangre periférica [12], endometrio [13], pulpa dental [14], líquido ammiotico [15] y tejido tumoral [16]. Estas células pueden caracterizarse con base en los criterios propuestos por la International Society for Cell Therapy (ISCT) e incluyen: adherencia al sustrato de cultivo, morfología fibroblastoide, con la capacidad para diferenciarse en células especializadas de la capa mesodérmica: adipocitos, condrocitos, osteoblastos [15], expresión de antígenos membranales: CD73, CD90 y CD105, así como ausencia de los antígenos como: CD34, CD45 y HLA-clase II [9, 10, 17].
Actualmente, se han aplicado en terapias celulares para disminuir la enfermedad injerto contra huésped o GvDH [18], regeneración epitelial en colon [19], ulceras crónicas [20, 21], ulceras asociadas a esclerosis sistémica [8] colitis ulcerativa [22] y pie diabético [23]. Sin embargo, pocos estudios han realizado la aplicación de Células Troncales Mesenquimales derivadas de Gelatina de Wharton para el tratamiento de ulceras crónicas [24]. Por ello, en este trabajo se realizó la aplicación de CTM derivadas de gelatina de Wharton en dos pacientes con diagnóstico de úlcera crónica flebostática, donde se analizaron las modificaciones estructurales del tejido mediante técnicas histológicas, área de la herida, índice de cierre antes y después del tratamiento.
Metodología
Presentación de los casos
Caso 1: Paciente femenina, 55 años de edad con diabetes mellitus tipo 2, insuficiencia venosa periférica crónica y úlcera flebostática en región maleolar del miembro pélvico derecho, más de 3 años de evolución. Caso 2: Paciente femenina, 56 años de edad con insuficiencia venosa periférica crónica, úlcera flebostática en región maleolar del miembro pélvico derecho, más de 5 años de evolución con falla de injerto autólogo.
Recolección cordones umbilicales
La selección de cordones umbilicales se realizó en base a los criterios establecidos por la Ley General de Salud Mexicana, la Norma Oficial Mexicana NOM-253-SSA1-2012 y por el Banco de Sangre de Cordón Umbilical del Instituto Mexicano del Seguro Social Centro Médico Nacional “La Raza”. Una vez seleccionadas las posibles donadoras y previa firma del consentimiento informado, se realizó la recolección de los cordones en condiciones de esterilidad, en una solución amortiguada de fosfatos o PBS (NaCl 8.06 g, KCl 0.22 g, Na2HPO4 1.15 g, KH2PO4 0.20 g H2O 1000 mL-1) y se mantuvieron a 4 °C hasta la extracción de las CTM-GW.
Aislamiento de las CTM-GW
El cordón se cortó en secciones de aprox. 3mm, fueron eliminadas las arterias y vena umbilicales, se disgregó enzimáticamente primero con colagenasa tipo I al 1% en PBS (Sigma-Aldrich, USA) y posteriormente con tripsina al 0.1 %, en agitación constante a 37.5 °C por 60 y 30 minutos respectivamente. El sobrenadante, fue centrifugado a 180 g/10min, el botón celular se resuspendió en medio DMEM-F12 complementado con 10% de suero fetal bovino y 1% de antibiótico-antimicótico (Gibco®, USA). Las células fueron cultivadas en cajas Petri de 100 mm x 20 mm (Corning Centri Star™, USA), se mantuvieron a 37 °C en una atmósfera con humedad saturada con 5% de CO2 en incubadora modelo Galaxy 170R (R.T.L., Colombia). Cuando los cultivos tuvieron una confluencia del 80 - 90%, se realizó la resiembra de las mismas (pases), este procedimiento se repitió hasta obtener las células en un pase no mayor a 6 para poder caracterizar las células y aplicarlas en los pacientes.
Caracterización de las CTM-GW
Se realizó tomando en cuenta los criterios propuestos por la ISCT como: 1) Morfología fibroblastoide y adherencia; las células de Gelatina de Wharton humana se mantuvieron en observación mediante el uso de un microscopio Oxion Inverso (PCE Instruments, Chile), se realizó la documentación fotográfica con una cámara digital Samsung-ST150F 16.2-Megapixel (modelo: EC-ST150FBPBUS). La adherencia se determinó durante los cambios de medio, las células adheridas permanecieron en las cajas Petri en tanto, las células en suspensión, fueron desechadas durante este procedimiento; 2) Pruebas de plasticidad celular. Para inducir la diferenciación hacia osteoblastos y adipocitos, las CTM-GW se cultivaron con Stempro® Osteogenesis Differentiation y Stempro® Adipogenesis Differentiation (USA) durante 21 días. Para comprobar la diferenciación se realizó: a) Tinción con rojo de alizarina S (1,2-dihidroxiantraquinona) (Merck Mlipore, USA): las células se lavaron con PBS y fijaron con formol al 10% durante 10 minutos, en seguida se agregó rojo de alizarina S (1,2-dihidroxiantraquinona) durante 10 minutos, se realizaron dos lavados con PBS. b) Tinción con rojo oleoso: las células se fijaron con formol al 10%, tiñeron con rojo Oleoso (Sigma-Aldrich,USA) en isopropanol al 60 % (Sigma-Aldrich, USA) por 10 min, y se lavaron en dos ocasiones con isopropanol al 60%. 3) Expresión de antígenos de superficie; las células se lavaron con PBS y se les agregó EDTA (ácido etildiaminotetraacético) 2mM (Research Organics, USA) para desprenderlas mediante raspado. Una vez en suspensión con NaCl 0.9 % se incubaron con los siguientes anticuerpos anti-humano; anti-HLA-DR (cat. sc-3939); anti-CD34 (cat. Sc-343503); anti-CD45 (cat. MA1-12219, Thermo Scientific); anti-CD105 (cat. 323204); anti-CD73 (cat. 344004) y anti-CD90 (cat. 328108, Biolegend), lavaron con PBS y centrifugaron a 3000 rpm por 1 min. El botón celular se resuspendió en paraformaldehído (Sigma-Aldrich, USA) al 2 %, la lectura se realizó en un citómetro de flujo FACScalibur (Becton Dickinson, USA). Los resultados obtenidos se reportaron como porcentaje de células positivas para cada marcador tomando como 100 % el número total de eventos analizados.
Separación en etapas de estudio
El área de las heridas y el consumo de antiinflamatorios no esteroideos fueron estudiados en tres etapas diferentes: terapia convencional (TC); desde el momento de la valoración inicial (semana -6) al inicio del tratamiento (semana 0), 1er Dosis (1er-D); desde el inicio del tratamiento (semana 0) hasta la segunda aplicación (semana 4), y finalmente, 2da Dosis (2da-D); que abarcó desde el momento de la segunda aplicación (semana 4) hasta que las pacientes abandonaron el tratamiento (semana 9 aproximadamente).
Aplicación de CTM-GW en pacientes
Para realizar la aplicación de las CTM-GW en los pacientes se realizaron los siguientes pasos; 1) Cuantificación del área de la herida. Para calcular el área de daño se obtuvieron imágenes con una cámara digital Samsung-ST150F 16.2-Megapixel (modelo: EC-ST150FBPBUS) y el área se determinó con el programa ImageJ 1.46r, los valores obtenidos fueron expresados en centímetros cuadrados (cm2), 2) Preparación de la herida. Se realizó la curación con jabón quirúrgico neutro Antibenzil (1 g de cloruro de benzalconio · 100 mL-1 de vehículo) (Altamirano farmacéuticos), solución salina al 0.9% (PISA farmacéutica), 3) Preparación de las células para su aplicación: Las CTM-GW fueron despegadas con tripsina/EDTA (Sigma-Aldrich, USA), y se aplicaron 100,000 ± 10,000 células ∙ cm-2 de herida, 4) Colocación del Surgicel® (Ethicon, USA): en el caso 2 se colocó una malla de celulosa regenerada oxidada absorbible 35 x 5 cm2 a la herida mediante puntos quirúrgicos con sutura Catgut crómico 3/0 (Ethicon, USA), 5) Aplicación de las CTM-GW. Se realizó directo en la herida mediante infiltración intradérmica e irrigación en el lecho de la herida en dos ocasiones, el día de la primera aplicación se consideró como día 0 y la segunda dosis se realizó a la cuarta semana, por último las lesiones se protegieron con un apósito hidrocoloide DuoDERM® (ConvaTec, Nordic Capital y Avista Capital Partners), gasas y apó-sitos estériles hasta la valoración de las mismas.
Histología
Los cortes histológicos fueron teñidos con Hematoxilina y Eosina (H-E), las biopsias se tomaron antes de iniciar el tratamiento y a los 30 días de la primera aplicación, fijaron con formol al 10 % amortiguado (formaldehido 4%, NaH2PO4·H2O 4 g, Na2HPO4·7H2O 6.5 g · H2O 1000 mL-1), fueron incluidos en parafina, se realizaron cortes semifinos de 4-7 μm, se montaron en portaobjetos, Tinción por Hematoxilina y Eosina: las laminillas con los tejidos se desparafinaron, hidrataron y tiñeron con Hematoxilina de Harris. Posteriormente, las laminillas se lavaron con agua corriente, contrastaron con eosina, deshidrataron, aclararon y montaron con resina de metacrilato/Acrilato (Entellan® Merck, Alemania).
Respuesta de la lesión
La recuperación de la lesión fue determinada al plantear el índice úlcera, que se interpretó por el porcentaje del área de la herida abierta remanente con respecto al área de la herida al inicio del tratamiento. También se expresó la tasa de recuperación (Tr) de la herida como el cociente Tr=Ar/tr, donde Ar es el valor del área recuperada (cm2) durante el tratamiento, y tr son los días que duró la recuperación del área. Las extensiones de las áreas ulceradas y recuperadas fueron evaluadas a través del análisis de imágenes con el programa ImageJ.
Resultados
Caracterización celular
Morfología fibroblastoide y adherencia a las placas de cultivo: las células aisladas mostraron una morfología alargada que asemejaba a fibroblastos, característica relacionada con la adherencia de las CTM a la placa de cultivo (Figura 1A).

Figura 1 Obtención y caracterización de las CMM-GW. (A) Cultivos celulares en 6º pase, (↑) células de forma fibroblastoide. (B) Células en medio de diferenciación osteogénica, (↑) acúmulos de Ca++ y fosfato extracelular teñidas con rojo de alizarina. (C) Células en medio de diferenciación adipogénico, (↑) con vesículas lipídicas intracelulares teñidas con rojo oleoso. (D) Análisis de la expresión de proteínas hematopoyéticas de superficie por citometría de flujo de 10 mil eventos celulares.
Diferenciación osteogénica: los cultivos mostraron positividad para la tinción de rojo de Alizarina, lo que indica la presencia de Ca++ y fosfatasa alcalina como distintivo de las células mesenquimales diferenciadas a osteoblastos (Figura1B).
Diferenciación adipogénica: en los cultivos mantenidos con medio adipogénico se pudieron apreciar pequeñas vesículas lipídicas en el citoplasma, positivas para la tinción de rojo Oleoso, específico para los adipocitos (Figura 1C). Expresión de antígenos de superficie: los marcadores de superficie que se analizaron para las células aisladas fueron CD90/CD73 (93.38% de positividad) y CD105 (35.98% de células positivas), mientras que la expresión de antígenos hematopoyéticos HLA-DR, CD34 y CD45 estuvo prácticamente ausente (0.04 y 0.16%, respectivamente) en los cultivos (Figura 1D). Con ello se cumplieron los criterios propuestos por la ISCT.
Respuesta de la lesión hacia el tratamiento
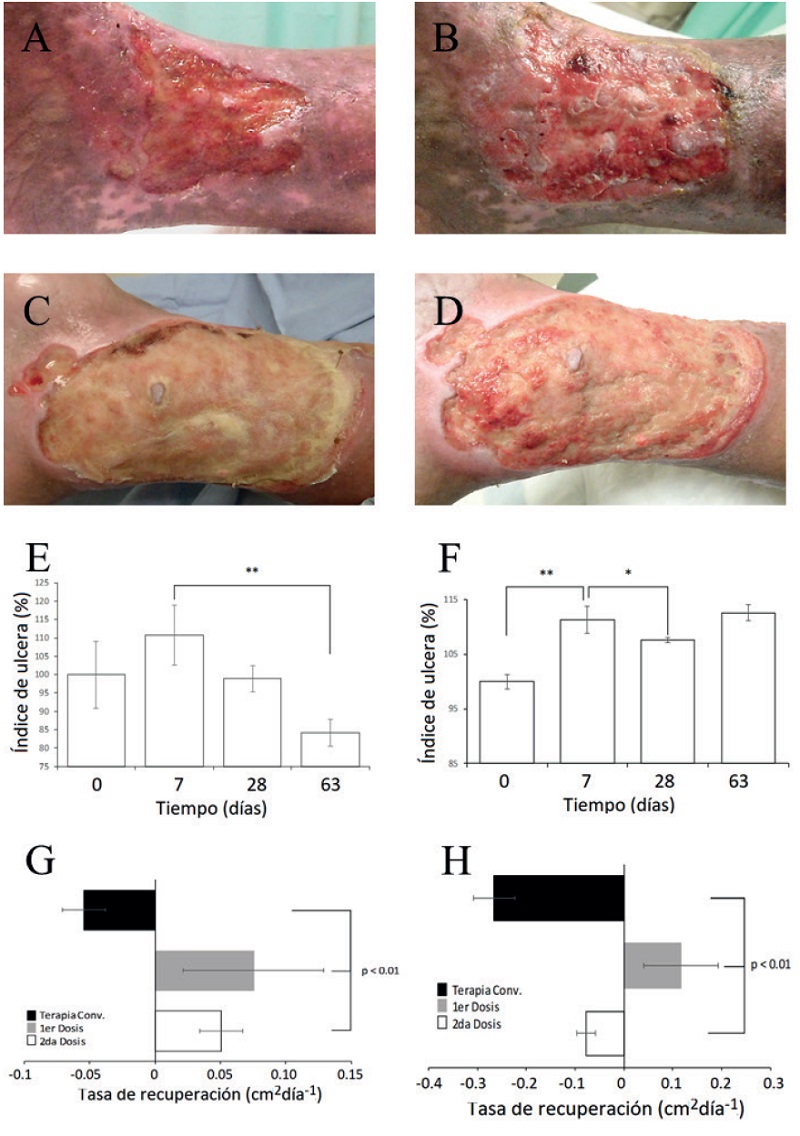
Caso 1; la Figura 2A muestra la herida al día 0 del tratamiento, donde se puede observar un estado eritematoso y exudativo, sin evidente proceso de infección en la zona, por otro lado, la Figura 2B obtenida al séptimo día de la primera aplicación de las mesenquimales donde es posible apreciar la formación de tejido en el lecho de la misma. Caso 2; la Figura 2C muestra el área de lesión recubierta por la malla de Surgicel® al inicio de la aplicación celular. En la Figura 2D se aprecia la formación de tejido sobre la malla colocada al inicio del tratamiento, con lo que se disminuyó la profundidad de la lesión. Para representar el beneficio del tratamiento con células solamente y células en Surgicel®, se llevó a cabo un análisis de índice de úlcera y tasa de recuperación, las cuales se describen a continuación.
Índice de úlcera y tasa de recuperación
En el caso 1; durante el periodo de observación se pudo apreciar un incremento en el porcentaje del área al día 7 (Figura 2E), sin embargo, al término del tratamiento (día 63), la herida mostro una disminución del área de lesión. Por otro lado, con el análisis de las áreas de herida se calculó la tasa de recuperación de herida, en el cual se demostró que con el tratamiento convencional este valor era negativo (-0.05), lo que señala un aumento en el área afectada. Posteriormente, con el tratamiento de células mesenquimales, la tasa de recuperación mostró valores significativamente positivos (0.05 y 0.10), lo que indica un índice de recuperación de herida favorable.
En el caso 2 esta paciente mostró un área de herida incrementada con el tratamiento convencional (Figura 2F, día 0); e igual que pasó en el caso 1, el índice de úlcera aumentó al día 7; no obstante, en el día 28 posterior a la primera aplicación el índice de úlcera alcanzó a disminuir y se mantuvo en el tiempo hasta el día 63 (Figura 2F). Por otro lado, el análisis de la tasa de la recuperación de la herida mostró valores negativos con el tratamiento convencional (0.3, Figura 2H) y aunque alcanzó valores positivos (0.15 en la primer dosis), subsecuentemente se reflejó en un valor negativo en la tasa de cierre; sin embargo, éste número negativo se mantuvo menor al 0.1, que fue menor al que se presentó al inicio del tratamiento (Figura 2H), lo que refleja que con el tratamiento número 2 las condiciones de úlcera mejoraron con el material Surgicel®.
Análisis histológico de las úlceras antes y después del tratamiento
En los resultados de las tinciones por H&E para el caso 1; fue posible apreciar previo al tratamiento, un infiltrado inflamatorio perivascular así como microangiopatía (3A, flechas) y las fibras depositadas en el área de lesión (3A, asteriscos). Después de administrarse la aplicación de células mesenquimales (Figura 3B), el infiltrado inflamatorio disminuyó (3B, flechas) y las fibras de colágeno fueron más abundantes (3B, asteriscos), delimitando los nuevos vasos sanguíneos que son perceptibles en la tinción (3B, cabezas de flecha obscuras). En el caso 2, previo a la aplicación de las células mesenquimales (Figura 3C), se aprecian extensas zonas de necrosis (3C, estrellas), edema (3C, cabezas de flecha claras), infiltrado inflamatorio perivascular, vasculitis, microangiopatía (3C, asteriscos) y microcoágulos de fibrina en vasos sanguíneos. En esta paciente se presentaron mayores beneficios por el tratamiento de la ulcera con las células mesenquimales y Surgicel®, que fueron observados en los cortes histológicos (Figura 3D); donde la zona de necrosis fue desplazada (3D estrellas) por un aumento de células que conformaron una zona de proliferación vascular. Debido a lo anterior, la conformación del tejido puede verse más sólido, como se mostró en las fotos de la lesión de la Figura 2.
Discusión
El desarrollo de estrategias de medicina regenerativa o terapia celular con células troncales mesenquimales ha demostrado tener resultados a corto plazo, además de aminorar los costos en el sector salud [25, 26]. Para ello es importante que la obtención no sea invasiva, que sea posible su trasplante autólogo o alogénico, que el aislamiento y cultivo se basen en las buenas prácticas de manufactura y por último, cumplir con los postula-dos propuestos por la sociedad internacional para la terapia celular (ISCT) [27].
Las úlceras son lesiones cutáneas de tamaño y forma variable que persisten por más de 6 semanas que no responden a tratamiento convencional, por lo que se transforman en crónicas [28]. Estas heridas se caracterizan por presentar alteraciones en la estructura microvascular que se favorece por diferentes comorbilidades metabólicas preexistentes, y por lo tanto, su tratamiento resulta difícil, largo y costoso, afectando de forma importante la calidad de vida del paciente [28-30].
En este trabajo se aplicó terapia regenerativa a partir de CTM derivadas de gelatina de Wharton (tejido de cordón umbilical de obtención no invasiva) en úlceras crónicas. Las CTM fueron aisladas y caracterizadas en base a los criterios propuestos por la ISCT [27]. Primeramente, la naturaleza troncal de las células fue evidenciada por presentar morfología de tipo fibroblastoide, adherencia a los recipientes de cultivo, capacidad de diferenciación tanto osteogénica como adipogénica, y se identificaron los antígenos de superficie CD90, CD73 y CD105, por lo que los cultivos utilizados en este estudio cumplieron los criterios para ser utilizados en terapia [27].
Las ulceras crónicas de pacientes con diabetes mellitus recientemente han sido tratadas con CTM de diferentes fuentes como M.O. [31, 32], tejido adiposo [33, 34, 35] y piel [36]. En este trabajo, se confirmó lo reportado previamente por muchos investigadores, donde las CTM suprimen la inflamación excesiva, estimulan la angiogénesis de novo, facilitan la cicatrización y reducen el tamaño de la herida, por lo que brinda enormes posibilidades para la sanación de dichas úlceras [37]. Las características histológicas macroscópicas y físicas de la herida (inflamación evidente, apertura de herida) después de la primera aplicación, mostraron la formación de tejido de granulación y fibrótico al séptimo día del tratamiento con las CTMs. La cicatrización fue más evidente en el caso 2 (Figura 2c y d), donde se utilizó la malla de Surgicel® [38]. Se pudo observar un efecto aditivo de las CTM con el Surgicel. Para éste último, se han descrito los beneficios en casos de úlceras pero sin aplicación de CTM [39], por lo que al utilizarlo en con-junto con las CTM tuvo mayores beneficios. Chen y cols., (2015) [40] en un modelo de ratón, demostraron que las CTM-MO en combinación con un hidrogel n-isopropilamida (NIPAM) a los 35 días post-implante una disminución de la inflamación, formación de tejido de granulación, aumento de macrófagos M2, angiogénesis y regeneración tisular.
En nuestro trabajo, a los 65 días post-tratamiento encontramos que disminuye el tamaño de la lesión y presencia de formación de vasos sanguíneos. Cabe señalar que el tamaño de las lesiones en el modelo murino es muy pequeño (aproximadamente 0.5 cm2) a comparación de las lesiones de nuestros pacientes (aproximadamente 10 x 7 cm2) por lo que la diferencia es muy marcada entre ambos grupos de trabajo [40].
Las CTM estimulan diferentes mecanismos moleculares y celulares [41-44], por ejemplo: a) Se promovió la diferenciación de las CTM a diferentes tipos celulares [41] como células endoteliales [29], pericitos [45], musculo liso [46], fibroblastos [47-49], miofibroblastos [50, 51] o queratinocitos [52], todas ellas indispensables en los procesos de angiogénesis [29, 53] y regeneración de piel [25, 440 33]; b) probable liberación de diferentes factores de crecimiento y citocinas que promueven la proliferación de las células residentes [41] y c) las CTM reestructuraron el microambiente, mejorando las condiciones para la regeneración tisular [41].
Ya que las úlceras crónicas presentan sucesiones continuas de inflamación (afectando la formación de tejido y remodelación), no se concluye su cicatrización o regeneración, ocasionando que se retrase el cierre de la herida [54]. En este estudio, los análisis histopatológicos iniciales para ambos casos, mostraron procesos inflamatorios crónicos como microangiopatía y zonas de fibrosis y necrosis (típico de dichas lesiones) [54-56]; sin embargo, a partir del tratamiento con las CTM fue posible apreciar en los dos casos una disminución de la cantidad de linfocitos infiltrantes, que se relaciona a la capacidad inmunomoduladora de las células mesenquimales en presencia de ambientes inflamatorios crónicos, permitiendo así la regeneración de piel. [41, 52, 54]. Lo anterior conlleva a un incremento en la cantidad y calidad de vasos sanguíneos formados [57, 58], los cuales también fueron observados en los cortes histológicos de las pacientes con tratamiento. El efecto que se mostró a corto plazo al aplicar las CTM-GW sobre el cierre de las heridas crónicas, concuerda con los resultados de Navone (2014) [59] quien utilizó un andamio de fibroína y CTM, donde la herida se reduce en un 40%. Kazohide M., y colaboradores (2015) [60] utilizaron células sobre un hidrogel de ácido hialurónico al 4% y se redujo la ulcera a los 28 días post-tratamiento (similar a nuestros resultados). Por otro lado, el grupo de Wu y cols (2017) [61] demostró que el uso de CTM derivadas de placenta redujo el tamaño de las lesiones en 51% de los pacientes en un plazo mayor que este estudio (3 meses postrasplante). Ribeiro y cols., (2014) [62] observaron que las CTM-GW (1 x 105/cm2) incluidas en un hidrogel de polivinil alcohol, a los 60 días post-tratamiento la herida sana al 100%, así los cortes histológicos mostraron reepitelización, tejido de granulación y formación de vasos sanguíneos en la herida. En este trabajo solo muestra reducción de la herida y la formación de vasos sanguíneos. Sin embargo hay que destacar que las ulceras crónicas son de pacientes diabéticos e insuficiencia venosa periférica crónica con más de 3 y 5 años de evolución [62].
Al realizar el análisis del área de la herida, se pudo observar una apertura considerable en la lesión que llevaba largo tiempo con terapia convencional, lo que indica que ésta no fue suficiente para favorecer el cierre; sin embargo, después de la primera dosis se pudo apreciar una disminución del área que se mantuvo en el tiempo. Esta mejoría pudiera deberse al efecto de las citocinas secretadas por las células mesenquimales sobre los fibroblastos o miofibroblastos [50], además de los otros efectos de las CTM ya mencionados. Aunque el análisis de la herida mostró mejoría debido al tratamiento, la lesión no se recuperó en su totalidad; nosotros proponemos ajustar a una mayor dosis celular y al menos otras dos aplicaciones, sobre todo por la extensión de la lesión. Por otro lado, en el caso 2 se demostró que la aplicación de células en conjunto con materiales que promueven el soporte celular (en este caso utilizamos un producto derivado de la oxidación de la celulosa) [38], es una mejor alternativa para recuperar el tejido en menor tiempo, por lo que la medicina regenerativa en este tipo de lesiones, pueda dar paso al siguiente nivel, que es la “ingeniería de tejidos”, donde se puede utilizar la piel autóloga, alogénica o sintética [25, 52], así como biomateriales, con el fin de potencializar la resolución de las heridas flebostáticas crónicas.
Conclusiones
La terapia celular con aplicación de CTM provenientes de gelatina de Wharton sobre úlceras flebostáticas de difícil manejo, es adecuada y representa una interesante alternativa médica por sus resultados a corto plazo, y podría aplicarse en otros tipos de lesiones. Además de lo anterior, la utilización de materiales como el producto de la oxidación de la celulosa, permite una mejor regulación de los procesos inmunológicos y modeladores del tejido; esto abre las puertas para que en este tipo de lesiones se aplique la ingeniería de tejidos en conjunto con células troncales. Lo anterior, también representaría una reducción del tiempo de convalecencia.











 nueva página del texto (beta)
nueva página del texto (beta)