Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos de cardiología de México
versión On-line ISSN 1665-1731versión impresa ISSN 1405-9940
Arch. Cardiol. Méx. vol.76 supl.4 Ciudad de México oct./dic. 2006
Investigación básica
Filamina plaquetaria: Una proteína del citoesqueleto integradora de la función celular+
Platelet filamin: A cytoskeletal protein involved in cell signal integration and function
Elizabeth García,* David Jay*
* Departamento de Biomedicina Cardiovascular, Instituto Nacional de Cardiología, Ignacio Chávez.
+ Este trabajo fue apoyado en parte por el donativo U40188–Q del Consejo Nacional de Ciencia y Tecnología (CONACYT) otorgado a David Jay.
Correspondencia:
Ma. Elizabeth García.
Departamento de Biomedicina Cardiovascular,
Instituto Nacional de Cardiología, Ignacio Chávez.
(INCICH Juan Badiano Núm. 1 Col. Seción XVI, Tlalpan 14080. México, D.F.).
Tel. 5573–2911 Ext. 1237 Fax 5573–0926.
Correo electrónico: gape3y1@yahoo.com
Resumen
La activación de receptores celulares por estímulos fisiológicos o exógenos produce cambios dramáticos en la forma y función celulares; tales cambios dependen principalmente de la reestructuración de la malla de actina. En plaquetas se ha obtenido mucha de la información sobre el citoesqueleto. Dentro de las proteínas entrecruzadoras de actina filamentosa (Actina–F) como la espectrina, la fimbrina o la alfa actinina, la Filamina A (FLNa) es la más eficiente en formar geles ortogonales tridimensionales de actina. Además, une al citoesqueleto periférico de actina con la membrana celular a través de su dominio C–terminal de unión a glicoproteínas de membrana. La filamina mantiene la citoarquitectura plaquetaria y es esencial para el movimiento y cambio de formas celulares que suceden durante la activación plaquetaria. Estudios previos han mostrado que una gran variedad de proteínas con distintas funciones tales como traducción de señales, regulación de la transcripción de genes y movilización de receptores se asocian a la filamina, sugiriendo que ésta puede actuar como andamiaje u organizador de proteínas. El propósito de esta comunicación es el de describir brevemente las características de las macromoléculas asociadas a la FLNa plaquetaria y discutir un posible papel de la asociación de éstas a la filamina.
Palabras clave: Activación plaquetaria. Citoesqueleto. Filamina A. Plaquetas. Receptor de von Willebrand. Integrina llb/llla.
Summary
Activation of cellular receptors by diverse stimuli induces dramatic changes in shape and function to respond to the new circumstances of the cell. This modified behavior depends on the reorganization of the peripheral actin meshwork. An outstanding example of these processes can be found in platelets, from which much of the information available on cytoskeletal function has been obtained. Among the many actin–crosslinking proteins like spectrin, fimbrin or alpha actinin, filamin a (FLNa) emerges as the one with the highest potential in initiating the polimerization of actin filaments (F–actin) during the formation of tridimensional actin gels. FLNa also links actin filaments to the cytosolic domain of many membrane glycoproteins in platelets through its C–terminal region. In addition to participating in cell shape changes, FLNa is a scaffoldding protein that recruits numerous proteins involved in a completely different set of functions, including signal transduction, gene transcription regulation, and receptor translocation; however, the physiological role of FLNa in these processes has remained elusive. The purpose of the present communication is to briefly describe the characteristics of the macromolecules able to interact with FLNa and to discuss a possible role of FLNa during the transduction of signals from those molecular elements in platelets.
Key words: llb/llla Integrin. Cytoskeleton. Filamin A. Platelets. Platelet activation, von Willebrand receptor.
Las actividades del citoesqueleto dependen de tres tipos de filamentos, a saber: a) filamentos de actina (microfilamentos), formados por monómeros de actina y proteínas accesorias entrecruzadoras de actina, entre las que destaca la filamina, b) microtúbulos formados por tubulina y proteínas accesorias a ésta, como la proteína tau y c) filamentos intermedios que incluyen proteínas como la vimentina o la laminina. Cada uno de estos sistemas regula actividades fundamentales para la célula.
La reorganización tridimensional del citoesqueleto de actina permite varias funciones celulares tales como: cambios de forma, movimiento celular, división celular, fagocitosis y otros procesos que involucran un cambio celular en respuesta a estímulos externos. Los microfilamentos son polímeros del monómero de actina, subunidad proteica de 43 KDa denominada actina globular o actina G. Los filamentos de actina crecen por la adición de actina G en sus extremos, formando la actina filamentosa o actina F. In vitro, la actina G unida a ATP polimeriza en presencia de K+ y Mg2. La eventual hidrólisis de ATP para generar ADP hace a los filamentos inestables y susceptibles de reorganización al generar de nueva cuenta los monómeros originales.1 La importancia de la funcionalidad de los microfilamentos reside en la variabilidad de proteínas asociadas a ellos, (Tabla I).1,2 Dentro de las proteínas asociadas a actina está la filamina, filamina no muscular o FLNa (ABP, ABP–280 KDa o "Actin–Binding Protein") que es una fosfoproteína homodimérica, que entrecruza los filamentos de actina en una malla tridimensional citosólica. La filamina es la proteína más eficiente en iniciar la gelación de la F–actina, además de que une al citoesqueleto periférico de actina con la membrana celular a través de su dominio C–terminal de unión a glicoproteínas (GP), como el receptor del factor von Willebrand Gplb–V–IX o el receptor de fibrinógeno, GP Ilb/IIIa.3–5 En esta comunicación se describe la función de cada una de las proteínas asociadas a los filamentos de actina a través de la filamina. Así mismo, discutimos el posible papel de la filamina durante la señalización iniciada por las moléculas accesorias a ésta.
La filamina tiene una amplia distribución filogenética. La secuencia completa de nucleótidos de filamina obtenida de una genoteca derivada de células endoteliales (cADN de ABP) predice que cada subunidad de 280 KDa está constituida por 2,647 aminoácidos. Los dominios funcionales de cada subunidad incluyen una región N–terminal (estructura alfa hélice), de unión a actina F, también conocida como ABD ("Actin–Binding–Domain") de homología con calponinas y con proteínas presentes en vías de transducción de señales como Vav y IQGAP. Estudios recientes sugieren que la unión de ABD a actina es regulada por Calcio/Calmodulina. También tiene un dominio C–terminal de autounión y de unión a glicoproteínas de membrana.6 El resto de la proteína está constituida por 24 repetidas de 96 aminoácidos cada una en estructura beta plegada antiparalela. La filamina tiene dos sitios suceptibles a proteólisis por calpaína entre las repetidas 23 y 24 y un fragmento adicional entre las repetidas 15 y 16, generando un fragmento N–terminal de 180 KDa, y un fragmento C–terminal de 100 KDa que por acción prolongada de la calpaína puede originar un fragmento de 90 KDa y un péptido C–terminal de 10 KDa3,6 (Fig. 1).

Cuando la secuencia completa de nucleótidos de la filamina fue deducida, el análisis de la secuencia deducida de aminoácidos permitió predecir la existencia de múltiples sitios potenciales de fosforilación para diversas cinasas: tres sitos para proteína cinasa dependiente de AMP cíclico (PKA), treinta y tres sitios para proteína cinasa C (PKC), treinta sitios para caseína cinasa II (CCII), e inclusive unos sitios para tirosina cinasa (YC). De hecho existen más de 380 residuos de serina/treonina en la filamina.
Hay tres isoformas de filamina en mamíferos A, B y C. La filamina A se encuentra ampliamente distribuida en células no musculares, por ejemplo plaquetas y células endoteliales.7 La filamina B se encuentra principalmente en células musculares y la filamina C, se encuentra en músculo esquelético y cardíaco en la edad adulta.8 La localization en el genoma de los tres genes de filamina es altamente conservada. Los tres isotipos de filamina muestran entre sí 60% – 80% de homología en las secuencias completas, con excepción de las dos regiones bisagra, susceptibles a corte por calpaína, las cuales muestran grandes divergencias.4,6,7
La estructura de los dímeros de filamina es similar a una inmunoglobulina, su estructura flexible puede inducir ramificaciones ortogonales de actina–F de gran ángulo. Los ángulos formados entre los monómeros de filamina son inversamente proporcionales a la concentración de filamina en plaquetas.4 La formación de ases paralelos de filamentos de actina es promovida cuando la proporción molar de filamina a actina es 1:10–50, mientras que una estequiometría de 1:150–740 lleva a la formación de redes ortogonales de actina. Existen varios tipos de entrecruzamiento de la actina causados por la filamina (tipos X, T o Y).
Papel del citoesqueleto de actina y de la filamina en la plaqueta
Las plaquetas son estructuras celulares anucleadas que se forman en la megacariocitopoyesis a nivel de la médula ósea, por fragmentación de la membrana plasmática de los megacariocitos, para posteriormente distribuirse por el torrente sanguíneo. El citoesqueleto de la plaqueta consiste en una red de estructuras filamentosas que mantienen la forma discoide de la plaqueta en reposo.9,10 Incluyen filamentos de actina,11,12 el anillo marginal de microtúbulos,13 moléculas de miosina14 así como moléculas de unión a actina como filamina, espectrina, vinculina, talina, tropomiosina entre otras, todos ellos formando el esqueleto membranal y citoplásmico plaquetario (Fig. 2). Por otro lado, el citoesqueleto tiene el papel de dirigir y promover los rápidos cambios de forma inducidos por la activación plaquetaria.15

Los procesos de adhesión y activación plaquetaria cumplen un papel fisiológico esencial en la formación del coágulo ante un daño tisular. También constituyen un elemento central durante eventos patológicos tromboembólicos y todo esto se inicia después de la unión de receptores de superficie específicos hacia componentes tales como la colágena, trombina, vWF y ADP.14 Cuando las plaquetas se activan ocurre una rápida polimerización de filamentos de actina que determina el cambio de forma discoide a la forma extendida que involucra la formación de estructuras denominadas filopodia y lamelipodia. La secreción del contenido granular, así como la expresión de substancias procoagulantes en la superficie plaquetaria que conducen a la agregación para la formación de un coágulo son eventos paralelos y sinérgicos.16–20 Los cambios inducidos por la activación plaquetaria resultan de procesos como la fosforilación/defosforilación y ruptura proteolítica por calpaína de proteínas del citoesqueleto. La reorganización específica depende de la combinación de señales a las que la plaqueta está expuesta. De esta manera los cambios antes mencionados van acompañados de la activación de diversas familias de proteínas cinasas y la subsecuente fosforilación de un gran número de proteínas. A este respecto estudios han mostrado que el citoesqueleto es un blanco principal de estas enzimas.21
Regulación de la filamina por fosforilación
Como ya se mencionó, la FLNa es una fosfoproteína. A este respecto, estudios previos mostraron que la FLNa, aislada de plaquetas humanas, es una mezcla de formas fosforiladas en distinto grado desde 18 hasta 40 moles de fosfato/mol de monómero de ABP.21,22 De hecho, se ha demostrado que la fosforilación/defosforilación de la filamina es un evento importante, involucrado en la reorganización del citoesqueleto de actina durante la activación plaquetaria.21 Este proceso no sólo modula la habilidad de la filamina de entrecruzar filamentos de actina sino que también, al ser fosforilada por la cinasa dependiente de AMPc (PKA) disminuye la susceptibilidad de ésta a la degradación por calpaína,22 una cisteín proteasa dependiente de calcio cuya actividad da cuenta de más del 95% de la actividad total proteolítica de la plaqueta y cuya presencia también ha sido demostrada en una gran diversidad de tejidos, incluyendo el endotelio.23–26
Interacción de la filamina con otras proteínas
En los últimos años, se ha encontrado que una amplia variedad de proteínas se une a la filamina (más de 20 hasta la fecha), incluyendo receptores transmembranales y moléculas de señalización (Fig. 3) y la mayoría de éstas interaccionan con el extremo C–terminal de la filamina.27
De esta manera, la filamina, al unir una gran variedad de moléculas tendría un papel fundamental, no únicamente como estructuradora del citoesqueleto, sino también como molécula mediadora de señales a partir de los cambios o rearreglos generados en la malla de actina en respuesta a diversos estímulos. En la Tabla II se muestran algunas de las principales moléculas accesorias de la filamina y se resumen las principales características funcionales de ellas. En este punto, cabe mencionar que no se sabe hasta la fecha si los procesos de fosforilación/defosforilación recién mencionados de la FLNa y la subsecuente reorganización del citoesqueleto jueguen algún papel en la señalización derivada a partir de estas moléculas accesorias. A continuación describiremos brevemente algunas de las interacciones más importantes, que pueden jugar un papel principal en la función plaquetaria, asimismo, expondremos un posible papel para la fosforilación de la FLNa en este proceso.
Recientemente se resolvió la estructura cristalina del complejo FLNa–integrinas β.51 Se determinó que la repetida 21 de la FLNa brindaba la interfase apropiada para unir a la proteína con el dominio citoplásmico de la integrina.
Como se menciona más adelante, la determinación de esta estructura brindó un marco conceptual para entender aspectos de la función de las integrinas. En este momento cabe recordar, que la habilidad de los receptores de adhesión (integrinas) de transmitir señales químicas y de fuerza mecánica a través de la membrana celular, depende, en última instancia, de su interacción con el citoesqueleto subyacente. Así, previamente, se había demostrado que el receptor GPIb–V–IX (receptor del factor vW) estaba vinculado a la malla periférica de actina a través de su unión con la FLNa.52,53 La interacción se da con el dominio citoplásmico de la glicoproteína IB, en particular con la GP Iba. La glicoproteína IB (GP Ib) es una glicoproteína de la membrana plaquetaria compuesta de un heterodímero, una cadena alfa y una cadena beta, unidas por puentes disulfuro. La Gplb funciona como receptor del factor von Willebrand (vWF) y es también el receptor de alta afinidad para trombina54 (Fig. 4). El complejo de receptores incluye la asociación no covalente de las subunidades alfa y beta con las glicoproteínas IX y V en plaquetas. La unión del complejo GP Ib–IX–V al vWF facilita la adhesión inicial plaquetaria al endotelio vascular después del daño vascular, y también inicia eventos de señalización, activación plaquetaria, trombosis y hemostasis. Varios polimorfismos y mutaciones se han descrito en el gen que codifica para la subunidad alfa de este receptor, algunos de ellos son la causa del síndrome de Bernard–Soulier y plaquetas con el fenotipo patológico de von Willebrand.55
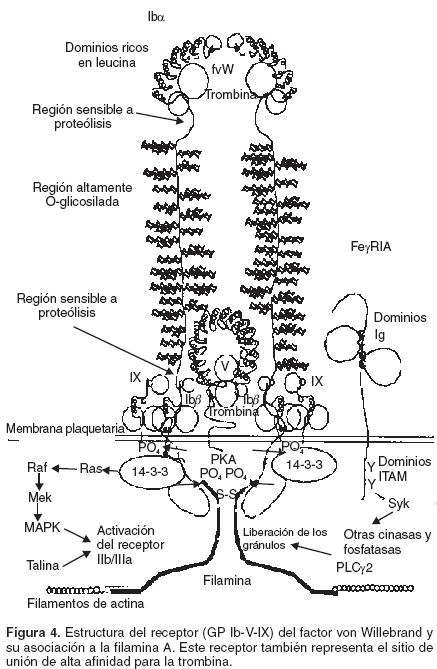
Un dato fundamental que se encontró con la resolución del modelo atómico de la interacción FLNa–integrina fue que el sitio de unión de la FLNa a la integrina se traslapaba con el sitio de unión de la talina (otra proteína entrecruzadora de actina) a la integrina. Es decir, la FLNa y la talina competían por su unión a la integrina. Datos previos habían demostrado que la talina era la principal proteína encargada de iniciar la activación de adentro hacia afuera ("inside–out activation") del receptor Ilb/IIIa (αIIb/β3) del fibrinógeno a través de su unión al dominio citoplásmico de la integrina β3.56 Como se recordará, en plaquetas en reposo el receptor Ilb/IIIa es incapaz de unir fibrinógeno con afinidad elevada. Sin embargo, cuando las plaquetas son activadas por distintos agonistas como la trombina, el ADP, la epinefrina, el colágeno o endoperóxidos de prostaglandinas, la conformación de la GPIIb/IIIa cambia observándose una unión aumentada por el fibrinógeno.57 A este fenómeno es al que se le llama activación de adentro hacia afuera y depende de la preactivación plaquetaria. Datos previos han mostrado que durante la activación plaquetaria la FLNa es fragmentada por proteasa neutra dependiente de calcio (calpaína)22,58,59 y que los fragmentos producto de esta hidrólisis pueden ser liberados de la membrana para participar en vías de señalización corriente abajo.60 Como se menciona enseguida, estos productos de degradación pueden participar en eventos posteriores durante la agregación plaquetaria y además liberarían a la integrina β que ahora estaría en posibilidad de ser activada por la talina; brindando una explicación para el mecanismo molecular de activación de adentro hacia fuera del receptor de fibrinógeno.
Como se mencionó, otro ejemplo en donde la FLNa puede jugar un papel principal en la vía hemostática, mediada por su interacción con otras macromoléculas, es durante la agregación plaquetaria, especialmente en la formación de las protuberancias de la membrana plaquetaria (filopodia) que se observan durante la generación y posterior retracción del coágulo.15 Estudios previos habían mostrado que la inhibición plaquetaria por agentes que elevan la concentración de AMP cíclico (AMPc) tales como la prostaciclina protegían a la FLNa de la degradación por calpaína.22 Esto permitía mantener una red íntegra de la malla periférica de actina evitando los cambios de forma y estructura propios de la activación plaquetaria. Esta reducción de la susceptibilidad de la FLNa a calpaína se daba como consecuencia de su fosforilación por la Proteína Cinasa dependiente de AMPc (PKA).
Estudios posteriores mostraron que la fosforilación se efectuaba de manera específica en la serina 2152 localizada en el extremo C–terminal de la proteína.58 Contrario a estas observaciones, Vadlamudi et al encontraron subsecuentemente que la fosforilación de este mismo residuo (Ser2152) por la Proteína Cinasa 1 activada por p21 (Pak 1) iniciaba la reorganización de la red de actina, generando fenómenos dinámicos en la membrana celular.61 Ellos también encontraron una acción recíproca entre Pak 1 y FLNa es decir, Pak 1 fosforilaba a la FLNa y la FLNa activaba a Pak 1. Más recientemente, nosotros propusimos un modelo que podía resolver esta contradicción y que además sugería una función nueva para la FLNa.60 Como ya se ha mencionado, la activación inicial de las plaquetas es capaz de inducir la hidrólisis de la FLNa por calpaína. La proteólisis de la proteína, a su vez, libera fragmentos de la FLNa desde sus sitios de anclaje en la membrana. Como se muestra en la Tabla II, la región C–terminal de la FLNa es capaz de unir proteínas del grupo de las pequeñas GTPasas; en particular destaca la Cdc42.45 En este caso la unión de la GTPasa con la FLNa es independiente de GTP y hasta la fecha no se ha encontrado ningún efecto de Cdc42 sobre la FLNa. El modelo propuesto60 asume que el fragmento de FLNa liberado de la membrana es capaz de transportar a la GTPasa hasta el dominio CRIB de Pakl, que es el sitio en donde Cdc42 se une a la cinasa cuando su actividad es estimulada por autofosforilación.62 Posteriormente, Pak 1 activado por el complejo FLNa fragmentada–Cdc42 sería capaz de refosforilar a la FLNa que no fue digerida por la calpaína durante la posterior formación de filopodia durante la activación plaquetaria.
En conclusión, podemos decir que a partir de su papel central como estructuradora de la malla de actina plaquetaria, la FLNa puede ejercer funciones fundamentales adicionales como integradora de vías de señalización. Es capaz, de esta manera, de integrar señales mecánicas desde receptores de adhesión hacia el citoesqueleto como en el caso de la GP Ib–IX–V. Además, posterior a la estimulación por agonistas específicos, genera productos de degradación que por un lado permitirían la activación interna del receptor Ilb/IIIa de fibrinógeno y además mediarían eventos en rutas corriente abajo importantes para la generación de fenómenos dinámicos de la membrana fundamentales para la formación y retracción del coágulo. Queda como importante campo de investigación resolver el papel que la FLNa pueda jugar en la señalización derivada de muchas de las otras macromoléculas accesorias a ella. Así como su participación en otros sistemas celulares.63
Referencias
1. Yang F, Condeelis J: Actin and associated proteins. Guidebook to the cytoskeletal and motor proteins. Kreis T, Vale R, Ed. A Sambrook and tooze publication at Oxford University Press, 1993, p. 3–20. [ Links ]
2. Ayscough KR: In vivo functions of actin–binding proteins. Curr Opin Cell Biol 1998; 10: 102–111. [ Links ]
3. Gorlin JB, Yamin R, Egan S, Stewart M, Stossel TP, Kwiatkowski DJ, Hartwig JH: Human endothelial actin–binding protein (ABP–280, non–muscle filamin): a molecular leaf spring. J Cell Biol 1990; 111: 1089–1105. [ Links ]
4. Stossel TP, Condeelis J, Cooley L, Hartwig JH, Noegel A, Schleicher M, Shapiro SS: Filamins as integrators of cell mechanics and signalling. Nat Rev Mol Cell Biol 2001; 2: 138–45. [ Links ]
5. Takafuta T, Wu G, Murphy GF, Shapiro SS: Human β filamin is a new protein that interacts with the cytoplasmic tail of glycoprotein Ibα. J Biol Chem 1998; 273: 17531–17538. [ Links ]
6. Arjan van der Flier, Sonnerberg A: Structural and functional aspects of filamins. Biochem Biophys Acta 2001; 1538:99–117. [ Links ]
7. Hartwig J, Stossel T: Isolation and properties of actin, myosin, and a new actin binding protein in rabbit alveolar macrophages. J Biol Chem 1975; 250: 5696–5705. [ Links ]
8. Maestrini E, Patrosso C, Manzini M, Rivella S, Rocchi M, Repetto M, Villa A: Mapping two genes encoding isoforms of the actin binding protein ABP–280, a dystrophin like protein, to Xq28 and to chromosome 7. Human Mol Genet 1993; 2: 761–766. [ Links ]
9. Isenberg WM, Bainton DF: Megakaryocyte and platelet structure. Hoffman R, Benz E J, Shatitil S J, Furie B, Cohen H J, Silberatein Hematology basic principles and practice. 2a. Ed. New York Churchill Livingston, 1995, p. 1516–1524. [ Links ]
10. Patel SR, Hartwig JH, Italiano JE: The biogenesis of platelets from megakaryocyte proplatelets. J Clin Invest 2005; 115: 3348–3354. [ Links ]
11. Debus E, Weber K, Osborn M: The cytoskeleton of blood platelets viewed by immunofluorescence microscopy. Eur J Cell Biol 1981; 24: 45–52. [ Links ]
12. Zobel, Manuel: The platelet reticular network. J Ultrastruct Res 1984; 89: 89–97. [ Links ]
13. White JG, Krumwiede M, Burris SM, Heagan B: Isolation of microtubule coils from platelets after exposure to aggregating agents. Am J Pathol 1986; 125: 319–326. [ Links ]
14. Tanaka K, Itoh K: Reorganization of stress like structures in spreading platelets during surface activation. J Struct Biol 1998; 124: 13–41. [ Links ]
15. Fox JE: Cytoskeletal proteins and platelet signaling. Thromb Haemost 2001; 86: 198–213. [ Links ]
16. Holmsen H: Prostanglandin endoperoxide–thromboxane synthesis and granule secretion as positive feedback loops in the propagation of platelet responses during "the basic platelet reaction ". Thromb Haemost 1977; 38: 1030–41. [ Links ]
17. Rosenberg S, Stracher A, Lucas RC: Isolation and characterization of actin and actin–binding protein from human platelets. J Cell Biol 1981; 91:201–211. [ Links ]
18. Rosenberg S, Lawrence J, Stracher A: Effect of various extraction solutions and thrombin activation on the composition of the platelet cytoskeleton. Cell Motil 1982; 2: 317–332. [ Links ]
19. Hartwig JH, Barkalow K, Azim A, Italiano J: The elegant platelet: signals controlling actin assembly. Thromb Haemost 1999; 82: 392–8. [ Links ]
20. Hartwig JH: The platelet: form and function. Semin Hematol 2006; 43: 94–100. [ Links ]
21.Wu MP, Jay D, Stracher A: Existence of multiple phosphorylated forms of human platelet actin binding protein. Cell Mol Biol Res 1994; 40: 351–357. [ Links ]
22. Chen M, Stracher A: In situ phosphorylation of platelet actin–binding protein by cAMP–dependent protein kinase stabilizes it against proteolysis by calpain. J Biol Chem 1989; 264: 14282–14289. [ Links ]
23. Phillips DR, Jakabova M: Ca2+ dependent proteases in human platelets specific cleavage of platelet polyp eptides in the presence of added Ca2+J Biol Chem 1977; 252: 5602–5605. [ Links ]
24. Zhang Z, Lawrence J, Stracher A: Phosphorylation of platelet actin binding protein protects against proteolysis by calcium dependent sulfhydryl protease. Biochem Biophys Res Commun 1988; 151: 355–360. [ Links ]
25. Jay D, Stracher A: Expression in Escherichia coli and phosphorylation with cAMP–dependent protein kinase of the N–terminal region of human endothelial actin–binding protein. Biochem Biophys Res Commun 1994; 202: 764–771. [ Links ]
26. Jay D, Stracher A: Expression in Escherichia coli, phosphorylation with cAMP–dependent protein kinase and proteolysis by calpain of a 71–kDa domain of human endothelial actin binding protein. Biochem Biophys Res Commun 1997; 232: 555–558. [ Links ]
27. Stossel TP, Condeelis J, Cooley L, Hartwig JH Noegel A, Schleicher M, Shapiro S: Filamins as integrators of cell mechanics and signalling. Nat Rev Mol Cell Biol 2001; 2: 138–145. [ Links ]
28. Xu WF, Xie ZW, Chung D, Davie E: A novel human actin–binding protein homologue that binds to platelet glycoprotein Ibα. Blood 1998; 92: 1268–1276. [ Links ]
29. Meyer SC, Zuerbiq S, Cunningham CC, Hartwig JH, Bissell T, Gardner K, Fox JE: Identification of the region in actin–binding protein that binds to the cytoplasmic domain of glycoprotein Ibα. J Biol Chem 1997; 272: 2914–2919. [ Links ]
30. Calderwood, D, Shattil S, Ginsberg M: Integrins and actin filaments: reciprocal regulation of cell adhesion and signaling. J Biol Chem 2000; 275: 22607–22610. [ Links ]
31. Ott I, Fischer E, Miyagi Y, Mueller B, Ruf W: A role for tissue factor in cell adhesion and migration mediated by interaction with actin–binding protein 280. J Cell Biol 1998; 140: 1241–1253. [ Links ]
32. Ohta Y, Stossel T, Hartwig J: Ligand–sensitive binding of actin–binding protein (ABP) to immunoglobulin G Fc receptor I(FcgRl, CD64). Cell 1991; 67: 275–282. [ Links ]
33. Liu G, Thomas L, Warren RA, Enns CA, Cunningham CC, Hartwig JH, Thomas G: Cytoskeletal protein ABP–280 directs the intracellular trafficking of furin and modulates protein processing in the endocytic pathway. J Cell Biol 1997; 139: 1719–1733. [ Links ]
34. Thompson TG, Cha TM, Hack AA, Brosius M, Rajala M, Lidov HGW, McNally ME, Watkins S, Kunkel LM: Filamin 2 (FLN2): a muscle–specific sarcoglycan interacting protein. J Cell Biol 2000; 148: 115–126. [ Links ]
35. Van der Ven PFM, Wiesner S, Salmikangas P, Auerbach D, Himmel M, Kempa S, HayeB K, Pacholsky D, Taivainen A, Schroder R, Carpen O, Fürst DO: Indications for a novel muscular dystrophy pathway: g–filamin, the muscle–specific filamin isoform, interacts with myotilin. J Cell Biol 2000; 151: 235–247. [ Links ]
36. Stahlhut M, van Deurs B: Identification of filamin as a novel ligand for caveolin–1: evidence for the organization of caveolin–1–associated membrane domains by the actin cytoskeleton. Mol Biol Cell 2000; 11:325–337. [ Links ]
37. Schwarzman AL, Singh N, Tsiper M, Gregori L, Dranovsky A, Vitek MP, Glabe CG, George–Hyslop PH, Goldgaber D: Endogenous presenilin 1 redistributes to the surface of lamellipodia upon adhesion of Jurkat cells to a collagen matrix. Proc Natl Acad Sci 1999; 96: 7932–7937. [ Links ]
38. Guo Y, Zhang S, Sokol N, Cooley L, Boulianne G: Physical and genetic interaction of filamin with presenilin in Drosophila. J Cell Sci 2000; 113: 3499–3508. [ Links ]
39. Li M, Bermak C, Wang Z, Zhou Q: Modulation of dopamine D2 receptor signaling by actin–binding protein (ABP–280). Mol Pharmacol 2000; 57:446–452. [ Links ]
40. Browne K, Johnstone R, Jans D, Trapani J: Filamin (280–kDa actin–binding protein) is a caspase substrate and is also cleaved directly by the cytotoxic T lymphocyte protease granzyme B during apoptosis. J Biol Chem 2000; 275: 39262–39266. [ Links ]
41. Edwards D, Towb P, Wasserman S: An activity–dependent network of interactions links the Rel protein Dorsal with its cytoplasmic regulators. Development 1997; 124: 3855–3864. [ Links ]
42. Leonardi A, Ellinger–Ziegelbauer H, Franzoso G, Brown K, Siebenlist U: Physical and functional interaction of filamin (actin–binding protein–280) and tumor necrosis receptor–associated factor 2. J Biol Chem 2000; 275: 271–278. [ Links ]
43. Marti A, Cunningham LC, Ohta Y, Hartwig J, Stossel TP, Kyriakis JM, Avruch J: ABP–280 binds the SAPK activator SEK–1 and is requiredforTNFa activation of SAPK in melanoma cells. J Biol Chem 1997; 272: 2620–2628. [ Links ]
44. Ozanne D, Brady M, Gaughan L, Cook S, Neal D, Robson C: Androgen receptor nuclear translocation is faciliated by the F–actin crosslinking protein filamin. Mol Endocrinol 2000; 14: 1618–1626. [ Links ]
45. Ohta Y, Suzuki N, Nakamura S, Hartwig J. Stossel T: The small GTPase RalA targets filamin to induce filopodia. Proc Natl Acad Sci 1999; 96: 2122–2128. [ Links ]
46. Bellanger JM, Bellanger JM, Astier C, Sardet C, Otha Y, Stossel TP, Debant A: TheRacl– and RhoG–activating domain of the bifunctional guanine nucleotide exchange factor Trio targets filamin to remodel cytoskeletal actin. Nature Cell Biol 2000; 2: 888–892. [ Links ]
47. Krief S, Faivre JF, Robert P, Le Douarin B, Brument LM, Lefrere I, Bouzyk MM, Anderson KM, Greller LD, Tobin FL, Souchet M, Bril A: Identification and characterization of cvHsp. A novel human small stress protein selectively expressed in cardiovascular and insulin–sensitive tissues. J Biol Chem 1999; 274: 36592–36600. [ Links ]
48. Petrecca K, Miller D, Shrier A: Localization and enhanced current density of the Kv4. 2 potassium channel by interaction with the actin–binding protein filamin. J Neurosci 2000; 20: 8736–8744. [ Links ]
49. Zhuang QQ, Rosenberg S, Lawrence J, Stracher A: Role of actin binding protein phosphorylation in platelet cytoskeleton assembly. Biochem Biophys Res Commun 1984; 118: 508–513. [ Links ]
50. Yuan Y, Shen ZJ: Interaction with BRCA2 suggests a role for filamin–1 (hsFLNa) in DNA damage response. J Biol Chem 2001; 276:48318–48324. [ Links ]
51. Kiema T, Lad Y, Jiang P, Oxley CL, Baldassarre M, Wegener KL, Campbell ID, Ylanne J, Calderwood DA: The molecular basis of filamin binding to integrins and competition with talin. Mol Cell 2006; 21: 337–347. [ Links ]
52. Solum NO, Olsen TM: Glycoprotein Ib in the Triton–insoluble (cytoskeletal) fraction of blood platelets. Biochim Biophys Acta 1984; 799: 209–220. [ Links ]
53. Okita JR, Pidard D, Newman PJ, Montgomery RR, Kunicki TJ: On the association of glycoprotein Ib and actin–binding protein in human platelets. J Cell Biol 1985; 100: 317–21. [ Links ]
54. Jamieson GA, Tandon NN, Greco NJ: Human platelet Thrombin receptor model for platelet activation. Editor, Rao GHR. En: Handbook of platelet physiology and pharmacology. Norwell, Massachusetts. Kluwer Academic Publishers, 1999, p. 21–37. [ Links ]
55. http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?CMD=search&DB=omim
56. Calderwood DA: Talin controls integrin activation. Biochem Soc Trans 2004; 32: 434–437. [ Links ]
57. Shattil SJ: Function and regulation of the beta 3 integrins in hemostasis and vascular biology. Thromb Haemostas 1995; 74: 149–155. [ Links ]
58. Jay D, García E, Lara JE, Medina MA, de la Luz Ibarra M: Determination of a cAMP–dependent protein kinase phosphorylation site in the C–terminal region of human endothelial actin–binding protein. Arch Biochem Biophys 2000; 377: 80–84. [ Links ]
59. Jay D, García E, de la Luz Ibarra M: In situ determination of a PKA phosphorylation site in the C–terminal region of filamin. Mol Cell Biochem 2004; 260: 49–53. [ Links ]
60. García E, Stracher A, Jay D: Calcineurin dephosphorylates the C–terminal region of filamin in an important regulatory site: a possible mechanism for filamin mobilization and cell signaling. Arch Biochem Biophys 2006; 446: 140–50. [ Links ]
61. Vadlamudi RK, Li F, Adam L, Nguyen D, Ohta Y, Stossel TP, Kumar R: Filamin is essential in actin cytoskeletal assembly mediated by p21 –activated kinase 1. Nat Cell Biol 2002; 4: 681–690. [ Links ]
62. Manser E, Leung T, Salihuddin H, Zhao ZS, Lim L: A brain serine/threonine protein kinase activated by Cdc42 and Rac1. Nature 1994; 367: 40–46. [ Links ]
63. Diaz–Valencia SD, Almaraz B Mdc J, Arias RLE, Hernández RR, Rojo DA, Guillen N, Vargas M: TheABP–120 C– end region from Entamoeba histolytica interacts with sulfatide, a new lipid target. Bio chem Biophys Res Common 2005; 338: 1527–1536. [ Links ]














