Introducción
Las especies del género Candida son microrganismos clasificados como comensales, ya que forman parte de la microbiota humana y se localizan en los tractos gastrointestinales, genitales y en la piel (Pfaller et al., 2007; Mixão., 2020). Sin embargo, en personas inmunosuprimidas o médicamente comprometidas, Candida puede provocar una candidiasis. La candidiasis es la enfermedad micótica más común a nivel mundial, la cual puede agravarse cuando el hongo entra en el torrente sanguíneo provocando una candidiasis invasiva o candidemia (Garnacho-Montero et al., 2012; McCarty et al., 2021). En el sector médico hay siete especies de Candida que infectan al humano causando la candidiasis, entre ellas se encuentran: C. tropicalis, C. glabrata, C. parapsilosis, C. stellatoidea, C. krusei y C. kyfer (McCullough et al., 1996; Khaled et al., 2019). Sin embargo, C. albicans es la especie con mayor incidencia en los aislados clínicos a nivel mundial (Biasoli et al., 2010; Talapko et al., 2021). No obstante, en los últimos años otras especies de Candida como C. glabrata, C parapsilosis y C. tropicalis han mostrado un aumento en su incidencia en aislados clínicos (Silva et al., 2012; Karkowska-Kuleta et al., 2020).
Los pacientes infectados con candidiasis presentan diferentes síntomas, los más comunes son una dermatitis con enrojecimiento y comezón, en algunos casos se puede producir fiebre, debilidad o fatiga, dolor muscular, dolor de cabeza y dolor abdominal. En pacientes cuya infección llega al grado de candidemia o candidiasis invasiva, la infección puede llegar a propagarse a zonas como ojos, riñones, cerebro e hígado (Figura 1), lo cual generalmente se presenta en pacientes postquirúrgicos o inmunodeprimidos (Pappas et al., 2018; Lazo et al., 2018).
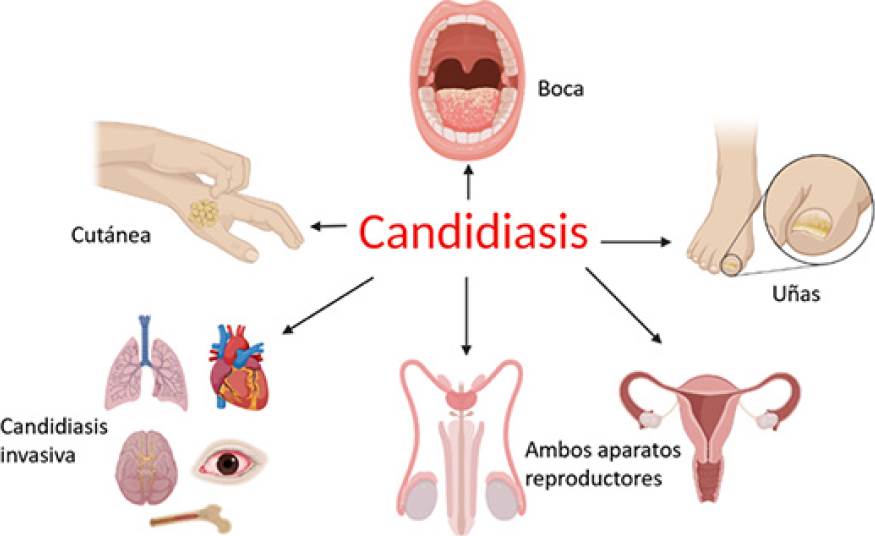
Fuente: Elaboración de los autores (en biorender.com).
Figura 1 Diferentes zonas en donde se presenta la candidiasis en humanos.
Actualmente se utilizan principalmente cuatro tipos de antimicóticos para atacar la infección por Candida: los polienos, los azoles, las equinocandinas y la flucitosina (Pappas et al., 2016; Pastrana-Gómez et al., 2020). Sin embargo, se han aislado cada vez con mayor frecuencia algunas especies de Candida como C. glabrata y C. auris con multirresistencia a los fármacos comúnmente utilizados, representando una seria amenaza (Arendrup y Patterson, 2017; Lone y Ahmad, 2019). C. auris se aisló por primera vez en el 2009, no obstante, en un corto plazo se detectó en varios países (Figura 2), causando infecciones invasivas difíciles de tratar (Chowdhary et al, 2017; Lone y Ahmad, 2019). Es por ello que la búsqueda de alternativas para controlar este tipo de microrganismos es una necesidad prioritaria.

Fuente: Tomada de Chowdhary et al. (2017).
Figura 2 Mapa global donde se muestra la rápida aparición de cepas clínicas de C. auris multirresistentes, desde el primer reporte en el 2009 hasta el 2017. El valor entre paréntesis indica el año del reporte de C. auris en el país o estado respectivo.
La nanotecnología es una ciencia multidisciplinaria que actualmente se está aplicando en diversos campos de investigación, uno de ellos es la biomedicina. En este sentido, las NPs metálicas podrían utilizarse para controlar especies de bacterias y hongos que presenten multirresistencia a los fármacos convencionales. Sin embargo, aún faltan estudios que demuestren que su uso resultaría beneficioso y no perjudicial para el humano o el medio ambiente. Una alternativa que se está evaluando es el uso de NPs sintetizadas de manera biológica o ecoamigable, pues no involucran el uso de químicos tóxicos, sino de material biológico (Castro-Longoria et al., 2017; Ijaz et al., 2020). En este trabajo se describe la problemática de la resistencia del género Candida y se incluyen los estudios más relevantes que han evaluado el potencial de las NPs como agentes antifúngicos contra diversas especies de Candida.
Las nanopartículas como agentes antimicrobianos
La nanotecnología crece a pasos agigantados y su utilización ha tenido un gran impacto en diversas áreas, entre ellas la medicina. Mediante la nanotecnología se han creado nuevas herramientas que se pueden utilizar para tratamientos, diagnósticos, monitoreo y control de sistemas biológicos, a este campo se le denomina nanomedicina (Mauricio et al., 2018). En la nanomedicina se utilizan NPs cuya dimensión en al menos una de sus caras es de nanómetros. Las propiedades de las NPs generalmente dependen de parámetros como el tamaño y la forma, los cuales son importantes para definir su factibilidad de internalizarse en las células (Ghosh Chaudhuri, 2012).
Las NPs metálicas son de particular interés en medicina debido a su capacidad antimicrobiana, al haberse demostrado que son eficaces para la inhibición de bacterias, hongos y virus (Ingle et al., 2014; Lakshminarayanan et al., 2018) (Figura 3). Sin embargo, su uso clínico es todavía controversial, por ello hacen falta un mayor número de estudios que comprueben que, aparte de ser efectivas contra los microrganismos patógenos, sus efectos adversos al humano o daños al medio ambiente sean mínimos (Castro-Longoria et al., 2017).
Nanopartículas metálicas para combatir la resistencia de Candida
La resistencia que generan los microrganismos como Candida es alarmante, se estima que el 70% de las infecciones intrahospitalarias son resistentes al menos a uno o más de los tratamientos actuales (Tang et al., 2017). El uso de las NPs metálicas en la clínica es todavía controversial; asimismo, existen productos en el mercado que contienen plata, como Acticoat®, Aquacel®, Contreet®, Actisorb Silver 220® y Urgotul SSD®. Estos productos son comercializados y se aplican principalmente para evitar infecciones en la piel en pacientes con quemaduras o úlceras crónicas (Castro-Longoria et al., 2017). Algunos de estos productos contienen plata nanocristalina, otros solo describen que contienen plata para liberación prolongada de iones. Por lo tanto, las NPs metálicas pudieran ser una solución para controlar microrganismos multirresistentes a los antimicrobianos convencionales. Hasta el momento, las NPs más estudiadas para combatir microrganismos son las nanopartículas de plata (AgNPs), y se ha demostrado que tienen la capacidad de inhibir bacterias Gram negativas y Gram positivas (Guzman et al., 2012). Además de la acción antibacteriana, a determinadas concentraciones, las AgNPs son capaces de inhibir también a C. albicans (Vázquez-Muñoz et al., 2014; Martínez-Andrade et al., 2018). Un resultado importante es la sinergia que presentan las NPs en combinación con antifúngicos convencionales, pues se ha reportado que aumentan su efectividad contra Candida. Por ejemplo, Vázquez-Muñoz et al. (2014) informaron que el uso combinado de Fluconazol, un fármaco fungistático, con AgNPs comerciales sintetizadas químicamente, redujo la proliferación celular de C. albicans.
Se ha documentado que cuando C. albicans se expone a las AgNPs se induce una rápida y elevada producción de especies reactivas de oxígeno (ROS), lo cual conduce a la muerte celular de la levadura (Hwang et al., 2012; Lee et al., 2019). En análisis bajo microscopía electrónica se ha observado cómo las AgNPs tienden a aglomerarse alrededor de la pared celular de Candida (Figura 4) y una exposición prolongada provoca la formación de poros finalizando en la muerte celular (Vázquez-Muños et al., 2014; Martínez-Andrade et al., 2018).

Fuente: Tomado de Vázquez-Muñoz et al. (2014).
Figura 4 Micrografías de C. albicans expuestas a AgNPs mostrando acumulación de NPs alrededor de la célula. A) Micrografía tomada bajo microscopía electrónica de barrido. B) Micrografía tomada bajo microscopía electrónica de transmisión.
Las NPs de cobre (CuNPs) también se han reportado como agentes antimicrobianos, al actuar como un fármaco de amplio espectro contra bacterias. La actividad de las CuNPs ya se ha demostrado también en contra de la levadura C. albicans. La exposición de las células a las NPs provoca daños en la pared y membrana celulares, generando poros en su superficie provocando la lisis de la célula (Cheong et al., 2020). Este tipo de NPs se han puesto a prueba con cepas de C. albicans resistentes a los azoles, demostrando que tienen la capacidad de impedir que Candida pase de su forma levaduriforme a su fase de pseudo-hifa (fase infecciosa), además de reducir el tamaño de biopelículas formadas por el hongo (Mudiar y Kelkar-Mane, 2020).
Nanopartículas biosintetizadas para combatir la resistencia de Candida spp
Aunque las NPs sintetizadas químicamente son efectivas contra microrganismos patógenos, la principal desventaja que presentan es el uso de diferentes compuestos utilizados durante la síntesis, o los subproductos generados por la misma, algunos de estos compuestos como el dióxido de sulfuro, formaldehído, óxidos de nitrógeno, metales ligeros y pesados, además de compuestos de cloración son altamente tóxicos para el humano y el medio ambiente. Por ello, una de las alternativas para eliminar el uso de químicos potencialmente tóxicos es la síntesis biológica, la cual involucra solamente el material biológico que sirve como agente reductor y estabilizante. Se ha comprobado que las NPs metálicas sintetizadas por el método biológico también son altamente efectivas para la inhibición de bacterias (Murillo-Rábago et al., 2022) y también se han evaluado para la inhibición de C. albicans obteniendo resultados prometedores (García-Marín et al., 2022). Incluso, son capaces de inhibir especies de Candida que presentan resistencia a los antifúngicos convencionales (El-Sherbiny et al., 2020).
Los extractos de plantas son altamente utilizados para la biosíntesis de NPs, y se han reportado para la biosíntesis de AgNPs y otros metales para la inhibición de Candida. Por ejemplo, las AgNPs sintetizadas con extractos de la planta Lotus lalambensis mostraron diámetros de inhibición de hasta 19 mm, con concentraciones de 50 µg/mL de AgNPs, en contra de C. albicans. Además, se reportó daño en la pared celular, la internalización de las NPs y la degradación de la membrana, con una alta producción de ROS. Los autores también reportaron una baja toxicidad de las AgNPs en células de mamíferos (Abdallah y Ali, 2021).
En el trabajo de Mohammadi et al. (2019) se reportó la síntesis de dos tipos de AgNPs, una utilizando extractos de la planta Zingiber officinale y otra con extractos de Thymus vulgaris, las cuales se probaron para la inhibición de C. albicans. Se reportó una concentración muy baja de AgNPs para la inhibición del hongo. La concentración mínima inhibitoria (CMI) fue de 0.7 µg/mL y 0.5 µg/mL para NPs sintetizadas con Z. officinale y T. vulgaris, respectivamente. La cantidad de Fluconazol necesaria para la inhibición del hongo fue de 16 µg/mL, lo cual contrasta con las CMI de las AgNPs. Además, se realizó un estudio de toxicidad en fibroblastos humanos (HDF-1), demostrando una baja toxicidad para ambas NPs. Un estudio reportó que la cantidad de Fluconazol necesaria para inhibir cepas de Candida fue mayor a los 64 µg/mL y mediante el uso de AgNPs sintetizadas a partir de extractos de la levadura Saccharomyces cerevisiae, se demostró una CMI de 2 a 4 µg/mL de AgNPs (Niknejad et al., 2015).
Las AgNPs biosintetizadas con extractos de la bacteria Rothia endophytica demostraron también una mejor actividad antifúngica que el Posaconazol en contra de C. albicans. Se reportó que la CMI fue de 62.5 µg/mL para las AgNPs y 125 µg/mL para el Posaconazol. Adicionalmente, se demostró que las AgNPs provocaron poros en la superficie de la célula, incluida una alta peroxidación lipídica con repercusiones en todos los ácidos grasos, lo cual condujo a la muerte celular (Elbahnasawy et al., 2021).
En un estudio reciente se evaluó la sinergia de AgNPs biosintetizadas en combinación con varios antifúngicos convencionales y se encontró que particularmente con el Itraconazol se obtuvo una mayor actividad contra C. glabrata, C. albicans, y C. tropicalis, registrando porcentajes de sinergismo relativo de 74.32, 57.78 y 36.37%, respectivamente (Figura 5) (Yassin et al., 2022).

Fuente: Imagen tomada y modificada de Yassin et al. (2022).
Figura 5 Sinergismo de las AgNPs en combinación con Itraconazol contra especies de Candida.
La síntesis biológica de NPs de cobre (CuNPs) se ha incrementado últimamente al ser más económica y con un amplio potencial de aplicación en diferentes campos. De igual forma que para las AgNPs, el material biológico más utilizado como agente reductor para la biosíntesis son las plantas, particularmente extractos de hojas, seguido por los hongos y por último las bacterias (Din y Rehan, 2017). Se ha reportado que las CuNPs son eficientes para inhibir diferentes especies de Candida. Por ejemplo, Tahvilian et al. (2019) sintetizaron CuNPs con extractos de hojas de Allium saralicum y se encontró que la CMI para C. albicans fue de 4 mg/mL, además, esta misma concentración fue suficiente para inhibir otras especies de Candida como C. krusei, C. glabrata y C. guilliermondii, todas reportadas con anterioridad en casos de resistencia. Mediante el extracto de la planta Prunus mahaleb se sintetizaron CuNPs, y se reportó una CMI de 0.125 µg/mL para inhibir a C. albicans (Dashtizadeh et al., 2021), lo cual demuestra que el agente reductor aumenta la eficiencia de las NPs. Las CuNPs tienen efectos similares a las AgNPs al entrar en contacto con la levadura, tienen la capacidad de adherirse alrededor de la célula, lo cual implica el deterioro de la pared celular, esto hace que las NPs internalicen más rápidamente la célula y ocasionen lisis celular (Padmavathi et al., 2020). Una ventaja de las NPs es su tamaño pequeño, esto ocasiona que internalicen la célula por difusión pasiva e inicie una bioacomulación dentro de la célula, además de la liberación de iones dentro de la célula, ocasiona la muerte temprana de las células de C. albicans (Martínez et al., 2021).
Recientemente se ha reportado la capacidad antifúngica de las NPs de óxido de cobre (CuONPs) biosintetizadas mediante el uso del hongo Trichoderma sp. Se reportó que son altamente efectivas contra C. albicans, pues poseen un tamaño pequeño (5.8 ± 3.5 nm) y se acumulan alrededor de toda la célula, internalizándose (Figura 6) y provocando la generación de especias reactivas de oxígeno (ROS) y, finalmente, la muerte celular. Aunado a esto, se reportó que a determinadas concentraciones el efecto tóxico en tres líneas celulares es mínimo (Garcia-Marin et al., 2022).

Fuente: Imagen tomada de García-Marín et al. (2022).
Figura 6 Células de C. albicans expuestas a nanopartículas de óxido de cobre. A) y C) Muestran la célula completa, y, B) y D) muestran zonas amplificadas donde se observan acumulaciones de las nanopartículas, las cuales son señaladas con flechas.
Otras NPs metálicas sintetizadas por medio del método biológico (Tabla 1) y probadas en contra de Candida, son las NPs de óxido de zinc (ZnONPs). Un estudio reciente realizó la biosíntesis de ZnONPs con extractos de plantas, Beta vulgaris, Cinnamomum tamala, Cinnamomum verum y Brassica olerace. Todas las ZnONPs mostraron actividad antifúngica en contra de C. albicans (Pillai et al., 2020), no obstante, el resultado no fue tan efectivo como el de las NPs de plata y cobre. Asimismo, recientemente se sintetizaron NPs de dióxido de titanio (TiO2NPs) utilizando una mezcla de extractos de las plantas Azadirachta indica, Ficus benghalensis y Syzygium aromaticum, y se encontró que a una concentración de 100 µg/mL se inhibe la formación de biopelículas de C. albicans (Achudhan et al., 2020). Esto demuestra la búsqueda constante de alternativas, y que en un corto plazo será posible utilizar en la clínica uno o varios productos nanotecnológicos para la inhibición de especies de Candida multirresistentes a los antifúngicos convencionales.
Tabla 1 Efecto antifúngico en especies de Candida de las nanopartículas metálicas producidas con distintos reductores biológicos.
| Tipo de NP | Agente reductor | Efecto antifúngico | Especie de Candida | Referencia |
|---|---|---|---|---|
| Óxido de cobre | Metabolitos secundarios del hongo Trichoderma asperellum | Fungicida | C. albicans | García-Marín et al. (2022) |
| Plata | Extractos de la planta Lotus lalambensis | Fungicida | C. albicans | Abdallah y Ali (2021) |
| Plata | Extractos de la planta Zingiber officinale | Fungicida | C. albicans | Mohammadi et al. (2019) |
| Plata | Extractos de la planta Thymus vulgaris | Fungicida | C. albicans | Mohammadi et al. (2019) |
| Plata | Extractos de la levadura Saccharomyces cerevisiae | Fungicida | C. albicans | Niknejad et al. (2015) |
| Plata | Extractos de la bacteria Rothia endophytica | Fungicida | C. albicans | Elbahnasawy et al. (2021) |
| Plata | Extracto acuoso de la cáscara de Punica granatum en sinergia con itraconazol | Fungicida | C. glabrata, C. albicans, y C. tropicalis | Yassin et al. (2022) |
| Cobre | Extractos de hojas de Allium saralicum | Fungicida | C. albicans, C. krusei, C. glabrata, y, C. guilliermondii | Tahvilian et al. (2019) |
| Cobre | Extracto de la planta Prunus mahaleb | Fungicida | C. albicans | Dashtizadeh et al. (2021) |
| Oxido de zinc | Extractos de las plantas, Beta vulgaris, Cinnamomum tamala, Cinnamomum verum y Brassica olerace | Fungicida / Fungistático | C. albicans | Pillai et al. (2020) |
| Dióxido de titanio | Mezcla de extractos de las plantas Azadirachta indica, Ficus benghalensis y Syzygium aromaticum | Fungicida | C. albicans | Achudhan et al. (2020) |
Fuente: Elaboración de los autores.
Conclusiones y perspectivas
Se ha demostrado que las nanopartículas metálicas sintetizadas químicamente y por medio de métodos biológicos son efectivas para la inhibición de especies de Candida. Además, que la efectividad de las nanopartículas aumenta al combinarse con antibióticos convencionales. Sin embargo, las nanopartículas sintetizadas biológicamente representan una mejor opción, al no involucrar el uso de químicos tóxicos potencialmente dañinos al humano y al medio ambiente. Por lo tanto, representan una excelente alternativa para solucionar la problemática de la resistencia del género Candida. Por consiguiente, en un futuro cercano, la nanotecnología hará posible contar con nuevas y mejores opciones que contribuyan a solucionar el problema de la multirresistencia. Por lo anterior, es importante que se realicen un mayor número de estudios para evaluar el potencial clínico de las nanopartículas, sobre todo aquello que involucre aislados clínicos que presenten multirresistencia, y la correspondiente evaluación utilizando modelos in vivo.











 nueva página del texto (beta)
nueva página del texto (beta)



