Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Hidrobiológica
versión impresa ISSN 0188-8897
Hidrobiológica vol.11 no.1 Ciudad de México jun. 2001
Composición y abundancia de las macroalgas halino-resistentes en los sedimentos minero-medicinales en salinas de Cuba
Genoveva Popowski Casañ,1 Magalys Sánchez Lorenzo2 y José N. Álvarez-Cadena3
1 Centro Nacional de Termalismo, Ministerio de Salud Pública de Cuba. Ave. 243 #19815 Carretera del Wajai. Fontanar. Boyeros. Cuba. FAX:(537) 453599. E-mail: p_sarria@mixmail.com
2 Instituto de Oceanología. Ministerio de Ciencia y Tecnología y Medio Ambiente. Cuba. Ave. 1ra #18406 e/ 184 y 186. Playa. C. Habana. Cuba. E-mail: ecomar@oceano.inf.cu
3 Universidad Nacional Autónoma de México, Instituto de Ciencias del Mar y Limnología. Unidad Académica Puerto Morelos. Apdo. Postal 1152, Cancún, Quintana Roo, 77501. México. E-mail: inac@mar.icmyl.unam.mx
Recibido: 16 de julio de 2000
Aceptado: 24 de enero de 2001
Resumen
Se estudian la composición y la abundancia de las microalgas en la columna de agua y en los sedimentos de varias salinas de Cuba. La clorofíta Dunaliella salina (26° Bé) y las cianobacterias (13 a 26° Bé) predominan en la comunidad aportando al medio halino substancias biológicamente activas, producto de su metabolismo, tales como proteínas, carotenos, glicerol, vitaminas, etc. De un total de 5,253,206 células, las especies más abundantes de cianobacterias fueron: Aphanothece halophytica (49.8%), Myxobaktron salinum (24%), Synechococcus sp (12.5%), Spirulina nodosa (9.2%) y Gloeocapsa sanguinea (4.3%). Cuando la salinidad fue menor a 13° Bé, la comunidad estuvo representada principalmente por diatomeas y dinoflagelados quienes aportan sílice y pectina al medio. La naturaleza y propiedades químicas de los fangos halinos dependen en gran medida de la abundancia y composición de las microalgas presentes que intervienen en su naturaleza y transformación, de tal forma que estos sedimentos minero medicinales poseen propiedades específicas las cuales son inherentes a su lugar de extracción dentro de la salina, por lo cual pueden ser aplicados a diferentes tratamientos, ya sea médicos o cosmetológicos.
Palabras clave: Microalgas, salinas, fangos medicinales, Cuba.
Abstract
Studies on the composition and abundance of salt-tolerant microalgae from the water column and sediments from Cuban salines are analyzed. The Chlorophyte Dunaliela salina (26° Bé) and Cyanobacteriae (13 to 26° Bé) dominated in the environment enriching the sediments with biologically active by-products, such as proteins, carotenes, glycol, vitamins, etc. From a total of 5,253,206 cells, the most abundant Cyanobacteriae species were: Aphanothece halophytyca (49.8%), Myxobaktron salinum (24%), Synechococcus sp (12.5%), Spirulina nodosa (9.2%) and Gloeocapsa sanguinea (4.3%). At salinities lower than 13° Bé, diatoms and dinoflagellates were the main groups in the community and contributed with silice and pectin to the muds. The nature and Chemical properties of these haline mineral muds depend on the abundance and composition of the microalgae, wich in turn depend on the site they were collected. These muds having different properties can be used on specific treatments, both, medical or in cosmetology.
Key words: microalgae, salt-works, medicinal muds, Cuba.
Introducción
El uso de los fangos medicinales, para aliviar algunos malestares osteo-articulares, se remonta a la época de los romanos a quienes se les atribuye la primacía de tomar baños de fango con fines curativos (Delmas-Marsalet, 1967; Lary, 1980; Dupuis, 1994). Desde esa época hasta el presente, este tratamiento ha ido tomando cada vez más valor terapéutico gracias al avance de la ciencia (De Roeck-Holtzhauer y Bodilis, 1991; Monpoint y Guilhou, 1991). En la actualidad existe una tendencia progresiva hacia el aprovechamiento de estos recursos naturales, incluyendo el uso de las aguas madres y los fangos minero-medicinales o peloides. Estos tratamientos han tenido una creciente aceptación y han sido aplicados en numerosas afecciones en el hombre, o incluso con fines estéticos en balnearios y en cosmetología (Frances y Boisnic, 1989; De Roeck-Holtzhauer et al., 1989; De Roeck-Holtzhauer y Leray, 1990; Dereure et al., 1990; Privat, 1991; Couté, 1993; Sukenik et al., 1994).
Las salinas representan una valiosa fuente de recursos renovables explotables, no solamente por su principal producto, la sal, sino por toda la gama de derivados de las salmueras residuales o colaterales y de sus fangos, entre otros. En Cuba, los fangos de varias de sus salinas y sus aguas madres se han incorporado para su explotación (Luaces y García, 1996; Regal y Andión, 1996; Rodríguez et al., 1996).
Las microalgas existentes en estos sistemas halinos son de gran importancia en la formación y cualidad de los fangos debido a que liberan substancias, producto de su metabolismo, biológicamente activas, tales como proteínas, vitaminas, carotenos, ficocianina entre algunos de ellos. Estos metabolitos permiten la proliferación de bacterias en la columna de agua y en el sedimento, lo cual es posible gracias a que las bacterias del sedimento aprovechan los productos de las lisis celulares de las microalgas o de sus secreciones. Todo esto aunado a la presencia de otras microalgas que habitan allí, producen un bio-gel de consistencia untuosa que se mezcla en gran medida con el sedimento interviniendo en su transformación y enriquecimiento (Lary, 1980).
Los objetivos de este trabajo son los de conocer las características de las microalgas de las aguas madres y fangos medicinales de las salinas de Cuba, enfatizando su importancia y su utilización en tratamientos de salud y de cosmetología.
Materiales y métodos
Se realizaron muestreos en la columna de agua de las salinas Bidos, 9 de Abril, Puerto Padre, Cerro Guayabo, Frank País, Joa, Baitiquirí, El Real y Macambo; y de sedimento en las salinas Bidos, 10 de Abril y El Real (Fig. 1). Las recolectas se realizaron al inicio y final de las cosechas de la sal en cada salina desde 1989 hasta 1996. Estos muestreos se efectuaron en diferentes fechas para cada salina ante la imposibilidad de muestrear simultáneamente.
En cada salina se ubicaron 5 estaciones, una de ellas fija para la toma de muestras de agua con salinidad promedio de 3,5° Bé y otras cuatro en áreas cuya salinidad corresponde a las precipitaciones de las siguientes sales: Fe2O3 (9.5 ° Bé); CaCO3 (13.5° Bé); CaSO4 (22.5° Bé) y NaCl (26° Bé).
En cada laguna se recolectaron 10 litros de agua que fueron filtrados con una malla de 133 mm, que permitiera la eliminación de todos aquellos elementos de estas dimensiones o mayores, para el análisis del fitoplancton según metodología de Popowski y Borrero (1989). Los sedimentos se analizaron tomando 1cc de fango diluidos en 50cc de agua de mar filtrada y siguiendo la misma técnica para fitoplancton de los autores antes mencionados. Los resultados se expresan en células por mililitros (cel.ml-1) para las muestras de agua y en células por gramo (cel.g-1) en las muestras de sedimento. La determinación de materia orgánica particulada fue hecha de acuerdo a Lovegrove (1966). Un grado Bé = 10,7 UPS.
Resultados y discusión
De un total de 9,269,696 cél.ml-1, los grupos de microalgas en orden de importancia fueron: cianobacterias (58.3%), dinoflagelados (40.2%), falgelados (0.6%), clorofitas (0.4%) y diatomeas (0.3%).
Las cianobacterias (5,253,206 cel/ml-1) además de ser el grupo más importante en abundancia, se presentó en todos los sistemas halinos estudiados con densidades máximas en salinidades entre 13 y 26° Bé (Fig. 2A).
Las clorofitas estuvieron representadas únicamente por Dunaliella salina Teodoresco con mayores concentraciones en Joa (22,100 cel/ml-1 principalmente en salinidades a partir de los 13° Bé (Fig. 2B).
Las diatomeas y los dinoflagelados estuvieron bien representados en salinidades menores a 13° Bé (Figs. 3A, B), pero estos grupos no proliferan a salinidades más altas y son substituidos por cianobacterias, flagelados y clorofitas.
Las cianobacterias Aphanothece halophytica Fremy (49.8%), Myxobaktron salinum Hansgirg (24%) y Synechococcus sp. (12.5%), contribuyeron con más del 86% de esta flora (Figs. 4 A, B y C) mientras que Spirulina nodosa Schiller y Gloeocapsa sanguinea (Ag.) Kütz lo hicieron con 9.2% y 4.3% respectivamente (Figs. 5 A y B).
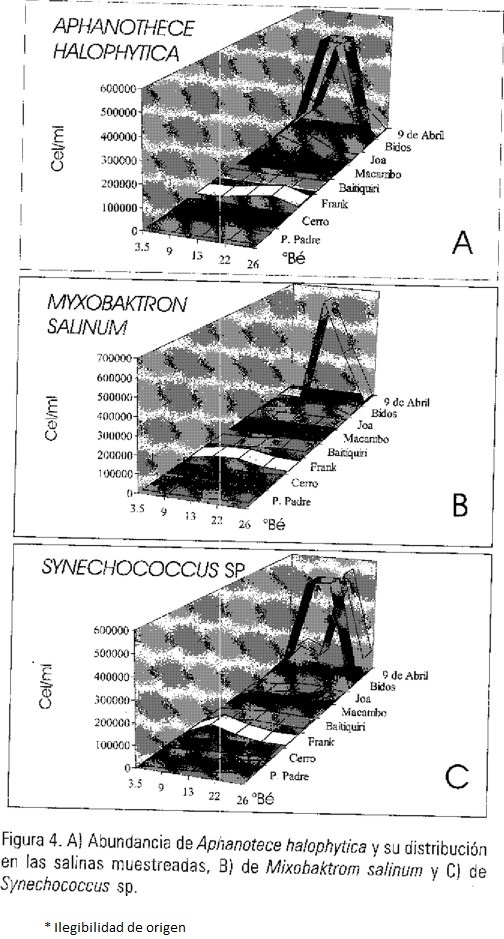

Aphanothece halophytica fue encontrada en mayor abundancia en las salinas de Bidos y 9 de Abril en salinidades de 13 y 22 Bé. De esta cianobacteria se sabe que produce un bio-gel de origen lipopolisacárido, y Tindall et al. (1977), reportan que su contenido en proteínas (76%) es superior al de otras cianobacterias e incluso al de varias especies de Spirulina. La alta calidad de sus proteínas y la fácil digestibilidad de sus ácidos grasos permiten situarla como un excelente complemento alimenticio potencial comparable a las de Spirulina.
Myxobaktrum salinum (24%) fue encontrada en bajas abundancias en casi la totalidad de las salinas, no se encontró en Joa, y tuvo sus más altos registros en la salina 9 de Abril en donde se recolectaron 986,000 cel.l-1 que representó el 78% del total capturado.
Synechococcus sp. (12.5%) fue importante en las salinas 9 de Abril y Bidos en salinidades entre 13 y 22° Bé, pero se mantuvo en bajas cantidades en el resto de los sistemas halinos.
Spirulina nodosa (9.2%) se registró con mayor abundancia en Cerro Guayabo (314,092 cel.l-1 y en Joa (117.725 cel.l-1) en salinidades de 26° Bé y no se encontró en el resto de las salinas, excepto en Puerto Padre aunque en cantidades mínimas (54,570 cel.l-1).
El género Spirulina, es uno de los más estudiados mundialmente por su valor nutritivo y sus múltiples aplicaciones. El contenido proteico de esta alga está catalogado inmediatamente después de las proteínas de la yema de huevo, adoptada como proteína de valor promedio por la FAO (Durand-Chastel, 1993).
Así también varios autores reportan la acción terapéutica que poseen los ácidos grasos poli-insaturados que contiene Spirulina, tales como el ácido linolénico (G. L. A.) (Clement et al., 1967; Bulik, 1993; Durand-Chastel, 1993). Éstos ácidos grasos disminuyen algunas lesiones inflamatorias, particularmente en casos de quemaduras, permitiéndole a la piel una mayor resistencia y una cicatrización y sensibilidad de mejor calidad. Estos compuestos han sido similarmente aplicados en ulceraciones y constituyen una importante ayuda en la prevención del envejecimiento cutáneo (Monpoint y Guilhou).
Por otro lado la ficocianina (uno de sus pigmentos principales) estimula el sistema inmunológico dando protección en enfermedades de esta naturaleza (Ijima et al., 1982). Otro de sus componentes, la ficobilina, está considerada como agente antitumoral y ha sido utilizada en tratamientos de úlceras y hemorroides sangrantes (Dainippon INK, Chemical and Tokyo Kenkyukai, 1983).
Spirulina posee un alto contenido del complejo vitamínico R-12 con múltiples usos en afecciones osteo-articulares, además de contener vitaminas C, E y provitamina A. Bulik (1993) atribuye a esta cianobacteria una acción preservadora, debido a sus propiedades enzimáticas y a los agentes antioxidantes que interfieren con los radicales libres que propician el proceso de envejecimiento, evitando la degeneración celular y permitiendo una vida más longeva y joven.
Gloeocapsa sanguinea (4.3%) se reportó en relativamente altas densidades en Joa, a salinidades entre 9 y 13° Bé principalmente. Sus concentraciones fueron mínimas en las salinas de Puerto Padre y Cerro Guayabo y no se recolectó en Baitiquirí.
Las cianobacterias son el grupo más importante y predominan en abundancia y distribución en los sistemas halinos con concentraciones máximas en salinidades desde 13 hasta 26° Bé. Estas microalgas son las principales productoras primarias en este tipo de ecosistema, y Berland et al. (1989) mencionan que tienen la capacidad de sobrevivir en ambientes extremos de salinidad, temperatura y pH. El éxito de este grupo de microalgas se debe a que pueden alcanzar su equilibrio osmótico mediante la acumulación intracelular de iones de potasio. Así también, su metabolismo les permite incrementar la concentración de carbohidratos y aminoácidos de 2 a 4 veces su valor durante el ajuste osmótico en ambientes con salinidades altas. Otro mecanismo de adaptación de las cianobacterias a este medio ambiente consiste en responder a los cambios de salinidad, alterando su forma o produciendo un gel de lipopolisacárido que les permite aislarse del medio. La membrana celular de este grupo de cianobacterias está constituida por lipoproteínas, pectina, hemicelulosa y celulosa la cual se mucilaginiza produciendo un gel que vierte al exterior (Jones y Yopp, 1979).
Dentro del grupo de las clorofitas, Dunaliella salina fue la única representante con máximas concentraciones en Joa a 26° Bé (Fig. 2B); esta especie es capaz de adaptarse a altas concentraciones de sal a través de un mecanismo osmorregulador, consistente en la producción de b caroteno y glicerol intracelularmente de manera proporcional a la concentración de sal en el exterior (Ginsburg et al., 1990; Giordano, 1992). Su pared celular es elástica y puede rápidamente ajustar la presión osmótica por flujo de agua a través de la membrana citoplasmática. Brown et al. (1989) reportan que esta microalga contiene 57% de proteínas, 32% de carbohidratos, 9% de lípidos y 8% de minerales. Dunaliella posee un contenido proteico de hasta 40% en peso seco y bajo determinadas condiciones de iluminación, alta salinidad y bajo contenido en nitrógeno puede producir hasta 50% de su peso seco en glicerol y 8% en β caroteno.
Este β caroteno ha sido utilizado en forma de extracto seco, en píldoras, mediante atomizadores en la industria de cosméticos y como aditivo en productos para la protección solar (Schlipalius, 1991; Borowitzka, 1991). Así también tiene aplicaciones en oftalmología por su contenido en provitamina A, al mismo tiempo que se ha comprobado su efecto antitumoral y en ciertas fotodermatosis.
Las diatomeas y los dinoflagelados debido a que están constituidos principalmente por sílice y pectina respectivamente, y en algunas diatomeas se ha observado que la membrana celular incrementa su contenido de sílice en función de grupos sulfhídricos disueltos en el medio. Estos compuestos azufrados caracterizan en gran medida a este tipo de sedimentos halinos (Margalef, 1983). Sin embargo, diatomeas y dinoflagelados no se desarrollan a salinidades mayores a 13° Bé posiblemente por las extremas condiciones halinas y térmicas.
El contenido de materia orgánica particulada varía de una salina a otra, pero en casi la totalidad de ellas el aporte fundamental está dado por las microalgas con más del 50%. Así también la composición de las microalgas en la columna de agua de las salinas tiene un papel determinante en la composición de los peloides y proveen información relativa a las potencialidades en su uso.
Los muestreos en sedimento reflejan diferencias en la concentración y composición de las microalgas. En la Salina 10 de Abril, los sedimentos estuvieron constituidos por una comunidad de diatomeas (entre los 9 y 22° Bé) acompañada por un predominio de cianobacterias que presentan su máxima densidad a 13° Bé (Tabla 1). En esta salina la abundancia de microalgas es superior a las observadas en El Real donde la comunidad está representada totalmente por cianobacterias y sus mayores concentraciones están desplazadas hacia los estanques de 22° Bé (Tabla 1).
Las especies dominantes son: en la salina 10 de Abril Aphanothece halophytica y en El Real Myxobaktron salinum, en esta última también se encuentran en menor cantidad a Gloeocapsa sanguinea y Aphanothece halophytica, mientras que las diatomeas Nitzchia sp y Navicula sp lo son en la salina 10 de Abril (Tabla 1).
Las áreas de donde actualmente se extraen los fangos con fines terapéuticos son las salinas Bidos (10,8° Bé) y El Real (22° Bé), sin embargo, las otras salinas son potencialmente explotables en cuanto a estos recursos medicinales o de belleza. La composición y la abundancia de las microalgas que se encuentran en la columna de agua son diferentes que las del sedimento, esencialmente debido a diferencias en salinidad. Bidos presenta, en el fango, densidades superiores (hasta 178,500 cel.g-1) respecto de El Real (17,200 cel.g-1) y mayores también en la columna de agua (717,400 cel.ml-1 y 9,100 cel.ml-1 respectivamente). El grupo dominante para ambas salinas es el de las cianobacterias pero sus especies varían en cada lugar. Dentro de las especies de cianobacterias en Bidos se identificaron a Aphanothece halophytica, Myxobaktron salinum, Spirulina nodosa y a Gloeocapsa sanguinea que fue la más abundante en el fango que en la columna de agua, en el resto de las especies se presentó la situación opuesta (Tabla 2).

Los contenidos en lípidos (974mg l-1 y proteínas (652mg l -1) de los sedimentos de El Real son aportados por las cianobacterias ya que a esta salinidad (22° Bé) se presentan las mayores abundancias (Miravet et al., 1993). Esta distribución indica que las especies estarán localizadas en determinadas salinas y en determinados rangos de salinidad y así su aporte al medio no será igual ni en magnitud ni en composición.
Como se ha podido observar, las macroalgas, en particular las cianobacterias y las clorofitas, tienen un papel importante en la formación de los fangos medicinales ya que parte de la naturaleza del sedimento depende en gran medida de la composición y concentración de la microflora que habita en los diferentes ambientes salinos. Las sustancias bioactivas, producto de su metabolismo, enriquecen y/o transforman el sedimento y pueden ser utilizadas en tratamientos medicinales específicos, así como en centros de talassoterapia, balnearios y estéticas. La aplicación de estos sedimentos varía de acuerdo a sus propiedades en su composición específica las cuales a su vez dependen del yacimiento de donde fueron extraídos.
Conclusiones
1. Las cianobacterias son el grupo de microalgas predominantes tanto en la columna de agua como en el sedimento en las salinas estudiadas.
2. Las especies dominantes en la columna de agua fueron: Aphanothece halophytica, Myxobaktron salinum, Synechococcus sp, Spirulina nodosa y Gloeocapsa sanguinea. La clorofita Dunaliella salina, por otro lado contribuyó substancialmente a la composición de los fangos. En el sedimento se encuentran además a las diatomeas Nitzschia sp y Navicula sp cuando las salinidades no exceden los 13° Bé.
3. Las microalgas aportan más del 50% del contenido en la naturaleza de los sedimentos y de las aguas madres de estas salinas. Su distribución, composición y abundancia en los diferentes yacimientos permitirán hacer un mejor y específico uso de los peloides en los diferentes tratamientos médicos y de cosmetología.
Agradecimientos
Agradecemos la colaboración de Francisco Escobar de la Llata, Francisco Ruiz Rentería y de Gabriel Rosado Perera de la sección de Cómputo de la Unidad Académica Foránea Puerto Morelos, ICMyL, UNAM, por su ayuda en la realización de las gráficas.
Literatura citada
Berland, B. T. Le Campion y M. H. Campos Baeta, 1989. Interaction de la salinité et de la température sur la morphologie, la croissance et la composition cellulaire d'une cyanobactérie halótolérante. (Aphanothece sp). Botanica Marina 32: 317-329. [ Links ]
Borowitzka, L. J., 1991. Development of western biotechnology's algal b carotene plant. Bioresource Technology 38: 251-252. [ Links ]
Brown, M. R., S. W. Jeffrey y C. D. Garland, 1989. Nutritional aspects of microalgae used in mariculture, a literature review. CSIRO Marine Laboratories Report 205. [ Links ]
Bulik, C. G., 1993. How the Spirulina, a blue-green alga, preserves the cell from degeneration and extends youth to human. Spirulin Algue de Vie. 121-132. [ Links ]
Clement, G. M., M. Rebeler y C. Zarrouk, 1967. Wound treating medicaments containing algae. Frivli Medical. 5279.
Couté, A., 1993. Les microalgues et le thermalisme. Presse Thermale et Climatique 130(1): 36-45. [ Links ]
Dainippon Ink and Chemical and Tokyo Kenkeyukai (Inventors and assignee). 1983. Antitumoral agents containing phycobilin also to treat ulcers and hemorrhoidal bleeding. JP 58065216 A 830418. [ Links ]
Delmas-Marsalet, P. A., 1967. Utilisation des boues médicinales à travers les ages. Concours Méd, 89. [ Links ]
De Roeck-Holtzauer, Y., C. Claire y F. Bresdin, 1989. Algues: Santé et Beauté. Revue des Phytotherapie 2: 16-24. [ Links ]
De Roeck-Holtzauer, Y. et I. Bodilis, 1991. Thalassothérapie, thermalisme, peut-on tester leur efficacité? Quelques données sur les algues et les boues marines. Premier Colloque Scientifique Français sur la biotechnologie des microalgues et des cyanobacteries appliqués au thermalisme. 27-42. [ Links ]
Dereure, O., N. Basset-Segun y J. J. Guiilhou, 1990. Preséntation générale des rétinoïdes dans le vieillissement cutané., Ed. Sauramps Medical: 115-121.
Dupuis, M., 1994. Neyrac-Les-Bains. De l'origine á nos jours. Presse Thermale et Climatique 131(1): 40-45. [ Links ]
Durand-Chastel, H., 1993. La Spiruline, algue de vie. Monaco. Musée Oceanographique. Editeurs Scientifiques: FranVois Donmengue, Hubert Durand-Chastel, Anne Toulemont. [ Links ]
Frances, C. y S. Boisnic, 1989. Radicaux libres et cosmetologie. Journal Medicale Esthetic et Cirugie Dermatologica. Vol XVI (64): 289-294. [ Links ]
Ginsburg, M., G. Wezinger, M. Cohen y B. Ginsburg, 1990. The adaptation of Dunaliella to wisely-differing salt concentrations. Journal of Experimental Botany 41: 685-692. [ Links ]
Giordano, M., 1992. Effeti di differenti condizioni di coltiro sulla biologia della microalga verde alotollerante Dunaliella salina PhD. Thésis, University of Genova, Italy. 1-46. [ Links ]
Ijima, N., I. Fugii, H. Shimamatsu y S. Katch, 1982. Anti tumor agent and method of treatment there with. U. S. Patent pending, REF. No. P1150-726-A 82679. [ Links ]
Jones, J. H. y J. H. Yopp, 1979. Cell wall constituents of Aphanothece halophytica. Journal of Phycology 15: 62-66. [ Links ]
Lary, A., 1980. La Pelothérapie. Presse thermale et climatique 117(1): 1-11. [ Links ]
Lovegrove, T., 1966. The determination of the dry weight of plankton and the effect of various factors on the values obtained. In: Barnes, H. (Ed.) Some contemporary studies in marine science. London. Allen and unwin Ltd. p. 429-67. [ Links ]
Luaces, D. y S. García, 1996. Uso del jabón de peloides en trabajadores con exposición a petróleo y derivados. II Congreso de Turismos de Salud y II Jornada de Termalismo. 27-31/Mayo. Cuba. [ Links ]
Margalef, R., 1983. Limnología. Ediciones Omega. Barcelona. España. 1010 pp. [ Links ]
Miravet, M. E., R. Guerra, M. Álvarez y D. Enríquez, 1993. Características químicas y microbiológicas de los sedimentos de la salina El Real. Informe interno. Inst. de Oceanología. Cuba. 1-5. [ Links ]
Monpoint, S. y J. J. Guilhou, 1991. Les microalgues: applications potentielles en dermatologie. Premier Colloque Scientifique FranVais sur la Biotechnologie des microalgues et des cyanobacteries apliquee au thermalisme. 93-96. [ Links ]
Popowski, G. y N. Borrero, 1989. Utilización de fijadores en flagelados y su aporte a la concentración del fitoplancton en el Golfo de Batabanó. Cuba. Reporte de Investigaciones 11: 1-8. [ Links ]
Privat, Y., 1991. Cosmétologie d'aparet et cosmétologie dite de soins, ou pour une nouvelle définition de la cosmétologie. Nouvelle Dermatologie 10(1): 10-11. [ Links ]
RegaL, P. y A. Andión, 1996. Efectos de la peloidoterapia sulfurada en artropatías crónicas. II Congreso de Turismos de Salud y II Jornada de Termalismo. 27-31/Mayo. Cuba. [ Links ]
Rodríguez, C., M. Costafreda, G. Rodríguez, O. Pages, L. Verges y J. Reborido, 1996. Modelo de quemaduras dérmicas A, AB, e hipodérmicas en ratas Wistar para la evaluación de sustancias con posible actividad regenerativa y cicatrizantes. II Congreso de Turismos de Salud y II Jornada de Termalismo. 27-31/Mayo. Cuba. [ Links ]
Schlipalius, L., 1991. The extensive commercial cultivation of Dunaliella salina. Bioresource Technology 38: 241-244. [ Links ]
Sukenik, S., H. Giryes, S. Halevy, L. Neumann, D. Flusser y D. Buskila, 1994. Treatment of psoriatic arthritis at the Dead Sea. Journal of Rhematology 21(7): 1305-1309. [ Links ]
Tindall, D., J. Yopp, W. Schmid y D. Miller, 1977. Protein and amino acid composition of the obligate halophile Aphanothece halophytica (cyanophyta). Journal of Phycology 13: 127-133. [ Links ]














