Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Chapingo. Serie horticultura
versión On-line ISSN 2007-4034versión impresa ISSN 1027-152X
Rev. Chapingo Ser.Hortic vol.17 spe 2 Chapingo ene. 2011
Efecto del ácido ascórbico sobre crecimiento, pigmentos fotosintéticos y actividad peroxidasa en plantas de crisantemo
Effect of ascorbic acid on growth, photosynthetic pigments and peroxidase activity of chrisantemum plants
Martha Elena Mora-Herrera1¶; Jezabel Peralta-Velázquez1; Humberto Antonio López-Delgado2; Rómulo García-Velasco1, Justino Gerardo González-Díaz1
1 Centro Universitario Tenancingo, Universidad Autónoma del Estado de México. km 1.5, Carretera Tenancingo-Villa Guerrero, Estado de México, C.P. 52400, MÉXICO. Tel. 01 714 140 77 24, Ext. 176, FAX. 01 714 140 77 25, Correo-e: marthaelenam@gmail.com (¶Autor para correspondencia).
2 Programa Nacional de Papa, Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP), Metepec, Estado de México, C. P. 52141. MÉXICO.
Recibido: 15 de noviembre, 2010.
Aceptado: 20 de septiembre, 2011.
Resumen
Los cultivos enfrentan problemas en el manejo agronómico y sufren enfermedades, lo que incrementa los costos y la contaminación ambiental. El ácido ascórbico (AA) es un compuesto antioxidante que induce respuestas relacionadas al crecimiento en las plantas para enfrentar el estrés. Se evaluó el efecto del AA en plantas de crisantemo (Dendranthema grandiflora Tzvelev) cultivar Polaris en condiciones de invernadero. Las plantas se asperjaron dos veces por semana con 0, 3.4 y 6.8 mM de AA a partir de los 30 días de cultivo y hasta la cosecha (100 días de cultivo). El AA incrementó significativamente la longitud del tallo, peso seco, número de botones y tallos por planta con respecto al testigo sin aplicación de AA, siendo el mejor tratamiento la concentración de 6.8 mM de AA el que incrementó la biomasa. Asimismo, el AA incrementó significativamente el contenido de proteína (36 %), pigmentos fotosintéticos totales (75 %) y actividad enzimática de la peroxidasa (33 %), con respecto al testigo, respuestas que se asociaron a los parámetros de crecimiento evaluados.
Palabras clave: Dendranthema grandiflora, crecimiento, contenido de proteína, actividad antioxidante.
Abstract
Crops face problems of agronomic management and diseases, increasing costs and environmental contamination. Ascorbic acid (AA) is an antioxidant compound which induces plant growth-responses to cope with stress. The effect of AA on chrisantemum (Dendranthema grandiflora Tzvelev) cv. Polaris under greenhouse condition was evaluated. Plants were sprayed twice a week with 0, 3.4 and 6.8 mM of AA from 30 days after transplant up to harvest time (100 days after transplant). AA significantly increased shoot length, dry weight, number of floral buds and stems per plant in contrast with control, being 6.8 mM the best treatment which enhanced biomass. AA significantly enhanced protein content (36 %), total photosynthetic pigments (75 %) and peroxidase activity (33 %) respecting the control, these responses were associated to the evaluated growth parameters.
Key words: Dendranthema grandiflora, growth, protein content, antioxidative activity.
INTRODUCCIÓN
En la actualidad, la agricultura es altamente dependiente de insumos y pesticidas sintéticos, los cuales contrarrestan el ataque de plagas y patógenos y coadyuvan a incrementar la producción. Los cambios ambientales, uso de cultivares susceptibles, desgaste de suelos y contaminación obligan a modificar continuamente las prácticas de manejo de los cultivos, lo que incide en un incremento de los costos y aumenta la contaminación ambiental (Vásquez, 2008). Estos problemas han obligado a la búsqueda de alternativas para el manejo integrado de los cultivos como: control biológico, variedades resistentes, plantas transgénicas y abonos orgánicos, entre otras (Zavaleta-Mejía et al., 2003). En algunos cultivos de importancia alimenticia como la papa, se han venido estudiando nuevas opciones para incrementar la producción a través de las respuestas oxidativas y antioxidativas naturales en las plantas, para ser usadas y manipuladas en el manejo integrado de los cultivos (Mora-Herrera y López-Delgado, 2007; Romero-Romero y López-Delgado, 2009).
El estrés aumenta el estado de oxidación de la célula, lo cual induce un incremento en la síntesis de antioxidantes enzimáticos y no enzimáticos para contrarrestar los efectos de dicha oxidación. Los principales antioxidantes enzimáticos son: peroxidasas (POX), catalasa, superóxido dismutasa y glutatión S-transferasa. Los antioxidantes no enzimáticos más importantes son: ácido ascórbico (AA, vitamina C), α-tocoferol (vitamina E), glutatión y β-carotenos (Scandalios, 2005).
Se ha encontrado que algunos compuestos relacionados con las respuestas oxidativas y antioxidativas originadas por factores de estrés, como el ácido ascórbico, están involucrados en las respuestas de tolerancia a estrés biótico y abiótico y desarrollo óptimo (Shen y Yeh, 2010).
El ácido ascórbico está presente en cloroplastos, citosol, vacuolas y espacio apoplástico. El AA es quizás el antioxidante no enzimático más importante en las plantas, que participa en la defensa contra el estrés oxidativo biótico y abiótico por su función en la degradación del H2O2 vía el ciclo del glutatión-ascorbato (Smirnoff, 1996).
El AA participa en muchos procesos fisiológicos tales como: fotosíntesis, cofactor enzimático, homeostasis del sistema redox, como precursor en las rutas de síntesis de moléculas del metabolismo primario y secundario (Smirnoff, 1996) y regulador de POX (Sánchez et al., 1997; Stasolla y Yeung, 2007). Además está involucrado en el crecimiento, desarrollo y modulación del ciclo celular y/o división celular y la elongación celular (De Pinto y De Gara, 2004). Existen evidencias de que el AA aplicado exógenamente en algunos cultivos promueve el crecimiento, lo que lleva a un mejor rendimiento (El-Tohamy et al., 2008); y esto está asociado con un incremento en los pigmentos fotosintéticos como: en canola (Sakr y Arafa, 2009), papa (Romero-Romero y López-Delgado, 2009) y berenjena (Add-ElAziz et al., 2006). Asimismo, se ha reportado que el AA incrementa la resistencia a estrés y reduce el daño contra estrés biótico y abiótico (Shalata y Neumann, 2001; Athar et al., 2008; Romero-Romero y López-Delgado, 2009).
Por otro lado, las POX participan en varias funciones fisiológicas de las plantas tales como: lignificación, entrecruzamiento de polisacáridos de la pared celular, oxidación del ácido indolacético, regulación de la elongación celular y oxidación de fenoles ligados al crecimiento (Yoshida et al., 2003).
En la zona florícola del Estado de México, el cultivo del crisantemo (Dendranthema grandiflora Tzvelev.), especialmente el cultivar Polaris, es importante como flor de corte; se produce principalmente a campo abierto y en túnel (Benavides y Ramírez, 2003).
El objetivo de este estudio fue evaluar el efecto de la molécula antioxidante AA como un compuesto alterno involucrado en las respuestas de desarrollo, específicamente en la respuesta fisiológica de: crecimiento, contenido de pigmentos fotosintéticos, proteína total y la actividad enzimática de las POX, para mejorar el rendimiento en el cultivo de crisantemo cultivar Polaris.
MATERIALES Y MÉTODOS
El trabajo se realizó en un invernadero no tecnificado del Centro Universitario UAEM Tenancingo, ubicado en el km 1.5 de la Carretera Tenancingo-Villa Guerrero, Estado de México, cuyas coordenadas geográficas son: 18° 57' latitud norte y 99° 35' longitud oeste del meridiano de Greenwich, con altitud de 2,200 m.
Como material vegetativo se usaron esquejes con una altura promedio de 7 cm de Dendranthema grandiflora cultivar Polaris, adquiridos en la empresa PLANTAMAR en Santa Ana Ixtlahuatzingo, México, entre marzo y julio de 2008. Las plantas se desarrollaron a una temperatura promedio de 30 °C con una máxima de 50 °C y una mínima de 15 °C, humedad relativa promedio de 30-40 % y luminosidad promedio de 85 %.
Manejo del cultivo
Los esquejes se enraizaron aplicando en la base del tallo alfa naftil acetamida (1.2 g de i. a.·kg-1) y ácido indol-3-butírico (0.6 g de i. a.·kg-1), y se colocaron en charolas con tepojal por 15 días. Después se trasplantaron individualmente a macetas de 20 x 22 cm3; se usó como sustrato peat-moss y agrolita en una relación de 2:1. Las plantas se regaron dos veces por semana y se mantuvieron erguidas con tutores de madera sin desbotonar durante todo el ciclo. La fertilización se realizó dos veces durante el ciclo de cultivo con una solución de 100-50-200 mg·L-1 de N, P y K, para lo cual se utilizaron las sales de urea, fosfato monoamónico y nitrato de potasio.
Aspersiones de ácido ascórbico
Se prepararon soluciones de AA (Reasol) a las concentraciones de 0, 3.4 y 6.8 mM pH 5.7, 24 horas antes de la aplicación (AA oxidado), a las cuales se les agregó polisorbato 20 (Tween) como surfactante al 0.01 % (Romero-Romero y López-Delgado, 2009). Las soluciones se asperjaron sobre el haz de las hojas (15 ml por planta) dos veces por semana a partir de los 30 días de cultivo en invernadero y hasta los 100 días (cosecha). La aplicación se realizó con gota fina usando un aspersor manual (VenusPro) de 2 L de capacidad con boquilla de cono.
Las variables evaluadas fueron: proteína soluble, pigmentos fotosintéticos, actividad enzimática de POX, longitud, peso seco y número de tallos y de botones por planta en plantas de 100 días de cultivo. El experimento se realizó con 40 plantas por tratamiento.
Extracción de proteína
La extracción de proteína se realizó de acuerdo al método de Anderson et al. (1995). Se maceró un fragmento (100 mg) apical de hoja madura de la parte central del tallo principal. La proteína total se extrajo en una proporción de 1:4 ml con el amortiguador de fosfato de potasio (Baker; 50 mM, pH 7.2) conteniendo 5 mM de dithiothreitol (Sigma; DTT), 1 mM de ácido etilen diamino tetracético (Sigma; EDTA) y 2 % de polyvinyl pirrolidona (Baker; PVP). El extracto se centrifugó a 10,000 g durante 10 minutos a 4 °C. El sobrenadante se usó para cuantificar proteína y actividad enzimática de la POX.
Proteína soluble
El contenido de proteína se determinó por el método de Bradford (1976). A 5 µl del sobrenadante se le agregaron 0.25 ml de reactivo de Bradford (Biorad) en un volumen final de 1.2 ml, y después de cinco minutos se midió la absorbancia a 595 nm en un espectrofotómetro (Hach Dr/4000U). La cuantificación de proteína se hizo tomando como referencia albúmina sérica de bovino como estándar.
Peroxidasa (EC 1.11.1.7)
La actividad enzimática de la POX se midió de acuerdo con el método descrito por Srivastava y Dwivedi (1998), en una mezcla de reacción con amortiguador de fosfato de sodio 50 mM pH 7.0, 3.33 mM de guaiacol, 4 mM de H2O2 y 0.020 ml del sobrenadante de la muestra en un volumen final de 3 ml. La reacción se inició con la adición del sobrenadante a 25-28 °C. Como blanco se utilizó amortiguador de reacción sin sobrenadante. La oxidación del sustrato (guaiacol) se midió por el incremento en la absorbancia a 470 nm durante tres minutos en intervalos de 30 segundos. Para determinar la actividad de la POX se usó el coeficiente de extinción del guaiacol ε= 2.6 ·mmol-1·mm-1, en la ecuación nmol·min-1mg-1=(ε) (volumen final/volumen de la muestra) (mg de proteína).
Pigmentos fotosintéticos
La cuantificación de los pigmentos fotosintéticos se hizo de acuerdo al método de Lichtenthaler y Wellburn (1983). Cincuenta mg de tejido de hoja (madura, tomada de la parte central del tallo principal) se maceraron en 2 ml de acetona al 80 % (4 °C). El extracto se centrifugó a 2,500 g durante 10 minutos y el sobrenadante se recuperó y ajustó a 2 ml. Se midió la absorbancia a 470, 646 y 663. Las concentraciones de clorofila a (Chl a), clorofila b (Chl b), xantofilas y carotenoides (x+c) se calcularon empleando las fórmulas:
Chla = 12.21 A663 - 2.81 A646
Chlb = 20.13 A646 - 5.03 A663
Cx+c = (1000 A470 - 3.27 [Chla] -107 [Chlb])/229
Los resultados obtenidos se expresan en mg·g-1 de peso fresco (PF)
El contenido de proteína, la actividad enzimática de la POX y los pigmentos fotosintéticos se midieron en tejido de hoja de 12 plantas por tratamiento.
Diseño experimental y análisis estadístico
Se utilizó un diseño experimental completamente al azar con 40 plantas en bloques de 10 por tratamiento. Se realizó un análisis de varianza (ANOVA) y una comparación de medias mediante la prueba de Tukey (P<0.05); el software utilizado fue StarGraphics plus versión 5.0.
RESULTADOS Y DISCUSIÓN
Los tratamientos de AA en plantas de crisantemo cultivar Polaris incrementaron significativamente la longitud del tallo, peso seco, número de botones y tallos por planta con respecto al testigo; el mejor tratamiento fue la concentración de 6.8 mM de AA, debido a que incrementó la longitud en 17.5 %, el peso seco en 31 %, el número de botones en 48 % y el número de tallos en 31.8 % (Cuadro 1) con respecto al testigo. Estos resultados permiten inferir que el AA aplicado en plantas de crisantemo incrementa la biomasa, lo que en su momento lleva a un aumento en la productividad, que puede ser muy importante para incluir estos tratamientos en el sistema de manejo integrado de dicho cultivo.

Recientemente se encontró que la aplicación exógena de AA incrementó la productividad en plantas de gladiolo (Add-ElAziz et al., 2009), en tubérculos de papa (Romero-Romero y López-Delgado, 2009), en canola (Sakr y Arafa, 2009), berenjena (El-Tohamy et al., 2008), trigo (Athar et al., 2008), haba (Younis et al., 2009) y caoba (Add-ElAziz et al., 2006); incluso el incremento de biomasa de estos cultivos se dio bajo condiciones de estrés biótico o abiótico. Imai et al. (1999) reportaron que la aplicación exógena de AA puede estimular la producción endógena de AA, lo que estimula el crecimiento celular al modificar las condiciones de la pared celular y estimular la división celular (De Pinto y De Gara, 2004; Smirnoff, 1996). El incremento de biomasa inducido por AA observado en el cultivo de crisantemo, puede estar relacionado a su participación en la división de la célula y alargamiento celular.
Por otro lado, los tratamientos de AA en las plantas de crisantemo incrementaron significativamente el contenido de proteína (Figura 1) y pigmentos fotosintéticos (Figura 2) así como la actividad enzimática de la POX (Figura 3). El contenido de proteína incrementó 36 % en las plantas asperjadas con AA a la concentración de 6.8 mM con respecto al testigo, y el contenido de pigmentos aumentó en un 75 % en las plantas tratadas con 3.4 y 6.8 mM de AA con respecto al testigo; aunque la concentración más alta de AA (6.8 mM) indujo un incremento mayor en el contenido de clorofila a y de los carotenoides.

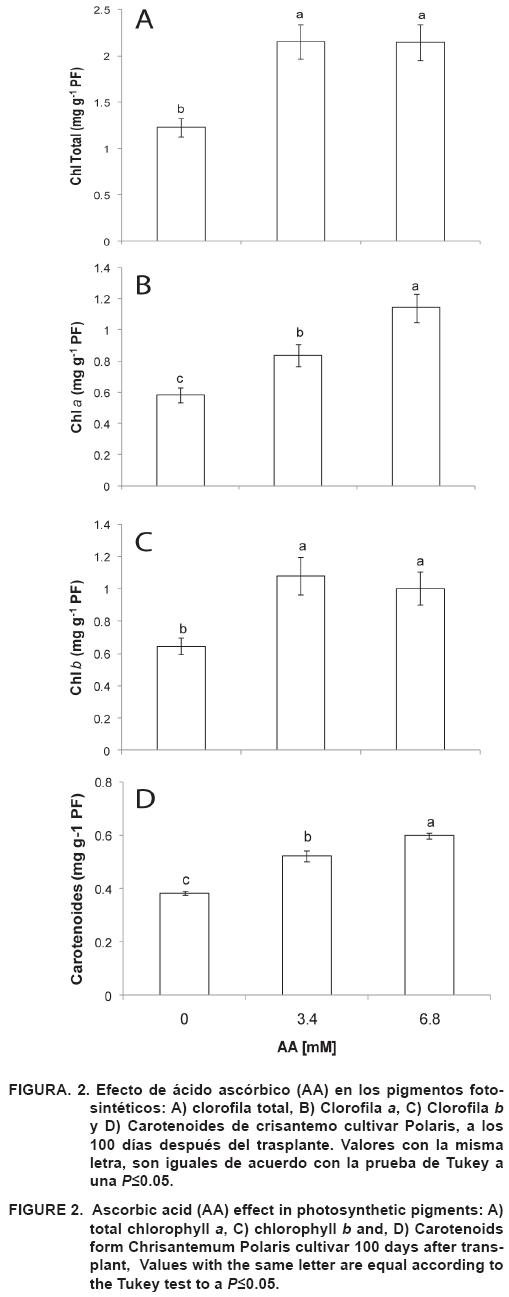

El incremento de proteínas y pigmentos fotosintéticos inducido por las aplicaciones de AA, se relaciona con la acumulación de biomasa observada en las plantas de crisantemo evaluada en este trabajo como longitud, peso seco y número de botones y tallos por planta; respuesta que se ha reportado en otros cultivos como: papa (Romero-Romero y López-Delgado, 2009), caoba (Add-ElAziz et al., 2006), gladiola (Add-ElAziz et al., 2009) y canola (Dolatabadian et al., 2008; Sakr y Arafa, 2009). Además, Athar et al. (2008) reportan que se requiere de una alta capacidad fotosintética para el crecimiento, y esto está ligado a la inducción de las rutas metabólicas en las cuales es necesario el incremento de la síntesis de proteínas en las cuales el AA participa (De Pinto y De Gara, 2004).
Es importante enfatizar que el incremento de pigmentos fotosintéticos inducido por AA en varios cultivos inclusive está relacionado con la protección contra estrés, porque algunos pigmentos fotosintéticos como los carotenoides tienen función antioxidante (Khan et al., 2006; Dolatabadian et al., 2008; 2009; Sark y Arafa, 2009; Romero-Romero y López-Delgado, 2009; Dolatabadian y Jouneghani, 2009), lo que hace a este compuesto potencialmente útil no sólo para el incremento de biomasa, sino también como posible inductor de tolerancia a factores de estrés en el cultivo de crisantemo, ya que se han observado efectos benéficos aun en plantas positivas al virus TSWV (datos no publicados).
Con respecto a la actividad enzimática de la POX, ésta aumentó 33 % en las plantas tratadas con 3.4 y 22 % con 6.8 mM de AA, con respecto al testigo. Esta respuesta es diferente a lo reportado en la literatura. Se ha encontrado que en trigo (Khan et al., 2006; Athar et al., 2008), frijol (Dolatabadian y Jouneghani, 2009) y canola (Dolatabadian et al., 2008) la aplicación de AA no modifica la actividad enzimática de la POX, pero afecta otras enzimas antioxidantes (Athar et al., 2008). En condiciones de estrés salino, inclusive baja los niveles de actividad de la POX (Dolatabadian et al., 2008; 2009) mientras que en Vicia faba los incrementa (Younis et al., 2009). De acuerdo a estas investigaciones y a los resultados obtenidos en este trabajo, la actividad enzimática de la POX va a depender de la concentración, forma de aplicación, número de aplicaciones, tipo de cultivo y etapa fenológica, entre otros factores. La inducción del crecimiento en las plantas de crisantemo por el AA probablemente se deba a que éste participe en alguna función metabólica relacionada con el crecimiento o desarrollo de la pared celular (Stasolla y Yeung, 2007), como se encontró en hipocótilos de pino, donde el AA interviene en la formación de los puentes de dehidrodiferulico y los polisacáridos catalizados por las POX durante el crecimiento celular (Sánchez et al., 1997).
CONCLUSIONES
El AA es un compuesto potencialmente útil para incrementar la biomasa en el cultivo de crisantemo cultivar Polaris, como una alternativa que puede ser encaminada a la productividad.
El AA es un compuesto que puede incluirse en el manejo integrado de los cultivos, por ser un compuesto económico e inocuo al ambiente.
AGRADECIMIENTOS
Al financiamiento otorgado por la Universidad Autónoma del Estado de México UAEM, proyecto 2525/2007U.
LITERATURA CITADA
ADD-EIAZIZ, N. G. A.; MAZHER, M. A. A., EL-HABBA, E. 2006. Effect of foliar spraying with ascorbic acid on growth and chemical constituents of Khaya senegalensis grown under salt condition. American-Eurasian Journal of Agricultural and Environmental Science 1(3): 207-214. [ Links ]
ADD-ELAZIZ, N. G.; TAHA LOBNA, S.; SOAD, M. M. I. 2009. Some studies on the effect of putrescine, ascorbic acid and thiamine on growth, flowering and some chemical constituents of gladiolus plant at nubaria. Ozean Journal of Applied Sciences 2(2): 169-179. [ Links ]
ANDERSON, M. D.; PRASAD, T. K.; STEWART, C. R. 1995. Changes in isozyme profiles of catalase, peroxidase, and glutathione reductase during acclimation to chilling in mesocotyls of maize seedlings. Plant Physiolgy 109: 12471257. [ Links ]
ATHAR, H. R.; KHAN, A.; ASHRAF, M. 2008. Exogenously appied ascorbic acid alleviates salt-induced oxidative stress in wheat. Environmental and Experimental Botany 63: 224231. [ Links ]
BENAVIDES, A.; RAMIREZ, H. 2003. Horticultural science and industry in Mexico overviw, Chronica Horticulturae 43: 2025. [ Links ]
BRADFORD, M. M. 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry 72(1-2): 248-254. [ Links ]
DE PINTO, M. C.; DE GARA, L. 2004. Changes in the ascorbate metabolism of apoplastic and symplastic spaces are associated with cell differentiation. Journal of Experimental Botany 55(408): 2559-2569. [ Links ]
DOLATABADIAN, A.; JOUNEGHANI, R. S. 2009. Impact of exogenous ascorbic acid on antioxidant activity and some physiological traits of common bean subjected to salinity stress. Notulae Botanicae Horti Agrobotanici Cluj-Napoca 37(2): 165-172. [ Links ]
DOLATABADIAN, A.; SANAVY, S. A. M. M.; CHASHMI, N. A. 2008. The effects of foliar application of ascorbic acid (vitamin C) on antioxidant enzymes activities, lipid peroxidation and proline accumulation of canola (Brassica napus L.) under conditions of salt stress. Journal of Agronomy and Crop Science 194: 206-213. [ Links ]
DOLATABADIAN, A.; SANAVY, S. A. M. M.; SHARIFI, M. 2009. Alleviation of water deficit stress effects by foliar application of ascorbic acid on Zea mays L. Journal of Agronomy and Crop Science 195: 347-355. [ Links ] EL-TOHAMY, W. A.; EL-ABAGY, H. M.; EL-GREADLY, N. H. M. 2008. Studies on the effect of putrecine, yeast and vitamin C on growth, yield and physiological responses of eggplan (Solanum melongena L.) under sandy soil conditions. Australian Journal of Basic and Applied Sciences 2(2): 296-300. [ Links ]
IMAI, T.; KINGSTON-SMITH, A. H.; FOYER, C. H. 1999. Ascorbate metabolism in potato leaves supplied with exogenous ascorbate. Free Radical Research 31: S171-S179. [ Links ]
KHAN, A.; AHMAD, M. S. A.; ATHAR, H-R.; ASHRAF, M. 2006. Interactive effect of foliarly applied ascorbic acid and salt stress on wheat (Triticum aestivum L.) at the seedling stage. Pakistan Journal of Botany 38(5): 1407-1414 [ Links ]
LICHTENTHALER, H. K.; WELLBURN, A. R. 1983. Determinations of total carotenoids and chlorophylls a and b of leaf extracts in different solvents. Biochemical Society Transactions 11: 591-592. [ Links ]
MORA-HERRERA, M. E.; LÓPEZ-DELGADO, H. A. 2007. Freezing tolerance and antioxidant activity in potato microplants induced by abscisic acid treatment. American Journal of Potato Research 84: 487-495. [ Links ]
ROMERO-ROMERO, M. T.; LÓPEZ-DELGADO, H. A. 2009. Ameliorative effects of hydrogen peroxide, ascorbate and dehydroascorbate in Solanum Tu,erosum Infected by phytoplasma. American Journal of Potato Research 86: 218-226. [ Links ]
SAKR, M. T.; ARAFA, A. A. 2009. Effect of some antioxidants on canola plants grown under soil salt stress condition. Pakistan Journal of Biological Sciences 12 (7): 582-588. [ Links ]
SÁNCHEZ, M.; QUEIJEIRO, E.; REVILLA, G.; ZARRA, I. 1997. Changes in ascorbic acid levels in apoplastic fluid during growth of pine hypocotyls. Effects on peroxidase activities associated with cell walls. Physiologia Plantarum 101: 815-820. [ Links ]
SCANDALIOS, J. G. 2005. Oxidative stress: molecular perception and transduction of signals triggering antioxidant gene defenses. Brazilian Journal of Medical and Biological Research 38: 995-1014. [ Links ]
SHALATA, A.; NEUMANN, P. M. 2001. Exogenous ascorbic acid (vitamin C) increases resistance to salt stress and reduces lipid peroxidation. Journal of Experimental Botany 52(364): 2207-2211. [ Links ]
SHEN, C-H.; YEH, K-W. 2010. The signal network of ascorbate homeostasis. Plant Signaling and Behavior 5(5): 570-572. [ Links ]
SMIRNOFF, N. 1996. The function and metabolism of ascorbic acid in plants. Annals of Botany 78: 661-669. [ Links ]
SRIVASTAVA, M. K.; DWIVEDI, U. N. 1998. Salicylic acid modulates glutathione metabolism in pea seedlings. Journal of Plant physiology 153(3-4): 409-414. [ Links ]
STASOLLA, C.; YEUNG, E. C. 2007. Cellular ascorbic acid regulates the activity of mayor peroxidases in the apical poles of germinating white spruce (Picea glauca) somatic embryos. Plant Physiology and Biochemistry 45: 188-198. [ Links ]
VÁSQUEZ, Y. 2008. Impacto en la salud asociado al uso de agroquímicos en la comunidad de Santa Ana Ixtlahuatzingo, municipio de Tenancingo, Estado de México. Boletín Informativo de Geografía de la Salud Núm. 6. [ Links ]
YOSHIDA, K.; KAOTHIEN, P.; MATSUI, T.; KAWAOKA, A. 2003. Molecular biology and application of plant peroxidase genes. Applied microbiology and Biotechnology 60(6): 665670 [ Links ]
YOUNIS, M. E.; HASANEEN, M. N. A.; KAZAMENT, A. M. S. 2009. Exogenously applied ascorbic acid ameliorates detrimental effects of NaCl and mannitol stress in Vicia faba seedlings. Protoplasma 239(1-14): 39-48. [ Links ]
ZAVALETA-MEJÍA, E.; ROJAS, M. R. I.; OCHOA, M. D. L. 2003. Manejo Ecológico de Enfermedades. Instituto de Fitosanidad. Colegio de Postgraduados, Montecillo, Estado de México. 114 p. [ Links ]














