Introducción
Los tumores del estroma gastrointestinal (GIST) son las neoplasias mesenquimales más comunes, representan 80% de estas últimas y son parte de un grupo de neoplasias no epiteliales de la tercera y cuarta capa (submucosa y muscular propia), pueden ser mesenquimales como un tumor estromal de diversos orígenes, por ejemplo los GIST, leiomioma, lipoma, tumor de la vaina de los nervios (schwannomas) o también pueden ser linfomas.1 Las tasas anuales de incidencia reportadas en todo el mundo son inferiores a 10-20 por millón, sin diferencias en género o raza. Es una enfermedad que puede surgir en cualquier parte del tracto digestivo en adultos.2
El GIST debe ser considerado un tumor raro: los estándares aceptados consideran que una enfermedad es rara cuando la prevalencia es menor de un caso entre cada 2,000 personas. Para el caso de los tumores, los indicadores señalan como rara a una neoplasia que se presenta en menos de tres de cada 100,000 individuos.3
Cuadro clínico
Los GIST suelen diagnosticarse en la quinta y sexta década de la vida con una frecuencia mayor en pacientes masculinos.4 El estómago (60%) y el yeyuno-íleon (30%) son los sitios primarios más comunes, y sólo un pequeño número de casos se ha reportado en colon y recto (< 5%), esófago y apéndice (< 1%);5 sin embargo, también se han descrito casos de GIST localizados en páncreas, vesícula biliar, mesenterio, epiplón mayor, epiplón menor y retroperitoneo (1.5 a 5%).5,6 Las lesiones duodenales representan aproximadamente del 3 al 5% de los casos.6,7
La manifestación secundaria más frecuente es la hemorragia macroscópica o en forma oculta en heces, la segunda manifestación es el dolor abdominal y también puede estar presente una tumoración, probablemente por compresión de los órganos vecinos, en particular en los casos en que el tumor alcanza un tamaño significativo.8
Estudios auxiliares para diagnóstico
Endoscopia digestiva
Es la primera prueba en los pacientes con hemorragia gastrointestinal. Endoscópicamente, se observa una protrusión lisa, de base amplia, con una mucosa normal, aunque en ocasiones hay una ulceración central. Los GIST se observan como tumores submucosos elevados, bien delimitados, a veces ulcerados y con coágulos (los cuales son datos sugestivos de malignidad) y son fácilmente identificados en la primera y segunda porción duodenales.9
Ultrasonografía endoscópica
Permite definir con gran precisión las distintas capas del tubo digestivo y visualizar los órganos vecinos, lo que la convierte en el mejor método diagnóstico de las lesiones submucosas del tracto digestivo. Sin embargo, la endosonografía no puede discernir entre un GIST y algún otro tumor de la pared intestinal como un leiomioma, por esta razón se recomienda la biopsia por aspiración con aguja fina para el diagnóstico histológico de la lesión.9
La biopsia con aguja trucut se ha utilizado asociada a la endosonografía, logrando diagnosticar adecuadamente GIST en 79% de los casos mediante histología y hasta en 97% cuando se utiliza inmunohistoquímica, pero este método no puede utilizarse en GIST menores de 3 cm, a menos que se prepare un bloque celular a partir de la obtención tisular para su envío a estudio histológico sujeto a prueba de inmunohistiquímica.10 Se han establecido algunos criterios endosonográficos que permiten la sospecha de un GIST maligno mediante este examen con especificidad de 80% y sensibilidad de 77% (Tabla 1).11
Tabla 1: Criterios endosonográficos para la sospecha de GIST malignos.31
| Tamaño tumoral >3 cm |
| Aspecto heterogéneo |
| Áreas hiperecogénicas |
| Áreas hipoecogénicas |
| Margen tumoral irregular |
| Margen tumoral lobulado |
| Calcificaciones en la pared e intratumorales |
| Aspecto quístico |
Tomado de: Beltrán MA, Valenzuela C, Diaz R, Haito Y, Larrai C. Tumores del estroma gastrointestinal del duodeno: revisión de literatura científica actual con énfasis en el tratamiento. Rev Colomb Cir. 2014; 29: 140-154.
Tomografía axial computarizada
El estudio radiológico con mayor disponibilidad en la actualidad para identificar y diagnosticar GIST es la tomografía axial computarizada (TAC). Prácticamente todos los GIST duodenales son detectados con TAC.12
Es la técnica de elección para detectar invasión local del tumor y enfermedad metastásica, los GIST son tumores hipervasculares que muestran un intenso contraste en la fase arterial. La mayoría muestra un contraste homogéneo y aparecen como masas endofíticas o exofíticas bien definidas.13
Resonancia magnética
Se considera útil en los GIST grandes y exofíticos para establecer su localización y relaciones con los órganos vecinos. Está indicada especialmente en los GIST anorrectales.14
Tomografía por emisión de positrones
Los GIST presentan gran avidez por el trazador 18F-fluoro-2-deoxi-D-glucosa (FDG) utilizado en la tomografía por emisión de positrones (PET). En la actualidad, se ha comprobado que la asociación PET/TAC mejora la precisión diagnóstica de las metástasis y el seguimiento de la respuesta clínica al tratamiento farmacológico. El PET es capaz de detectar lesiones tumorales de hasta 1 cm y metástasis epiplóicas que pasan desapercibidas en la TAC.15
Biopsia
La biopsia no es necesaria cuando hay una sospecha elevada de GIST y éste sea resecable. Sin embargo, en los casos en que la lesión submucosa sea indeterminada o que haya enfermedad metastásica y se plantee tratamiento paliativo, deberá obtenerse siempre el diagnóstico histológico por PAAF-USE (punción-aspiración con aguja fina guiada por ultrasonido endoscópico), la cual ha demostrado ser una técnica segura y poco invasiva con una sensibilidad del 100% y una especificidad del 80%. La precisión diagnóstica de la PAAF-USE aumenta con el diámetro tumoral del 71% (tumores < 2 cm) al 100% (tumores > 4 cm). No se recomienda realizar una biopsia percutánea, puesto que los GIST son lesiones hipervasculares y presentan riesgo de rotura y de diseminación peritoneal.16
Histopatología y biología molecular
Desde el punto de vista histológico y molecular, los GIST se caracterizan por:
Morfología fusiforme (70%), epitelioide (20%) o mixta.
Los GIST expresan un receptor proteico transmembrana de la familia de las tirosincinasas (KIT), codificado por el protooncogén c-kit ubicado en el cromosoma 4 (4q11-q12) que se cree que controla la proliferación celular y la apoptosis.17
Las biopsias tomadas con aguja fina guiadas por ultrasonido endoscópico pueden evidenciar a través de la inmunohistoquímica a Ki-67 o CD 117 para GIST.
Hirota y colaboradores, en 1998, demostraron el papel de la mutación de este protooncogén en el proceso de esta enfermedad,17 en la que la proteína KIT está presente en 90% de los GIST y se considera un marcador específico de estos tumores. Se trata de un receptor de membrana con una porción tirosincinasa, cuya activación es clave para la proliferación y supervivencia celular, y está hiperactivada en los GIST.18,19
Se han descubierto al menos dos mutaciones proactivadoras de la actividad tirosinasa de KIT y de otro receptor emparentado con KIT denominado PDGFR-α. Este hallazgo clasifica a los GIST desde el punto de vista molecular en tres subtipos: KIT-positivo (90%), PDGFR-positivo (5%), y KIT/PDGFR-negativo (5%), esta diferenciación puede tener implicaciones pronósticas y terapéuticas.19
Todos los GIST albergan algún potencial maligno, aunque sólo del 10% al 30% son clínicamente malignos y representan 1% de todos los tumores malignos del aparato digestivo. Los GIST primarios no se clasifican como benignos o malignos, pero se estratifican por la probabilidad de recurrencia después de la resección completa en un riesgo muy bajo, bajo, intermedio y alto con base en su tamaño y tasa mitótica con criterios de Fletcher (Tabla 2).20
Tabla 2: Clasificación pronóstica de Fletcher.
| Riesgo | Tamaño | Índice de proliferación |
|---|---|---|
| Muy bajo | < 2 cm | < 5/50 HPF |
| Bajo | Entre 2 y 5 cm | < 5/50 HPF |
| Medio | < 5 cm | 6-10/50 HPF |
| Alto | 5-10 cm | < 5/50 HPF |
| > 10 cm | Cualquiera | |
| Cualquiera | > 10/50 HPF |
* HPF = High power field, CGA = Campos de gran aumento.
Elaboración propia.
Los criterios de Fletcher relacionan el tamaño del tumor y el número de mitosis con el riesgo de comportamiento agresivo. La PET-18F-FGD ofrece información sobre la actividad metabólica y permite calibrar el grado de malignidad, ya que a mayor captación de glucosa por parte del tumor, mayor actividad metabólica y por tanto, mayor agresividad.21
GIST duodenales en pacientes con neurofibromatosis de tipo 1
La presencia de los GIST se observa ocasionalmente; sin embargo en 5% de los casos se aparecen asociados a un síndrome familiar, siendo la neurofibromatosis de tipo 1 el más común; además, se describen en la tríada de Carney y en el síndrome de Carney-Stratakis.22
El origen anatómico puede ser otro factor independiente para la estratificación del riesgo. Aunque los GIST duodenales son relativamente raros, representan 30% de todos los tumores primarios del duodeno y la gran mayoría de los pacientes tienen hemorragia gastrointestinal.23 En relación al tratamiento, los GIST duodenales representan un reto quirúrgico debido a la complicada relación anatómica alrededor del duodeno, a diferencia del estómago u otros segmentos intestinales donde es más fácil la completa resección con márgenes amplios. La resección amplia de los GIST duodenales, por lo regular, implicará una pancreaticoduodenectomía (PD), que es muy invasiva y quirúrgicamente desafiante.24
En los últimos años ha incrementado la tendencia de una resección limitada (LR), la cual ha demostrado un efecto comparable a PD en casos seleccionados. Sin embargo, el enfoque quirúrgico óptimo (LR o PD) para GIST duodenal aún no está estandarizado, ya que todas las pruebas disponibles se han derivado de pequeñas series retrospectivas. Debido a sus relaciones anatómicas estos tumores han sido clasificados separadamente de otros GIST del intestino delgado en una categoría separada.24
Tratamiento neoadyuvante
El primer inhibidor exitoso de moléculas pequeñas fue el mesilato de imatinib, inicialmente desarrollado como inhibidor específico de PDGFRα. Los GIST con mutaciones del exón 11 tienen la mejor respuesta clínica al imatinib; los pacientes sin mutaciones de la KIT o de PDGFRα no mejoran con imatinib.25 La United States Food and Drug Administration aprobó el uso del imatinib para tratamiento de GIST en el año 2002.25,26
Las indicaciones de tratamiento neoadyuvante con imatinib son la reducción tumoral preoperatoria y los tumores metastásicos avanzados. En casos seleccionados de GIST localmente avanzado o marginalmente resecable, la estrategia de citorreducción con imatinib neoadyuvante es una estrategia plausible. El uso de imatinib neoadyuvante en la práctica rutinaria asociada a cirugía tiene buenos resultados a largo plazo.25,26
Los candidatos para imatinib preoperatorio son aquellos pacientes que se beneficiarían de la reducción del volumen tumoral antes de la operación o en tumores con localizaciones complejas como los GIST duodenales de la segunda y la tercera porción.26
En algunas series de GIST duodenales, el imatinib se ha utilizado en el preoperatorio con buenos resultados en pacientes con tumores grandes, candidatos a pancreatoduodenectomía. En estos casos se reduce la fragilidad del tumor disminuyendo el riesgo de hemorragia y la posibilidad de rompimiento de la cápsula.26
Dosis y manejo del tratamiento neoadyuvante con imatinib
La dosis recomendada de imatinib es de 400 mg diarios hasta alcanzar la reacción máxima, que se confirma con dos TACs consecutivas que no muestran mayor regresión del tumor. Se requiere de un tratamiento preoperatorio de cuatro a 12 meses para alcanzar el efecto máximo.26
Abordaje quirúrgico
La resección quirúrgica completa constituye el único tratamiento curativo. El tratamiento quirúrgico óptimo incluye la resección del tumor con márgenes libres que puede incluir los órganos adyacentes. Los GIST no se diseminan por vía linfática y no presentan crecimiento submucoso, además son tumores bien encapsulados que raramente invaden órganos vecinos, por lo que la resección local o la duodenectomía segmentaria se considera suficiente y se asocia a una prolongada supervivencia libre de enfermedad. En los pacientes con GIST primarios, la resección quirúrgica ofrece una tasa de supervivencia a los cinco años de 48 a 70%.27
A diferencia de los GIST localizados en otros lugares del tubo digestivo, el tratamiento quirúrgico óptimo para los duodenales no se encuentra bien caracterizado y su establecimiento es escaso en la literatura quirúrgica.28
La resección quirúrgica puede llevarse a cabo mediante varias opciones. El abordaje debe ser dictado por la localización del tumor en el duodeno y por la capacidad para lograr una resección R0. La cirugía local o conservadora consiste en la resección en cuña o la resección de un segmento, debe tenerse en cuenta la anatomía duodenal y su proximidad a estructuras adyacentes como la ampolla de Vater, el páncreas, los vasos mesentéricos, el colédoco y el conducto pancreático.29
La resección local muchas veces es difícil, especialmente en la segunda porción. En la práctica clínica, hasta 86% de los GIST duodenales han sido tratados mediante pancreatoduodenectomía. Las opciones quirúrgicas reportadas para estos tumores dependen de su localización y su tamaño30 (Tabla 3).
Tabla 3: Procedimientos quirúrgicos de acuerdo con la localización del GIST en el duodeno.30
| Porción | Primera | Segunda | Tercera | Cuarta |
|---|---|---|---|---|
| Pared lateral | • Resección en cuña | • Resección en cuña más cierre primario/duodenoyeyunostomía, en Y de Roux | • Resección en cuña más cierre primario/duodenoyeyunostomía en Y de Roux | • Resección en cuña |
| GIST < 3 cm | • Resección segmentaria más Billroth I/gastro-yeyunostomía en Y de Roux | • Resección segmentaria más duodeno-yeyunostomía primaria | ||
| GIST >3 cm | • Resección segmentaria/antrectomía más gastroyeyunostomía en Y de Roux | • Whipple | • Whipple | • Resección segmentaria más duodeno-yeyunostomía primaria |
| • Whipple | • Resección segmentaria más duodeno duodenostomía | |||
| • Resección de la tercera y cuarta porción más duodenoyeyunostomía | ||||
| Pared medial | • Resección en cuña | • Whipple | • Whipple | • Resección segmentaria más duodeno yeyunostomía primaria |
| GIST < 3 cm | • Resección segmentaria más Billroth I/gastro-yeyunostomía en Y de Roux | • Resección segmentaria más duodeno-duodenostomía | ||
| • Resección de la tercera y cuarta porción más duodenoyeyunostomía | ||||
| GIST > 3 cm | • Whipple | • Whipple | • Whipple | • Whipple |
| • Resección segmentaria más duodeno yeyunostomía primaria |
Primera porción del duodeno
Los tumores localizados hacia la pared medial que se encuentran en contacto íntimo con la cabeza del páncreas, deben ser tratados mediante pancreatoduodenectomía. Los localizados en la pared lateral, cuando son menores de 3 cm, pueden tratarse mediante resección en cuña y sutura primaria o resección segmentaria31 (Figura 1).

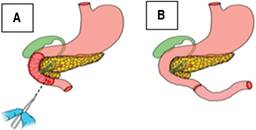
Figura 1: Procedimientos quirúrgicos para GIST de la primera porción duodenal. (A) Resección en cuña con sutura primaria. (B) Resección segmentaria con anastomosis primaria. (C) GIST que requiere resección segmentaria extensa. (D) Reconstrucción con anastomosis gastro-yeyunal en Y de Roux después de resección segmentaria ampliada al antro gástrico.
Segunda porción del duodeno
Los localizados en la pared medial del duodeno en contacto con la cabeza del páncreas o con la ampolla de Vater deben ser sometidos a pancreatoduodenectomía.31
Los tumores localizados en la pared lateral pueden tratarse mediante resección local en cuña con cierre primario o duodenectomía distal y reconstrucción mediante anastomosis entre el yeyuno y el duodeno restante o mediante anastomosis duodeno-yeyuno en Y de Roux.31 (Figura 2).
Tercera porción del duodeno
Los tumores pequeños o medianos localizados en la pared medial o lateral pueden tratarse mediante resección de la tercera y cuarta porción duodenal, y anastomosis término-terminal o lateroterminal primaria con el yeyuno (Figura 3 A y B). Cuando la resección en cuña deja un defecto muy grande y el cierre primario no es posible, el defecto puede resolverse mediante duodeno-yeyunostomía en Y de Roux (Figura 3 C y D). Cuando el tumor es muy grande con infiltración al páncreas, la pancreatoduodenectomía es la opción.31

Figura 3: Procedimientos quirúrgicos para GIST de la tercera porción duodenal. (A) Duodenectomía distal que incluye la tercera y cuarta porción del duodeno. (B) Reconstrucción de la duodenectomía distal mediante una duodeno-yeyunostomía término-terminal. (C) Resección en cuña de la tercera porción del duodeno. (D) Reconstrucción de la resección mediante una duodeno-yeyuno anastomosis en Y de Roux.
Cuarta porción del duodeno
Los GIST localizados en la cuarta porción pueden resecarse localmente y el tránsito intestinal se puede restaurar mediante anastomosis primaria término-terminal o lateroterminal entre la tercera porción duodenal y el yeyuno (Figura 4). Los tumores pequeños pueden tratarse mediante resección en cuña.31
Cirugía laparoscópica
La cirugía laparoscópica ha mostrado ventajas sobre las cirugías abiertas tradicionales mostrando una reducción en el dolor postoperatorio, menor incidencia de infecciones, menor riesgo de hernia o dehiscencia asociada con incisiones, así como una recuperación postoperatoria más rápida y como resultado una corta estancia hospitalaria. La laparoscopia proporciona resultados equivalentes a la cirugía abierta siempre que se logren márgenes negativos; sin embargo, existen todavía muy pocos reportes en la literatura sobre el uso de la resección laparoscópica para el GIST no gástrico.32
El uso de la técnica laparoscópica en GIST grandes y de ubicación con difícil acceso es limitado. La Red Nacional Integral del Cáncer restringe el uso de laparoscopia para tumores de menos de 2 cm de dimensión. En los GIST con difícil acceso, la movilidad del instrumento quirúrgico se ve afectada y la sutura se vuelve difícil de realizar; también puede dar como resultado márgenes de resección inadecuados y en consecuencia, progresión de la enfermedad, recurrencia y corta supervivencia. El sistema quirúrgico Da Vinci ofrece ergonomía superior, visión mejorada, precisión, destreza y control para que los cirujanos operen. Estudios recientes también encontraron que la resección robótica de mínima invasión fue oncológicamente segura y dio lugar a resultados favorables como un retorno más temprano de la función intestinal, reanudación más temprana de la dieta, menor duración del uso de la analgesia y una hospitalización postoperatoria más corta. No obstante, sólo se han publicado unos cuantos estudios sobre el uso del sistema Da Vinci en oncología.33
Otras técnicas de mínima invasión como serían la resección endoscópica por tunelización submucosa, la resección endoscópica de espesor total y la cirugía cooperativa endoscópica laparoscópica han mostrado buenos resultados clínicos, aunque todavía no se cuenta con estudios suficientes sobre su seguridad a largo plazo y aún se encuentran bajo investigación clínica.34
Tratamiento adyuvante
El mesilato de imatinib es la primera línea de tratamiento en pacientes con GIST avanzado, el cual mejora la supervivencia libre de enfermedad y la supervivencia general. Este medicamento ha sido aprobado para su uso después de la resección de GIST con elevado riesgo de recurrencia, a una dosis de 400 mg diarios. El maleato de sunitinib es la segunda línea de tratamiento para casos de GIST resistentes al imatinib.35
Pronóstico
La resección segmentaria o en cuña de GIST duodenal ha demostrado ser suficiente y curativa con una supervivencia libre de enfermedad satisfactoria en series que reportan sólo tumores del duodeno. La Tabla de pronóstico para GIST, desarrollada en el año 2001 por el taller de consenso patrocinado por The National Institutes of Health y The National Cancer Institute, recientemente modificada por Joensuu, es la que se utiliza para establecer el pronóstico de estos pacientes. La supervivencia a cinco años para tumores mayores de 10 cm es del 20% y en tumores menores de 5 cm llega a 65%. En pacientes operados por GIST duodenal localizado, a tres años la supervivencia global es de 98% y libre de enfermedad de 67%, y a cinco años la global es de 89% y libre de enfermedad es de 64%.35
Todos los GIST se asocian a riesgo de recurrencia; de 40 a 50% de todos los pacientes con resecciones potencialmente curativas desarrollan metástasis o recurrencias. A pesar del conocimiento actual sobre su biología, estos tumores se comportan erráticamente; aun en GIST de bajo riesgo se han reportado recurrencias a 20 o más años después de la resección quirúrgica. En 39% de los pacientes con GIST duodenal se han descrito recurrencias. En tumores de alto riesgo la recurrencia es inevitable. En casos de seguimiento de dos años se han encontrado recurrencias en 19%, con metástasis a distancia en 13 a 23%, recurrencia local en 2 a 15%, y recurrencia sincrónica local y a distancia en 4%. El lugar más común para el desarrollo de metástasis es el hígado. Sin embargo, es interesante que después de más de una década de investigación intensiva las conclusiones son las mismas, los factores determinantes de supervivencia más importantes son el recuento de mitosis y el tamaño tumoral.35
Presentación del caso
Se presenta paciente femenino de 54 años de edad con antecedentes de neurofibromatosis diagnosticada a los 35 años de edad. Tuvo tres episodios de sangrado de tres, dos y un año de evolución respectivamente, en el último de los cuales requirió de transfusión sanguínea. Cursó con diagnóstico de un año previo de pólipo duodenal ubicado en segunda porción del duodeno, justo delante de ampolla de Vater.
El estudio histopatológico informó la presencia de un tumor del estroma gastrointestinal, la tomografía axial computarizada reportó de igual manera un tumor en la segunda porción del duodeno de 42 × 36 mm y el estudio inmunohistoquímico de la biopsia tomada con aguja fina guidadas por ultrasonido endoscópico fue positivo para CD117, CD34 y DOGL. El ultrasonido endoscópico mostró una lesión en la pared lateral de la segunda porción del duodeno.
Dichos estudios se realizaron como protocolo de estudio durante el transcurso del año 2016, mismo que al concluir se optó por el abordaje quirúrgico mediante una incisión media supraumbilical, ya que se identificó un tumor de 3 cm en la pared lateral del duodeno. Se realizó resección en cuña dando margen macroscópico de 1 cm a la lesión tumoral haciendo un cierre primario en dos planos, como material de sutura se utilizó catgut crómico 2/0 y para el segundo plano seromuscular se empleó seda 2/0, para el manejo postquirúrgico se administró antibiótico terapia a base de ceftriaxona 1 g IV cada 12 horas por ocho días y manejo analgésico con tramadol 200 mg en infusión para 24 horas con ketorolaco 30 mg IV cada ocho horas (Figuras 5 y 6).
La paciente evolucionó sin complicaciones y fue dada de alta al octavo día con seguimiento por la consulta externa de cirugía general y oncología quirúrgica; durante el seguimiento por la consulta externa se contó con estudio de patología que reveló tumor duodenal compatible con tumor del estroma gastrointestinal de bajo riesgo de malignidad, de tamaño de 4 × 3 × 3 cm, con bordes quirúrgicos libres de tumor a 1 mm (Figura 7) y se envió a interconsulta para valoración al servicio de oncología médica que fue analizada el día 14 de diciembre de 2016 para continuar con protocolo de estudio y seguimiento, el cual inició con manejo a base de imatinib 400 mg cada 24 horas por 36 meses autorizado el 24 de enero de 2017.

Figura 7: A (HE 10X) y B (40). En (A) se observa una proliferación neoplásica mesenquimatosa, intramural, bien delimitada, no encapsulada, formada por células alargadas (patrón fusocelular), con escaso pleomorfismo. (B) Las células son alargadas, dispuestas en forma arremolinada, con núcleos de aspecto vesiculoso, escaso pleomorfismo y menos de dos mitosis/50 CAP.
Actualmente, la paciente asiste a seguimiento médico en los servicios de cirugía general, oncología quirúrgica y oncología médica con últimos reportes de control del día 12 de febrero de 2018 de PET/TAC con 18F-FDG sin evidencia de actividad metabólica aumentada.
Discusión
El tratamiento primario de los GIST duodenales es el abordaje quirúrgico, con resección tumoral completa y obtención de márgenes adecuadas; en algunos casos se puede planear una cirugía conservadora como en el caso de nuestra paciente.
Exponemos el tratamiento quirúrgico más frecuente del GIST duodenal. La resección local es apropiada cuando es factible y la pancreaticoduodenectomía debe reservarse para lesiones que no son susceptibles de resección local, por ejemplo, aquéllas que afectan la ampolla de Vater o las que tienen criterios de irresecabilidad de Fletcher. Nuestra paciente presenta bajo riesgo por tener un tamaño de tumor entre 2 y 5 cm (3 cm) y con una cuenta de menos de dos mitosis/50 CAP, por lo que la resección quirúrgica completa constituye el único tratamiento curativo y el tratamiento quirúrgico óptimo incluye la resección del tumor con márgenes libres.
Los GIST no se diseminan por vía linfática y no presentan crecimiento submucoso; además, son tumores bien encapsulados que raramente invaden órganos vecinos, por lo que la resección local o la duodenectomía segmentaria se considera suficiente y se asocia a una prolongada supervivencia libre de enfermedad. Por esta razón, los tumores localizados en la pared lateral de la segunda porción pueden tratarse mediante resección local en cuña con cierre primario o duodenectomía distal y reconstrucción mediante anastomosis entre el yeyuno y el duodeno restante o mediante anastomosis duodeno-yeyunal en Y de Roux. En el caso concreto de nuestra paciente, la opción quirúrgica fue la resección en cuña con cierre primario en dos planos como se recomienda en la presente revisión de literatura.
Nuestra paciente recibió terapia adyuvante a base de imatinib 400 mg/día correspondiendo con nuestra revisión bibliográfica, ya que el mesilato de imatinib es la primera línea de tratamiento en pacientes con GIST avanzado, el cual mejora la supervivencia libre de enfermedad y la supervivencia general. En cuanto al pronóstico, basándonos en la Tabla pronóstica de GIST primarios modificada por Joensuu, tenemos que en tumores menores de 5 cm la supervivencia llega a 65% a los cinco años.
Conclusión
El manejo de estos pacientes es multidisciplinario, integrado por radiólogos, oncólogos, gastroenterólogos, cirujanos, endoscopistas gastrointestinales y endosonografistas. Prácticamente la mitad de los casos se diagnostican de forma incidental. Los GIST deben tomarse en cuenta en el diagnóstico diferencial de los tumores digestivos ante la presencia de anemia o hemorragia digestiva de origen incierto.
El tratamiento de elección es quirúrgico, logrando una resección completa del tumor en 70 a 80% de los casos. La quimioterapia y la radioterapia tienen utilidad limitada, por lo que existen tratamientos como los inhibidores de tirosina quinasa que disminuyen la actividad del tumor en casos irresecables.
En comparación con la literatura, el protocolo que tuvo la paciente de este caso clínico fue adecuado y necesario tanto para su plan quirúrgico como para su tratamiento postquirúrgico. Al contar con las características antes mencionadas la mejor elección fue la resección en cuña, ya que este abordaje ha ido ganando aceptación por su menor morbimortalidad en comparación con la duodenopancreatectomía.
La mayoría de los reportes sobre GIST duodenales mencionan que el tratamiento quirúrgico óptimo no se ha determinado. Esto se debe a que no se han hecho estudios clínicos aleatorios y a que los reportes publicados constituyen la experiencia de uno o más centros de referencia. La revisión cuidadosa de estas publicaciones demuestra que los abordajes quirúrgicos para GIST duodenal son bastante estandarizados, tomando en cuenta la localización del tumor en el duodeno y sus relaciones anatómicas para decidir el tipo de abordaje quirúrgico.











 nueva página del texto (beta)
nueva página del texto (beta)