Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Agrociencia
versión On-line ISSN 2521-9766versión impresa ISSN 1405-3195
Agrociencia vol.42 no.4 Texcoco may./jun. 2008
Fitociencia
Optimización del proceso de extracción de flavonoides de flor de manzanilla (Matricaria recutita L.)
Optimization of the process of flavonoid extraction from chamomile (Matricaria recutita L.)
José C. Meneses–Reyes1, Ramón M. Soto–Hernández1* , Teodoro Espinosa–Solares3 y Martha E. Ramírez–Guzmán
1 Botánica,*(Autor responsable) (jcmeneses@colpos.mx) (msoto@colpos.mx)
2 Estadística. Campus Montecillo. Colegio de Postgraduados. 56230. km 36.5 Carretera México–Texcoco. Estado de México.
3 Ingeniería Agroindustrial. Universidad Autónoma Chapingo. 56230. km 38.5 Carretera México–Texcoco. Estado de México (espinosa@correo.chapingo.mx)
Recibido: Junio, 2007.
Aprobado: Enero, 2008.
Resumen
Matricaria recutita L. tiene varios usos medicinales, alimenticios y cosméticos. Su flor contiene altas cantidades de flavonoides, principalmente apigenina; su acción farmacológica y la calidad del extracto hidro–alcohólico varían según el contenido de este compuesto. Para optimizar el proceso de extracción de flavonoides y obtener un mayor rendimiento se usó el método de Taguchi. Los factores analizados fueron tiempo–temperatura (1–4 h a 70±0.5 °C y 12–48 h a 20 ±2 °C), proporción del disolvente metanol:agua (50:50 a 80:20) y tamaño de partícula de la flor (<0.42 y >2.00 mm). Para cuantificar flavonoides se usó el método colorimétrico cloruro de aluminio. La combinación óptima de niveles que maximiza (p<0.05) el rendimiento de flavonoides es el proceso realizado en 1 h a 70±0.5 °C, con una proporción del disolvente metanol:agua de 80:20 y un tamaño de partícula grande (>2.00 mm).
Key words: Matricaria recutita L., cloruro de aluminio, flores liguladas, metanol:agua, modelo Taguchi.
Abstract
Matricaria recutita L. has several uses in medicine, food and cosmetics. Its flower has high contents of flavonoids, mainly apigenine, whose pharmacological action and quality of its water–alcohol extract vary depending on its concentration. To optimize the process of flavonoid extraction and obtain higher yield, the Taguchi method was used. The factors analyzed were time–temperature (1–4 h at 70±0.5 °C), proportion of methanol: water (50:50 to 80:20) as solvent, and flower particle size (< 0.42 and >2.00 mm). To quantify flavonoids the aluminum chloride colorimetric method was used. The optimum combination of levels that maximizes (p<0.05) flavonoid yield is the process conducted with large flower particles (>2.00 mm) at 70±0.5 °C for 1 h in a solvent with 80:20 methanol:water.
Key words: Matricaria recutita L., aluminum chloride, ligulate flowers, methanol:water, Taguchi model.
INTRODUCCIÓN
La manzanilla (Matricaria recutita L.), una planta herbácea de la familia Asteraceae, se cultiva principalmente en Argentina, Egipto, Bulgaria, Hungría, España, República Checa, Alemania e Italia (Meireles, 2001; Tavares y Fonseca, 2004, Franke y Schilcher, 2005). Hay dos derivados principales de la flor de manzanilla: el aceite esencial y el extracto hidroalcohólico, que tienen usos medicinales, alimenticios y cosméticos. El extracto hidro–alcohólico se usa como antiinflamatorio y antipirético, musculotrópico espasmolítico, ansiolítico, vulnerario, desodorante, antibacteriano y estimulante del metabolismo de la piel (Svehlíková y Repcák, 2000; Franke y Schilcher, 2005; Svehlíková y Repcák, 2006). El contenido de flavonoides en el extracto hidroalcohólico de flor de manzanilla es el factor de calidad, y la apigenina es un constituyente mayoritario de este extracto; además en las preparaciones comerciales de flor de manzanilla se encuentra un espectro heterogéneo de contenido de este tipo de flavonoide (Franke y Schilcher, 2005). Considerando lo anterior, es necesario buscar métodos analíticos simples, rápidos y sensibles para cuantificar los flavonoides en la flor de manzanilla que validen su calidad.
Se han usado diferentes técnicas para extraer flavonoides presentes en flor de manzanilla (Cuadro 1) y su éxito depende de: parte utilizada de la planta, proporciones de disolventes, tiempo y temperatura. Por ejemplo, si el tiempo de extracción es 1 h los disolventes más usados son alcohol mezclado con agua (Cuadro 1). No se encontraron reportes del tiempo–temperatura de extracción, la cantidad de disolvente o la parte usada de la flor, lo cual es necesario para obtener un proceso reproducible. La eficiencia del proceso de extracción depende del tiempo, la temperatura, la proporción de disolventes y el tamaño de partícula (Grosso et al., 2005).
La combinación de factores que permite la máxima eficiencia de extracción puede determinarse con técnicas de optimización. El análisis del arreglo ortogonal de Taguchi se usa para optimizar los procesos con el mínimo número de experimentos. Su ventaja principal es que se pueden clasificar los factores de un experimento en controlables e incontrolables, y se pueden usar numerosos factores (Küçük y Kocakerim, 2005).
Por tanto, el objetivo de la presente investigación fue determinar las variables óptimas de la extracción hidro–alcohólica de flavonoides de la flor de manzanilla (Matricaria recutita L.). La hipótesis fue que la relación óptima de los factores de extracción permitirá la mejor extracción de flavonoides y un mejor rendimiento de ellos.
MATERIALES Y MÉTODOS
Este trabajo se realizó en el Colegio de Postgraduados, Montecillo, Estado de México. La flor de manzanilla (Matricaria recutita L.) proporcionada por los productores de la región de Joyacan, Cuijingo, Estado de México, México, se cosechó en diciembre de 2005. La cosecha se hizo cuando la flor estaba en plena apertura, es decir, cuando las flores liguladas estaban en posición horizontal y de 50 a 75% de flores tubulares abiertas. La flor se deshidrató a temperatura ambiente por 17 d, se descabezó y, mediante los tamices de malla 10 (2 mm) y 40 (0.42 mm), se separaron las partículas de acuerdo a su tamaño en: a) partícula grande (>2.00 mm) con 20.5% flores liguladas, 7.7% flores amarillas y 71.8% de tallo; b) partícula mediana (2.00 a 0.42 mm) con 19.3% flores liguladas, 62% flores tubulares y 19.3% de tallo; c) partícula pequeña (<0.42 mm) con 10.2% flores liguladas, 53.3% flores tubulares y 36.5% de tallo. El material se empacó en bolsas individuales de plástico con doble cierre hermético resellable y se mantuvo a 20±2 °C en un cuarto oscuro.
La extracción se hizo en tubos de ensaye con tapa de bakelita conteniendo 20 mL de disolvente y 1 g de flor de manzanilla; para tener la concentración deseada de disolvente se empleó agua desionizada. Para conocer el número de tratamientos requeridos se realizó la interacción de los factores y niveles (Cuadro 2). Los tratamientos a 70±0.5 °C se hicieron con incubación. El extracto se filtró y refrigeró para su estabilización por 3 d. Los flavonoides se cuantificaron con el método colorimétrico de cloruro de aluminio (Chang et al., 2002). Para obtener la curva tipo en la cuantificación de flavonoides, expresados como quercetina, se prepararon soluciones en concentraciones de 0 a 100 µg mL–1 y la ecuación generada fue:
A = –0.00869 + 0.007017C,
donde, A = la absorbancia a 415 nm; C = la concentración de la solución usada para el análisis colorimétrico (µg mL–1).
Los tratamientos se describen en el Cuadro 2. Para el análisis estadístico se consideraron factores controlables: proporción del disolvente, tiempo–temperatura y tamaño de partícula. Los niveles para proporción de disolvente se determinaron con base en lo reportado en la literatura (Cuadro 1) y se complementó con pruebas preliminares. El tiempo de extracción se seleccionó con base en lo reportado por Naczk y Shahidi (2004), donde los períodos varían de 1 min a 24 h y con respecto a los datos descritos en literatura (Cuadro 1); para la temperatura se incluyó un tratamiento a temperatura ambiente; respecto al tamaño de partícula para la flor de manzanilla, no se encontraron datos en la literatura revisada (Cuadro 2).
Se usó un diseño experimental con un arreglo factorial 6 x 4 x 3 y cuatro repeticiones. El modelo estadístico fue:
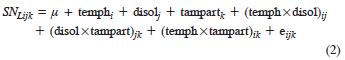
donde:

y = mg quercetina g –1 materia seca; nr = número de repeticiones del tratamiento.
Taguchi (1991) define la Ecuación 3 cuando se desea optimizar el proceso, maximizando la variable de respuesta. A esta transformación la denomina mayor es mejor (larger–the–better), que maximiza la señal sobre el ruido. SNLijk significa el efecto que tiene el i–ésimo nivel de tiempo–temperatura, del j–ésimo nivel de disolvente, del k–ésimo nivel de tamaño de partícula sobre mg de quercetina g –1 materia seca (y), transformado (Ecuación 3) µ = media general; temhi = tiempo–temperatura al i–ésimo nivel; i = 1,..., 6; disolj = proporción disolvente al j–ésimo nivel; i = 1,..., 4; tampartk= tamaño de partícula al k–ésimo nivel; i = 1,..., 3; eijk = error del i–ésimo nivel de tiempo–temperatura, del j–ésimo nivel de proporción del disolvente, del k–ésimo nivel de tamaño de partícula.
Conviene destacar que cuando el objetivo del proceso es alcanzar el valor máximo como en este caso, los valores máximos obtenidos por SNL son los óptimos (Küçük y Kocakerim, 2005).
En la Ecuación 4 se muestra el modelo general de producción para los factores significativos (Roy, 1990):

donde, 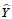 óptimo = resultado calculado a condiciones óptimas; Fnm = factor n a nivel m; y = promedio de las corridas.
óptimo = resultado calculado a condiciones óptimas; Fnm = factor n a nivel m; y = promedio de las corridas.
El intervalo de confianza (I.C.) para la predicción del valor óptimo (Ecuación 4) fue:

donde, F(n1 , n2) = valor de F para los grados de libertad (g.l.) n1 y n2 a los niveles de significancia α (α = 95%); el nivel de confianza es (1–α); n1 = grados de libertad (g.l.) de la media (el cual siempre es igual a 1); n2 = g.l. del error; Ve = varianza del error; Ne = número de réplicas equivalentes y está dado por:

RESULTADOS Y DISCUSIÓN
Con la curva de calibración (Ecuación 1) se calculó la concentración de flavonoides de los extractos preparados en el experimento. El diagrama de Box y Whiskers para el contenido de flavonoides se muestra en la Figura 1, donde se aprecia que los extractos están entre 1.42 a 10.89 mg g –1 y se forman dos grupos: los rendimientos altos se obtienen con los tratamientos realizados a 70±0.5 °C y los bajos con los efectuados a la temperatura ambiente (20±2 °C).
Para encontrar los niveles óptimos de cada factor (tiempo–temperatura, proporción del disolvente y tamaño de partícula), primero se obtuvo el promedio de cada corrida. El promedio de cada corrida se sustituyó en la Ecuación 3 para obtener los valores SNL. Con los resultados originales (y) y SNL (Cuadro 3), se realizaron dos análisis de varianza (A de V) (Cuadros 4 y 5), usando SAS versión 8.0. Los tres factores principales y todas las interacciones resultaron significativas respecto a y (Cuadro 4). Para la variable SNL los factores principales y la interacción tiempo–temperatura X proporción de disolvente, sólo resultaron significativos (Cuadro 5). Además, la transformación "mayor es mejor" identifica las señales significativas a pesar del ruido existente en cada corrida, lo que no ocurre con la variable de respuesta sin transformar.
El modelo estadístico usado para identificar los factores así como sus interacciones significativas fue:
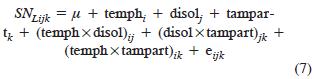
En la Figura 2 se muestra el comportamiento de las medias SNL de los niveles de cada factor y sus interacciones. Se observa que existen diferencias significativas en los seis tratamientos, formándose dos grupos en tiempo–temperatura. No hubo diferencias significativas en tres niveles de proporción del disolvente (75:25, 80:20 y 70:30), ni en tamaño de partícula en dos niveles (mediano y grande) (Figura 2).
En la Figura 3 se muestran las interacciones dobles de cada factor. Hay interacción significativa (p<0.05) entre los factores principales tiempo–temperatura x proporción de disolvente (A de V, Cuadro 5). La interacción indica que tiempo–temperatura (temh) depende de la proporción del disolvente (disol).
Para encontrar el óptimo, y a pesar de que en algunos casos los niveles de algunos factores no resultaron estadísticamente diferentes, se consideraron los máximos de estos valores (Cuadro 6). Así, el valor óptimo en términos de los valores originales (Cuadro 6), se calculó como:



usando la Ecuación (4),
donde el intervalo al 95% de confianza es:

usando la Ecuación (5)
F(n1, n2)=F0.05 n1 = 1 n2=g.l. del error 246, 3.8415
Ve = cuadrado medio del error, 0.33
Ne = 72/26 (25 g.l. + 1),
calculados en función del A de V de los datos originales (Cuadro 4).
Se consideraron los factores e interacciones significativos del A de V de SNL (Cuadro 5) para la estimación de 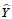 óptimo, ya que SNL maximiza la señal y minimiza el ruido.
óptimo, ya que SNL maximiza la señal y minimiza el ruido.
Una vez definidas las condiciones óptimas del proceso (Cuadro 6) y establecido el intervalo de confianza, se continuó con la prueba de confirmación con los mismos parámetros óptimos y el resultado fue 9.76 mg quercetina g –1 muestra en base seca (b.s.) (I.C. ±0.68), el cual es superior al 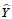 óptimo estimado con valor de 10.34 mg quercetina g –1 muestra b.s. La media general en rendimiento fue 6.48 mg quercetina g –1 muestra b.s., siendo 59.56% menor con respecto al proceso óptimo esperado y confirmando la eficiencia del proceso. El proceso con la combinación óptima obtuvo un rendimiento de 8.69 mg quercetina g –1 muestra b.s., un resultado que se encuentra dentro de los valores reportados (Cuadro 1).
óptimo estimado con valor de 10.34 mg quercetina g –1 muestra b.s. La media general en rendimiento fue 6.48 mg quercetina g –1 muestra b.s., siendo 59.56% menor con respecto al proceso óptimo esperado y confirmando la eficiencia del proceso. El proceso con la combinación óptima obtuvo un rendimiento de 8.69 mg quercetina g –1 muestra b.s., un resultado que se encuentra dentro de los valores reportados (Cuadro 1).
Las diferencias observadas entre el valor estimado y el promedio de las tres corridas de confirmación se deben a factores como variedades empleadas (Redaelli et al., 1981), condiciones de desarrollo del cultivo (Tavares y Fonseca, 2004), manejo poscosecha (Franke y Schilcher, 2005) y proceso de extracción (Cuadro 1).
Naczk y Shahidi (2004) reportan que los largos periodos de extracción que varían de 1 min a 24 h, incrementan la oportunidad de oxidación de los fenoles. Respecto a la proporción del disolvente metanol:agua, 50:50 fue la menos eficiente.
El contenido de flavonoides fue alto en la partícula grande, lo cual contradice el hecho de que un menor tamaño de partícula ofrece una mayor área de transferencia y por ende una mayor extracción. La explicación a esta discrepancia radica en que la partícula grande contiene flores liguladas que contienen 7–9% de apigenina–7–glucósido, el flavonoide más abundante en la flor de manzanilla (Franke y Schilcher, 2005; Švehlíková y Repcák, 2000; Maier et al., 1993).
CONCLUSIONES
Las condiciones óptimas de extracción de flavonoides a partir de manzanilla son tratamiento de 1 h a 70±0.5 °C, proporción de disolventes de 80:20 (metanol:agua), empleando un tamaño de partícula grande (>2.00 mm, donde existen flores liguladas).
Los valores predichos y los de confirmación están dentro del intervalo de confianza; entonces el modelo es adecuado para obtener un mayor rendimiento en la extracción de flavonoides.
Las condiciones óptimas identificadas con la metodología de Taguchi fueron reproducidas en el laboratorio. Este proceso de laboratorio es muy útil y puede reproducirse a escala industrial.
LITERATURA CITADA
Chang, C. C., M. H. Yang, H. M. Wen, and J. C. Chern. 2002. Estimation of total flavonoid content in propolis by two complementary colorimetric methods. J. Food Drug Anal. 10: 178–182. [ Links ]
Franke, R., and H. Schilcher. 2005. Chamomile. Industrial Profiles. Medical and Aromatic Plants–Industrial Profiles. Taylor & Francis, Florida. 289 p. [ Links ]
Grosso, N. R., V. Nepote, and C. A. Guzmán. 2005. Optmization of extraction of phenolic antioxidants from peanut skin. J. Sci Food Agric. 85: 33–38. [ Links ]
Küçük, Ö., and M. M. Kocakerim. 2005. Optimization of dissolution of ulexite in water saturated with sulphur dioxide. Chem. Eng. Proces. 44: 1005–1011. [ Links ]
Maier, R., C. Reinhold, K. Wolfgang, and R. Ernst. 1993. Purification and characterization of flavone 7–O–glucoside– specific glucosidase from ligulate florets of Chamomilla recutita. Planta Med. 59: 436–441. [ Links ]
Meireles M. A. de A. 2001. Supercritical extraction of essential oils, pigments and nutraceuticals from herbs, spices and medicinal plants. IV Encontro Brasileiro sobre Fluidos Supercríticos. Vol. 1 Salvador, BA, Brasil. pp: 25–26. [ Links ]
Miliauskas, G., P. R. Venskutonis, and T. A. Van Beek. 2004. Screening of radical scavenging activity of some medicinal and aromatic plant extracts. Food Chem. 85: 231–237. [ Links ]
Naczk, M., and F. Shahidi. 2004. Extraction and analysis of phenolics in food. J. Chromatog. A. 1054: 95–111. [ Links ]
Redaelli, C., L. Formentini, and E. Santaniello. 1981. Reversed– phase high–performance liquid chromatography analysis of apigenin and its glucosides in flowers of Matricaria chamomilla and chamomile extracts. Planta Medica. J. Medical Plant Res. 42: 288–292. [ Links ]
Roy R. 1990. A Primer on the Taguchi Method. Van Nostrand Reinhold (VNR), New York. pp: 116–139. [ Links ]
Švehlíková, V., and M. Repcák. 2000. Variation of apigenin quantity in diploid and tetraploid Chamomilla recutita (L.) Rauschert. Plant Biol. 2: 403–407. [ Links ]
Švehlíková, V., and M. Repcák. 2006. Apigenin chemotypes of Matricaria chamomilla L. Biochem. Syst. Ecol. 34: 654–657. [ Links ]
Taguchi, G. 1991. System of Experimental Design. Engineering Methods to Optimize Quality and Minimize Costs. Quality Resources and American Supplier Institute, New York. 1189 p. [ Links ]
Tavares, M. F. M., and F. N. Fonseca. 2004. Validation of a capillary electrophoresis method for the quantitative determination of free and total apigenin in extracts of Chamomilla recutita. Phytochem. Anal. 15:65–70. [ Links ]
WHO (World Health Organization). 1999. Monographs on Selected Medicinal Plants. Volume 1. Flos Chamomillae. World Health Organization. Geneva. pp: 86–94. [ Links ]














