Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Agrociencia
versión On-line ISSN 2521-9766versión impresa ISSN 1405-3195
Agrociencia vol.49 no.3 Texcoco abr./may. 2015
Ciencia de los alimentos
Análisis de ácidos fenólicos y actividad antioxidante de extractos acuosos de variedades de jamaica (Hibiscus sabdariffa L.) con cálices de colores diversos
Analysis of phenolic acids and antioxidant activity of aqueous extracts of jamaica (Hibiscus sabdariffa L.) varieties with calyxes of different colors
Alberto Reyes-Luengas1, Yolanda Salinas-Moreno2*, Manuel E. Ovando-Cruz3, Ramón I. Arteaga-Garibay4, Marcos D. Martínez-Peña4
1 Departamento de Ingeniería Agroindustrial. Universidad Autónoma Chapingo. 56200. Km 13.5 Carretera Los Reyes-Texcoco. Chapingo, México.
2 Laboratorio de Calidad de Cultivos para uso Humano y Pecuario. Campo Experimental Centro Altos de Jalisco. Instituto Nacional de Investigaciones Forestales Agrícolas y Pecuarias (INIFAP). 47600. Km 8, Carretera Tepatitlán-Lagos de Moreno. Tepatitlán de Morelos, Jalisco. *Autor responsable. (yolasm@gmail.com).
3 Campo Experimental Valles Centrales. INIFAP. Melchor Ocampo No. 7, Colonia Agencia Municipal, Santo Domingo Barrio Bajo 7, Etla, Oaxaca.
4 Laboratorio de Recursos Genéticos Microbianos. Centro Nacional de Recursos Genéticos. INIFAP. 47600. Boulevard de la biodiversidad No 400 Tepatitlán de Morelos, Jalisco.
Recibido: mayo, 2014.
Aprobado: marzo, 2015.
Resumen
El creciente mercado de bebidas funcionales requiere la caracterización específica de las fuentes de bioactivos, para seleccionar aquellas con la mayor cantidad del compuesto necesario en la formulación. La composición de ácidos fenólicos y contenido de antocianinas y proantocianidinas, de extractos acuosos de tres variedades de jamaica (Hibiscus sabdariffa L.), con rojo oscuro (Sudán), rojo claro (Criolla Nayarit) y blanco (Alma Blanca) en sus cálices, fueron evaluados mediante HPLC-DAD. Además, se determinó su actividad antioxidante. El diseño experimental fue completamente al azar y con tres repeticiones. El contenido mayor de ácidos fenólicos totales se detectó en Sudán y Alma Blanca (10.71±0.29 y 8.22±0.30 mg EAG g-1 MS). La fracción de ácidos fenólicos libres (AFL) fue abundante y con complejidad alta en los cálices de los tres colores. El ácido clorogénico y sus dos isómeros predominaron en las fracciones AFL y los ácidos fenólicos glucosilados (AFG) representaron entre 77.4 y 81.5 % del total de ácidos fenólicos en las tres variedades. Los cálices blancos tenían la cantidad mayor de ácido cafeico y derivados de protocatéquico. La actividad antioxidante mayor (p≤0.05) se presentó en el extracto de Sudán (IC50=113.3 μg mL-1). El color de los cálices puede ser un indicador del tipo predominante de fenoles en H. sabdariffa L. y ayudar en la selección de variedades para obtener formulaciones con propiedades nutracéuticas particulares.
Palabras clave: Hibiscus sabdariffa L., fenoles, antocianinas, cálices, color, actividad antioxidante.
Abstract
The growing market of functional beverages requires characterize specifically the sources of bio-actives to select those with the highest quantity of the compound needed in the formulation. The composition of phenolic acids and the content of anthocyanins and proanthocyanidins, from aqueous extracts of the calyxes of three varieties of jamaica (Hibiscus sabdariffa L.) were assessed using HPLC-DAD: dark red (Sudan), light red (Criolla Nayarit) and white (Alma Blanca). Antioxidant activity was also determined. The experimental design was completely randomized with three replications. The highest contents of total phenolic acids were detected in Sudan and Alma Blanca (10.71±0.29 and 8.22±0.30 mg GAE g-1 DM). The fraction of free phenolic acids (FPA) was abundant and was highly complex in the calyxes of the three colors. Chlorogenic acid and its two isomers were predominant in the FPA, and the glycosylated phenolic acids (GPA) accounted for 77.4 to 81.5 % of the total phenolic acids in the three varieties. The white Alma Blanca calyxes contained more caffeic and protocatechuic acid derivatives than the red calyxes of the other varieties. The highest antioxidant activity (p≤0.05) was found in the Sudan extract (CI50=113.3 μg mL-1). The color of the calyxes can indicate the predominant type of phenols in H. sabdariffa L. and aid in the selection of varieties for formulations with particular nutraceutical properties.
Key words: Hibiscus sabdariffa L., phenols, calyx, color, antioxidant activity.
Introducción
La jamaica (Hibiscus sabdariffa L.), o flor de jamaica como se le conoce en México, es una planta anual cultivada en los climas tropicales y subtropicales del mundo. Sus cálices se aprovechan para elaborar bebidas frías o calientes, mermeladas, salsas, y aderezos. En la medicina tradicional, los extractos acuosos de la decocción de los cálices deshidratados de jamaica se utilizan para el control de la presión arterial, alteraciones hepáticas o fiebre (Ali et al., 2005). Estos beneficios terapéuticos se atribuyen a la diversidad de los fitoquímicos de los cálices (Rodríguez-Medina et al., 2009; Ramirez-Rodriguez et al., 2011; Hopkins et al., 2013), en los que predominan los fenoles. Entre los fenoles más abundantes están las antocianinas (Tsai et al., 2002), que son responsables del color rojo brillante de los extractos de los cálices y son estudiadas ampliamente (Galicia-Flores et al., 2008; Ramírez-Rodríguez et al., 2011).
Los ácidos fenólicos son otro grupo importante de compuestos en los cálices de la jamaica y se encuentran en forma libre o conjugada. En frutas y hortalizas están principalmente en forma libre (Shahidi y Naczk, 2004), y en los cereales predominan en forma conjugada o ligada (Liu, 2007).
En extractos acuosos de jamaica se identificó el ácido clorogénico y sus isómeros I y II como los ácidos fenólicos principales (Fernández-Arroyo et al., 2011; Ramirez-Rodriguez et al., 2011), junto con los derivados de los ácidos protocatéquico y gálico (Ramirez-Rodriguez et al., 2011) y el ácido cafeico (Huang et al., 2009). Otros fenoles del tipo flavonoide, como quercetina y sus glucósidos, y los glucósidos de miricetina (Fernández-Arroyo et al. 2011; Ramirez-Rodriguez et al. 2011) y proantocianidinas (Sáyago-Ayerdi et al., 2007), del tipo catequina, epigalocatequina y epigalocatequin-galato (Huang et al., 2009) también están identificados en la flor de jamaica.
El color de los cálices de jamaica está asociado al contenido y tipo de fenoles. Los cálices oscuros tienen más antocianinas que los cálices claros, pero los blancos o verdes carecen de estos flavonoides (Christian y Jackson, 2009) o están en cantidades mínimas (Salinas-Moreno et al., 2012). La caracterización de los ácidos fenólicos de extractos acuosos de jamaica es limitada (Rodríquez-Medina et al., 2009; Ramírez-Rodríguez et al., 2011) y se ha realizado en variedades con cálices coloridos, por lo que se desconoce la composición de los blancos.
La actividad antioxidante asociada a las bebidas elaboradas a partir de la decocción acuosa de los cálices de jamaica (Prenesti et al., 2007) se atribuye a los fenoles que contienen, y destacan las antocianinas (Sáyago-Ayerdi et al., 2007) y los ácidos fenólicos. De estos últimos, el ácido clorogénico y sus derivados son los más importantes (Fernández-Arroyo et al., 2011).
El mercado creciente de las bebidas funcionales requiere caracterizar los fenoles de cada variante, para elegir la más adecuada para el diseño de bebidas con características nutraceúticas particulares.
Por lo tanto, los objetivos del presente estudio fueron: 1) analizar los ácidos fenólicos solubles (libres y conjugados) en los extractos acuosos de variedades de jamaica con color diferente de cálices mediante HPLC-DAD; 2) cuantificar flavonoides del tipo antocianinas y proantocianidinas; y, 3) determinar la actividad antioxidante de los extractos.
Materiales y Métodos
Material biológico
Las variedades de jamaica Sudán, con cálices rojo oscuro, Criolla Nayarit con cálices rojo claro y Alma Blanca con cálices blancos fueron estudiadas. Sudán y Alma Blanca fueron cultivadas en Santa María Cortijo, Jamiltepec, estado de Oaxaca; la Criolla Nayarit, fue cultivada en Huajicori, estado de Nayarit.
Preparación de los extractos acuosos
Los extractos se prepararon con 2.5 g de cálices secos y 100 mL de agua destilada. La mezcla hirvió 15 min, se separó el líquido de los cálices por decantación y la extracción se repitió en las mismas condiciones. Los extractos se juntaron, la solución se filtró con papel Whatman No. 4 y se aforó a 200 mL con agua destilada. Las siguientes variables se evaluaron en este extracto.
Ácidos fenólicos
Los ácidos fenólicos libres, glucosilados y esterificados se determinaron con el método de Bakan et al. (2003). Para determinar los ácidos fenólicos libres se realizaron dos extracciones líquido-líquido con 15 mL de acetato de etilo a 20 mL del extracto acuoso, después de ajustar su pH a 2, con HCl 2N. Las dos fases orgánicas se juntaron y concentraron a sequedad en un rota-evaporador (Heidolph instruments, mod. Laborata 4010 digital, Germany). El residuo se resuspendió en 2 mL de metanol grado HPLC. Las muestras se mantuvieron en frascos ámbar a -20 °C hasta su análisis. La fase acuosa restante se aforó a 20 mL con agua destilada y se dividió en dos volúmenes iguales.
Para la fracción de ácidos fenólicos glucosilados (AFG), a uno de los volúmenes se adicionaron 10 mL de HCl 2N y se colocó 1 h a 4 °C; el otro volumen se empleó para la fracción de ácidos fenólicos esterificados (AFE), al cual se añadieron 10 mL de NaOH 2N, se dejó reaccionar 3 h en oscuridad. Después se ajustó a 2 el pH de los extractos y se procesaron en la misma forma que los ácidos fenólicos libres. Los ácidos fenólicos totales en cada fracción se cuantificaron mediante la prueba Folin Ciocalteu (Singleton y Rossi, 1965). A 100 μL del extracto acuoso se adicionaron 125 μL de reactivo de Folin-Ciocalteu 1N, se agitó y se dejó reaccionar 6 min en oscuridad. La reacción se neutralizó con 1250 μL de Na2CO3 al 19 % y se aforó a 3 mL con agua destilada. La muestra se agitó y quedó en oscuridad 90 min. La absorbancia se midió en un espectrofotómetro (PerkinElmer, Lamda 25 UV/Vis, USA) a 760 nm. Una curva estándar de ácido gálico (20 a 100 μg L-1) fue realizada, y los resultados se expresaron en mg equivalentes de ácido gálico por g de MS (mg EAG g-1 MS).
Análisis de ácidos fenólicos por cromatografía líquida de alta resolución acoplada a detector con arreglo de diodos (HPLC-DAD)
Los ácidos fenólicos se analizaron con un equipo PerkinElmer serie 200 (USA), integrado por bomba cuaternaria, degasificador, detector de UV/Vis con arreglo de diodos (DAD), con auto-muestreador y columna analítica Hypersil ODS.2 (250×46 mm), con tamaño de partícula de 5 μm. El método de Glowniak et al. (1996) fue usado, y como fase móvil se empleó una mezcla de metanol: ácido acético: agua (25:1:75 v/v/v). La velocidad de flujo fue 1 mL min-1, el tiempo de corrida 22 min y el volumen de inyección 10 mL. La detección se realizó a 254 nm (derivados de p-hidroxibenzoico) y 320 nm (derivados de hidroxicinámico). La temperatura de la columna se mantuvo en 30 °C.
El detector con arreglo de diodos se usó para obtener el espectro de UV de cada pico del cromatograma de ácidos fenólicos. La identificación se realizó por comparación de los tiempos de retención con los estándares comerciales y sus respectivos espectros en UV. Para identificar cuál de los picos en el cromatograma correspondía al ácido clorogénico, se agregó a la muestra una pizca del estándar comercial. Una vez ubicado el pico correspondiente al ácido clorogénico, se usó la literatura y una librería de espectros de UV de los diferentes ácidos fenólicos reportados en Hibiscus sabdariffa L., y se identificaron los derivados de ácidos. Para la cuantificación se prepararon curvas patrón de los ácidos caféico, clorogénico, ferúlico, gálico, protocatéquico, p-cumárico, p-hidroxibenzoico y siríngico (Sigma, MN) en las mismas condiciones que las muestras.
Fenoles extractables totales y antocianinas totales
Para cuantificar los fenoles extractables totales (FET) se usó el método de Folin-Ciocalteu (Singleton y Rossi, 1965). Las antocianinas totales se determinaron al medir la absorbancia de los extractos acuosos en un espectrofotómetro (Perkin Elmer Lambda 25 UV/Vis, USA) de acuerdo con lo descrito por Abdel-Aal y Hucl (1999), y las adaptaciones de Salinas-Moreno et al. (2005). Una curva patrón de cianidina 3-glucósido (Polyphenols, Nw) fue realizada y los resultados se expresaron en mg equivalentes de cianidina-3-glucósido por g de MS (mg C3GE g-1 MS).
Proantocianidinas
Las proantocianidinas se evaluaron con el método de Wallace y Giusti (2010). Una alícuota de 20 μL de la muestra se hizo reaccionar con 2380 μL de metanol y 100 μL de solución de DMAC (4-dimetilamino cinamaldehido al 2 % en una mezcla 1:1 (v/v) de metanol y ácido sulfúrico 6 N). La reacción duró 25 min a temperatura ambiente, en oscuridad, y se leyó la absorbancia a 640 nm; la concentración fue calculada con una curva patrón de catequina (Sigma, MN). Los resultados se expresaron en μg equivalentes de catequina por mg de MS (μg EC mg-1 de MS).
Actividad antioxidante
Para evaluar la actividad antioxidante se usó el método del radical libre 2,2-difenil-1-picrilhidrazil (DPPH) (Sigma Aldrich Co®) descrito por Soler-Rivas et al. (2000) con una solución 100 μM de DPPH en metanol al 80 %. En una cubeta de cuarzo se colocaron 100 mL de extracto y 2.9 mL de DPPH. La absorbancia se monitoreó cada 5 min por 30 min a una longitud de onda de 515 nm. La absorbancia de referencia (A0) fue obtenida al sustituir el volumen de extracto por metanol al 80 %.
El porcentaje de reducción de DPPH se obtuvo de la expresión: DPPH (%)=(A0-An)100 / A0, donde A0 y An fueron las absorbancias de referencia y de la muestra, respectivamente. Los datos se usaron para determinar el parámetro IC50, que representa la concentración (μg mL-1) de compuestos fenólicos requerida para reducir 50 % del radical libre DPPH (Einbond et al., 2004).
Diseño experimental y análisis estadísticos
El diseño experimental fue completamente al azar. Con los datos de composición fenólica se realizó un ANDEVA y pruebas de comparación de medias (Tukey; p≤0.05). Todas las determinaciones se realizaron por triplicado. Los análisis se efectuaron con SAS System versión 9.0.
Resultados y Discusión
Ácidos fenólicos
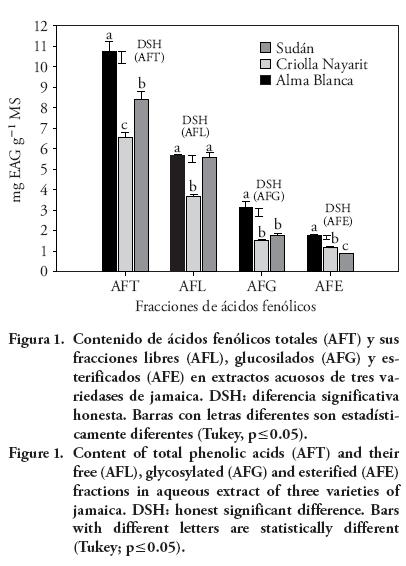
El contenido de ácidos fenólicos totales (AFT) fue diferente entre las variedades analizadas. Sudán tuvo el contenido mayor (p≤0.05) y Criolla Nayarit el menor (10.71±0.29 y 6.57±0.24 mg EAG g-1 MS). Los cálices blancos de Alma Blanca tuvieron contenido mayor (p≤0.05) de AFT que los de Criolla Nayarit, coloreados y con antocianinas (Figura 1). La fracción más abundante de ácidos fenólicos en las variedades analizadas fue la de los ácidos fenólicos libres (AFL). Un patrón similar fue reportado para frutas y verduras (Shahidi y Naczk, 2004). Los AFL en las variedades Sudán y Alma Blanca fueron similares (p>0.05), pero mayores que en Criolla Nayarit. El contenido mayor (p≤0.05) de ácidos fenólicos glucosilados (AFG) correspondió a Sudán y el menor lo tuvieron Criolla Nayarit y Alma Blanca. La fracción AFE fue la menor de las tres, con el contenido mayor (p≤0.05) en Sudán y el menor en Alma Blanca.
La fracción AFL mostró entre 12 y 13 picos de ácidos fenólicos o de sus derivados. La identidad de los derivados se obtuvo al comparar sus respectivos espectros en UV con los estándares comerciales y hubo coincidencia del espectro, pero no así del tiempo de retención (Figura 2).
En la fracción de AFL el ácido clorogénico y sus isómeros I (ácido 5-cafeoil quínico) y II (ácido 4-cafeoil quínico) fueron los más abundantes, los siguió el cafeico y los derivados del ácido protocatéquico (Cuadro 1). Alma Blanca destacó por sus contenidos elevados de ácido caféico y derivados de protocatéquico. Los contenidos de ácido clorogénico y sus isómeros fueron menores que 1924, 2755 y 1041 μg g-1 de clorogénico, isómero I e isómero II en extractos acuosos de cálices molidos de jamaica reportados por Fernández-Arroyo et al. (2011).
Las variedades de cálices coloridos tuvieron derivados de ácido gálico, ausentes en Alma Blanca, en cantidades más altas que los derivados del protocatéquico. También hubo derivados de los ácidos p-cumárico y ferúlico en cantidades pequeñas. El contenido de ácidos fenólicos totales fue parecido en Alma Blanca y Sudan y más alto que en Criolla Nayarit. Los valores obtenidos por HPLC fueron similares a los cuantificados con el método de Folin-Ciocalteau (Figura 1). Alma Blanca tuvo un contenido alto de derivados del ácido p-hidroxibenzoico, respecto a las variedades con cálices color rojo.
El ácido clorogénico y sus isómeros (I y II) también predominaron en la fracción de AFG, similar a la fracción de AFL en la proporción mayor del clorogénico sobre sus isómeros. Además el contenido de estos ácidos tuvo el orden Sudán>Alma Blanca>Criolla Nayarit. El ácido cafeico fue el segundo más importante en la fracción AFG y las variedades tuvieron el mismo orden por su contenido en los AFL. La variedad Sudán mantuvo la presencia de derivados del ácido siríngico en esta fracción, como en la de AFL; las otras variedades no tuvieron derivados de este ácido.
Los AFE representaron todos aquellos ácidos fenólicos no ligados a componentes de pared celular, pero poseen alguna molécula unida a su estructura mediante enlace éster (Liu, 2007). En las variedades analizadas destacó la cantidad de derivados de siríngico y p-hidroxibenzoico. Las variedades coloridas tuvieron cantidad alta de ácido cafeico, que podría provenir de la hidrólisis del ácido clorogénico, que es inestable al pH alcalino al que el extracto se somete para su análisis. La variedad Criolla Nayarit tuvo un contenido alto de derivados de protocatéquico, Sudán tuvo un valor varias veces menor y en Alma Blanca no se detectó en la fracción AFE. La variedad Sudan tuvo derivados de ácido siríngico en las tres fracciones de ácidos fenólicos analizadas.
En la fracción AFL de las variedades analizadas el ácido clorogénico representó 39.1, 43.9 y 37.1 % del total en Alma Blanca, Sudán y Criolla Nayarit. Al considerar los isómeros, la proporción creció hasta 77.4, 81.5 y 81.2 % en ellas. En Alma Blanca el ácido cafeico fue el cuarto en importancia (10.3 %), pero en las variedades coloridas los derivados del ácido gálico ocuparon esa posición. La predominancia del ácido clorogénico y sus isómeros en los extractos acuosos analizados coincidió con lo informado por Rodríguez-Medina et al. (2009) y Ramírez-Rodríguez et al. (2011), quienes obtuvieron el mismo resultado con técnicas de HPLC-MS. Pero este resultado contrastó con lo observado por Huang et al. (2009), ya que identificaron una fracción de Hibiscus spp rica en polifenoles, con ácidos protocatéquico (24.2 %) y cafeico (19.9 %) como los más abundantes. Las divergencias podrían deberse al disolvente usado para obtener los extractos, pues el etanol, en contraste con el agua, favorece la extracción del protocatéquico (Chao y Yin, 2009). Además, la genética de los materiales usados en cada caso puede ser diferente.
Entre los ácidos fenólicos en los cálices de jamaica, el protocatéquico es el más estudiado por sus efectos como antioxidante que puede proteger de la oxidación a las células hepáticas de ratas (Tseng et al., 1996), e inducir apoptosis en células afectadas por leucemia en humanos (Tseng et al., 2000). Además, el ácido clorogénico se ha relacionado con una reducción significativa de las presiones sistólica y diastólica (Watanabe et al., 2006).
Fenoles extractables totales, antocianinas y proantocianidinas en los cálices de jamaica
Los FET de una matriz vegetal o alimento son todos aquellos factibles de solubilizarse y ser extraídos con el disolvente usado (Saura-Calixto et al., 2007). En el estudio presente el contenido de FET fue estadísticamente diferente (p≤0.05) entre las variedades analizadas. El contenido mayor correspondió a Sudán y el menor a Alma Blanca (Cuadro 2). El contenido de FET en los tres genotipos fue similar al reportado en variedades con colores de cálices semejantes (Christian y Jackson, 2009).
El contenido de antocianinas totales fue mayor en Sudán y menor en Alma Blanca (p≤0.05). Las variedades con color diferente al blanco presentaron valores similares (3 a 25 mg EC3G g-1 MS) a los obtenidos por Juliani et al. (2009) en variedades cultivadas en Senegal. En Alma Blanca el contenido fue mayor que lo informado por Christian y Jackson, (2009). En las variedades con cálices rojos, la intensidad del color está relacionada con su contenido de antocianinas (Christian y Jackson, 2009; Salinas et al., 2012). La variedad Sudán, con cálices oscuros, presentó 2.4 veces más antocianinas que Criolla Nayarit, con cálices claros. Las antocianinas en los FET en las variedades con cálices rojos representaron 30 %, y en la de cálices blancos 2 %. Según Sáyago-Ayerdi et al. (2007), cerca de 30 y 60 % de los FET en jamaica de cálices rojos, son antocianinas y ácidos fenólicos.
Las proantocianidinas (PAs) fueron los fenoles menos abundantes en los extractos analizados. El mayor contenido se observó en la variedad Sudán (p≤0.05) y el menor en Alma Blanca. Su presencia en cálices de jamaica fue reportada por Obouayeba et al. (2014) al monitorear los fitoquímicos en extractos acuosos de jamaica. El método analítico utilizado (DMAC) detecta con mayor precisión monómeros de flavan-3-ols, y reacciona sólo con unidades terminales, sin discriminar monómeros, dímeros o trímeros (Hummer y Schreier, 2008). Así, las PAs en las jamaicas analizadas pueden ser de tipo flavanoles, porque Huang et al. (2009) reportaron presencia de catequina, epigalocatequina y epigalocatequin-galato en un extracto concentrado de jamaica. Las proantocianidinas se consideran fenoles con actividad antioxidante que ayudan en la prevención de problemas cardiovasculares, porque protegen el músculo cardíaco (Natella et al., 2002).
Actividad antioxidante
El IC50 es la concentración del extracto que reduce 50 % del radical libre. Los valores bajos de IC50 se asocian con el poder antioxidante mayor (Einbond et al., 2004). El patrón de la reducción del radical DPPH mostrado por Alma Blanca y Criolla Nayarit fue distinto al de Sudán (Figura 3).

La reducción por los extractos de Alma Blanca y Criolla Nayarit fue casi lineal, en tanto que la de Sudan fue exponencial. La variedad Sudán presentó IC50 menor que Alma Blanca y Criolla Nayarit, es decir, tiene poder antioxidante mayor, atribuido a su contenido alto de antocianinas, más que a sus ácidos fenólicos, que fueron similares a los de Alma Blanca. El IC50 de los extractos de Criolla Nayarit y Alma Blanca fue similar (p>0.05). La actividad antioxidante de Alma Blanca se atribuye a los ácidos fenólicos, pues prácticamente carece de antocianinas. La variabilidad entre métodos para medir la actividad antioxidante en extractos acuosos de jamaica y la forma de expresar los datos, dificulta la comparación de resultados. Según Pérez-Ramírez et al. (2015) el IC50 para una bebida de jamaica fue 13.6 mg de cálices secos mL-1 y los cálculos con la concentración de FET de la variedad Sudán dan un IC50 de 478.4 ug mL-1; por lo tanto, con poder antioxidante mayor. Los resultados mostraron el potencial antioxidante (ácidos fenólicos) de las variedades de Hibiscus spp. de cálices blancos similar al de las variedades con cálices de otro color.
Conclusiones
Independientemente de su color, los cálices son fuente abundante de ácidos fenólicos y otros flavonoides con actividad antioxidante. El color de los cálices puede ser un indicador del tipo predominante de fenoles y ayudar a la selección de las variedades para obtener formulaciones con propiedades nutracéuticas particulares.
Literatura Citada
Abdel-Aal, E.-S. M., and P. Hucl. 1999. A rapid method for quantifying total anthocyanins in blue aleurone and purple pericarp wheat. Cereal Chem. 76: 350-354. [ Links ]
Ali, B. H., N. A. Wabel, and G. Blunden. 2005. Phytochemical, pharmacological and toxicological aspects of Hibiscus sabdariffa L.: A review. Phytother. Res. 19: 369-375. [ Links ]
Bakan, B. A., C. Bily, D. Melcion, B. Cahagnier, B. C. Regnault-Roger, B. J. R. Philogene, and D. Richard-Molard. 2003. Possible role of plant phenolics in the production of trichothecenes by Fusarium graminearum strains on different fractions of maize kernels. J. Agric. Food Chem. 51: 2826-2831. [ Links ]
Chao, Y-C., and M.-C. Yin. 2009. Antibacterial effects of roselle calyx extracts and protocatechuic acid in ground beef and apple juice. Foodborne Pathog. Dis. 6: 201-206. [ Links ]
Christian, K. R., and J. C. Jackson. 2009. Changes in total phenolic and monomeric anthocyanin composition and antioxidant activity of three varieties of sorrel (Hibiscus sabdariffa) during maturity. J. Food Compos. Anal. 22: 663-667. [ Links ]
Einbond, S. L., A. K. Reynertson, L. Xiao-Dong, J. M. Basile, and J. E. Kennelly. 2004. Anthocyanin antioxidants from edible fruits. Food Chem. 84: 23-28. [ Links ]
Fernández-Arroyo, S., I. C. Rodríguez-Medina, R. Beltrán-Debón, F. Pasini, J. Joven, V. Micol, A. Segura-Carretero, and A. Fernández-Gutiérrez. 2011. Quantification of the polyphenolic fraction and in vitro antioxidant and in vivo anti-hyperlipemic activities of Hibiscus sabdariffa aqueous extract. Food Res. Inter. 44: 1490-1495. [ Links ]
Galicia-Flores, L. A., Y. Salinas-Moreno, B. M. Espinosa-García, y C. Sánchez-Feria. 2008. Caracterización fisicoquímica y actividad antioxidante de extractos de jamaica (Hibiscus sabdariffa L.) nacional e importada. Rev. Chapingo Serie Hortic. 14: 121-129. [ Links ]
Glowniak, K., G. Zgórka, and M. Kozyra. 1996. Solid phase extraction and reversed-phase high-performance liquid chromatography of free phenolic acids in some Echinacea species. J. Chromatogr. A 730: 25-29. [ Links ]
Hopkins, A. L., M. G. Lamm, J. L. Funk, and C. Ritenbaugh. 2013. Hibiscus sabdariffa L. in the treatment of hypertension and hyperlipidemia: A comprehensive review of animal and human studies. Fitoterapia 85: 84-94. [ Links ]
Huang, C. N., K. C. Chan, W. T. Lin, S. L. Su, C. J. Wang, and C. H. Peng. 2009. Hibiscus sabdariffa inhibits vascular smooth muscle cell proliferation and migration induced by high glucose - A mechanism involves connective tissue growth factor signals. J. Agric. Food Chem. 57: 3073-3079. [ Links ]
Hummer, W., and P. Schreier. 2008. Analysis of proanthocyanidins. Mol. Nutr. Food Res. 52: 1381-1398. [ Links ]
Juliani, H. R., C. R. Welch, Q. Wu, B. Diouf, D. Malainy, and J. E. Simon. 2009. Chemistry and quality of Hibiscus (Hibiscus sabdariffa L.) for developing the natural product industry in Senegal. J. Food Sci. 74: S113-S121. [ Links ]
Liu, H. R. 2007. Whole grain phytochemicals and health. J. Cereal Sci. 46: 207-219. [ Links ]
Natella, F., F. Belelli, V. Gentili, F. Ursini, and C. Scaccini, C. 2002. Grape seed proanthocyanidins prevent plasma postprandial oxidative stress in humans. J. Agric. Food Chem. 50: 7720–7725. [ Links ]
OBouayeba, A. P., N. B. Djyh, S. Diabate, A. J. Djaman, J. D. N'guessan, M. Kone, and T. H. Kouakou. 2014. Phytochemical and antioxidant activity of Roselle (Hibiscus sabdariffa L.) petal extracts. Res. J. Pharm. Biol. Chem. Sci. 5: 1453-1465. [ Links ]
Pérez-Ramírez, I. F., E. Castaño-Tostado, J. A. Ramírez-De León, N. E. Rocha-Guzmán, and R. Reynoso-Camacho. 2015. Effect of stevia and citric acid on the stability of phenolic compounds and in vitro antioxidant and antidiabetic capacity of a roselle (Hibiscus sabdariffa L.) beverage. Food Chem. 172: 885-892. [ Links ]
Prenesti, E., S. Berto, P.G. Daniele, and S. Toso. 2007. Antioxidant power quantification of decoction and cold infusions of Hibiscus sabdariffa flowers. Food Chem. 100: 433-438. [ Links ]
Ramírez-Rodríguez, M. M., M. L. Plaza, A. Azeredo, M. O. Balaban, and M. R. Marshall. 2011. Physicochemical and phytochemical properties of cold and hot water extraction from Hibiscus sabdariffa. J. Food Sci. 76, Nr. 3: 428-435. [ Links ]
Rodríguez-Medina, I. C., R. Beltrán-Debón, V. Micol Molina, V., C. Alonso-Villaverde, J. Joven, J. A. Menéndez, A. Segura-Carretero, A., and A. Fernández-Gutiérrez. 2009. Direct characterization of aqueous extract of Hibiscus sabdariffa using HPLC with diode array detection coupled to ESI and ion trap MS. J. Separ. Sci. 32: 3441-3448. [ Links ]
Salinas-Moreno Y., G. Salas-Sánchez, D. Rubio-Hernández, and N. Ramos- Lobato. 2005. Characterization of anthocyanin extracts from maize kernels. J. Chromatogr. Sci. 43: 483-487. [ Links ]
Salinas-Moreno, Y., A. R. E. Zúñiga-Hernández, L. B. Jiménez-De la Torre, V. Serrano-Altamirano, y C. Sánchez-Feria. 2012. Color en cálices de jamaica (Hibiscus sabdariffa L.) y su relación con características físico-químicas de sus extractos acuosos. Rev. Chapingo Serie Hortic. 18: 395-407. [ Links ]
Saura-Calixto, F., J. Serrano, and I. Goñi. 2007. Intake and bioaccessibility of total polyphenols in a whole diet. Food Chem. 101: 492-501. [ Links ]
Sáyago-Ayerdi S. G., S. Arranz, J. Serrano, and I. Goñi. 2007. Dietary fiber content and associated antioxidant compounds in roselle flower (H. sabdariffa L.) beverage. J. Agric. Food Chem. 55: 7786-7890. [ Links ]
Shahidi, F., and M. Naczk. 2004. Phenolic compounds in fruits and vegetables. In: Shahidi, F., and M. Naczk (eds). Phenolics in Foods and Nutraceuticals. CRC Press. pp: 131-239. [ Links ]
Singleton, V. L. and J. J. A. Rossi. 1965. Colorimetric of total phenolics with phosphomolybdic-phosphotungstic acid reagents. Am. J. Enol.Viticul. 16: 144-158. [ Links ]
Soler-Rivas, C., J. C. Espín, and H. J. Wichers. 2000. An easy and fast test to compare total free radical scavenger capacity of foodstuffs. Phytochem. Anal. 11: 330-338 [ Links ]
Tsai, Pi-Jen, J. Macintosh, P. Pearce, B. Camden, and B. R. Jordan. 2002. Anthocyanin and antioxidant capacity in Roselle (Hibiscus sabdariffa L.) extract. Food Res. Inter. 35: 351-356. [ Links ]
Tseng, T-H., C-J. Wang, E-S. Kao, and H-Y. Chu. 1996. Hibiscus protocatechuic acid protects against oxidative damage induced by tert-butylhydroperoxide in rat primary hepatocytes. Chem-Biol. Interac. 101: 137-148. [ Links ]
Tseng, T-H., E-S. Kao, H-Y. Chu, F-P. Chow, W-L. Lin, and C-J. Wang. 2000. Induction of apoptosis by Hibiscus protocatechuic acid in human leukemia cells via reduction of retinoblastoma (RB) phosphorylation and Bcl-2 expression. Biochem. Pharmacol. 60: 307-315. [ Links ]
Wallace, T. C., and M. M. Giusti. 2010. Evaluation of parameters that affect the 4-Dimethylaminocinnamaldehyde assay for flavonols and proanthocyanidins. J. Food Sci. 75: 619-625. [ Links ]
Watanabe, T. Y. Arai, Y. Mitsui, T. Yusara, W. Okawa, and Y. Kajihara. 2006. The blood pressure–lowering effect and safety of chlorogenic acid from green coffee bean extract in essential hypertension. Clin.Exp. Hypertens. 28: 439-49. [ Links ]














