Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Boletín médico del Hospital Infantil de México
versión impresa ISSN 1665-1146
Bol. Med. Hosp. Infant. Mex. vol.69 no.3 México abr./jun. 2012
Artículo de revisión
Tendencia mundial de la supervivencia en pacientes pediátricos con leucemia linfoblástica aguda. Revisión de las últimas cuatro décadas
Global trend of survival in pediatric acute lymphoblastic leukemia: a review of the last four decades
Mario Enrique Rendón-Macías,1 Nancy Carolina Reyes-Zepeda,2 Miguel Ángel Villasís-Keever,1 Jacobo Serrano Meneses,1 Alberto Escamilla Núñez1
1 Unidad de Investigación en Epidemiología Clínica, Unidad de Alta Especialidad Médica Hospital de Pediatría, Centro Médico Nacional Siglo XXI, Instituto Mexicano del Seguro Social
2 Servicio de Hematología, Centro Médico Nacional 20 de Noviembre, Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado México D.F., México
Autor de correspondencia:
Dr. Miguel Angel Villasis Keever
Correo electrónico: miguel.villasis@imss.gob.mx.
Fecha de recepción: 03-05-12
Fecha de aceptación: 11-05-12
RESUMEN
Introducción. La leucemia linfoblástica aguda es la neoplasia maligna más frecuente en la infancia. En la actualidad, el impacto de la quimioterapia ha resultado en una mayor supervivencia, aunque los resultados son diferentes entre los países.
Metodología. Se revisó la literatura médica disponible en Medline sobre el informe de supervivencia global y supervivencia libre de enfermedad en niños con leucemia linfoblástica aguda, desde finales de los años setenta hasta el 2007. Se analizó la supervivencia de acuerdo con el desarrollo económico del país (países desarrollados y en vías de desarrollo), y por edad, sexo, tipo celular y cuenta leucocitaria al diagnóstico.
Resultados. En países desarrollados se ha observado un incremento en la supervivencia global a cinco años, de 60% en 1984 a 83.5% en el 2007, y en la supervivencia libre de enfermedad, de 48.5% a 83.5%. En los países en desarrollo, hasta el 2006, el promedio de supervivencia global y libre de enfermedad continuaba en, aproximadamente, 60%.
La supervivencia con respecto a la edad es más favorable en los niños de 1 a 9 años (>80%) que en los mayores de 10 años (70-80%). Con respecto al sexo es 5% mayor en las mujeres que en los varones; con respecto al tipo celular es 10% mayor en leucemias de células B que en células T y, de acuerdo con la cifra de leucocitos, cuando la cifra resulta <10,000 mm3 al diagnóstico es 20% mayor que cuando los valores son >10,000 mm3. Existe escasa información para los países en desarrollo.
Conclusiones. La supervivencia de los pacientes con leucemia linfoblástica aguda sigue en aumento, sobre todo la supervivencia libre de enfermedad. Los factores pronóstico de edad, sexo, tipo celular y celularidad continúan siendo válidos. Es necesario realizar más estudios en países en vías de desarrollo.
Palabras clave: leucemia linfoblástica aguda, supervivencia, supervivencia libre de enfermedad, niños.
ABSTRACT
Background. Acute lymphoblastic leukemia (ALL) is the most common malignancy in childhood. The impact of chemotherapy has resulted in improved survival, although results have not been the same for all countries.
Methods. We reviewed the available medical literature in Medline on reports of overall and disease-free survival in children with ALL from the late 1970s to 2007. Survival was analyzed according to economic development (developed and developing countries) and according to age, sex, cell type and leukocyte count at diagnosis.
Results. In developed countries there has been an increase in overall 5-year survival from 60% in 1984 to 83.5% in 2007 and for disease-free survival from 48.5% to 83.5%. This was not registered in developing countries where until 2006 the average overall survival and disease-free survival was ~60%. At diagnosis, prognostic factors related with higher survival rates are age (1 to 9 years), sex (females), type of leukemia (B-cell leukemia) and leukocyte count <10,000 mm3. Information regarding survival rates is very scarce.
Conclusions. Survival of children with ALL is increasing, particularly disease-free survival rates. Prognostic factors related to survival are age, sex, cell type and leukocyte count. Further studies are needed in developing countries.
Key words: acute lymphoblastic leukemia, survival, disease-free survival, children.
INTRODUCCIÓN
Las leucemias agudas constituyen las neoplasias más frecuentes en la edad pediátrica.1 A escala mundial, su incidencia se estima entre 20 a 35 casos por cada millón de habitantes al año.2 Sin embargo, en México, la incidencia es mayor. Se estima que ocurren 49.5 casos nuevos por millón de habitantes al año.3 A pesar de que el cáncer en edad pediátrica es de alrededor del 1% de los casos nuevos de cáncer en una población, los mejores resultados del tratamiento se observan en este grupo etario.4
En particular, el concepto de la leucemia linfoblástica aguda (LLA) y varios tipos de linfomas ha cambiado: de ser enfermedades mortales ahora se consideran altamente curables. Este éxito se debe a diferentes factores. Principalmente se ha atribuido a la aparición de nuevos y mejores medicamentos quimioterapéuticos, además del apoyo a los pacientes para evitar, revertir o limitar los efectos secundarios a los mismos.5-9
A pesar de que existen varios informes sobre los resultados a mediano plazo del tratamiento de niños con LLA, no se conocen publicaciones que sinteticen el progreso obtenido en los últimos 25 años. Aun cuando, en los diferentes reportes, se observa el incremento en la supervivencia global y en la supervivencia libre de enfermedad, estos datos provienen principalmente de países desarrollados.9-12 Se cuenta con poca información sobre este aspecto de lo que sucede en países en vías de desarrollo, y la disponible no siempre tiene la calidad suficiente para juzgar críticamente el impacto del tratamiento que reciben los niños con LLA en estas regiones.13,14
Por lo anterior, el objetivo de esta revisión fue mostrar los cambios en la supervivencia global y libre de enfermedad que se han reportado a escala mundial, particularmente en los países desarrollados y, en la medida de lo posible, contrastarlos con lo que ocurre en los países en vías de desarrollo.
MÉTODOS
Se llevó a cabo una revisión sistematizada de los artículos disponibles en IndexMedicus, de 1960 al 2010. Se realizó la búsqueda a través de Medline mediante el uso de los siguientes términos MeSH (Medical SubHeadings): leukemia, survival, disease free survival, survival analysis, child, adolescent, mortality, prognosis. Se consiguieron las publicaciones in extenso de los resúmenes obtenidos, para identificar si cumplían con los criterios de selección. Se incluyeron los artículos que describieran cohortes de pacientes pediátricos con LLA, donde se mostrara la supervivencia global a cinco años o más a partir del inicio del seguimiento. Asimismo, para identificar un mayor número de publicaciones, se revisaron las citaciones de los artículos seleccionados.
Cada uno de los estudios incluidos debería reportar, por lo menos, el porcentaje de supervivencia global (o total). Sin embargo, también se consideraron las publicaciones que informaron la supervivencia libre de enfermedad, es decir, el porcentaje de supervivencia alcanzado después de obtener remisión completa, posterior al esquema inicial de tratamiento con quimioterapia (inducción a la remisión). Además, se juzgó pertinente agregar, como análisis secundario, la información de la supervivencia de acuerdo con los principales pronósticos establecidos a la fecha, que son el sexo (masculino o femenino), la edad de los pacientes (menores o mayores de 10 años), el número de leucocitos al momento del diagnóstico (< 10,000/mm3 o > 50,000/ mm3) y el tipo celular (linfoblastos tipo B o T).15
Para los propósitos de este estudio, la información, que se presenta por medio de cuadros y gráficos representativos, es solamente de tipo descriptivo. De cada artículo se obtuvo el porcentaje de supervivencia reportado a cinco años. Debido a que, generalmente, la supervivencia se describe en relación con las cohortes integradas durante un periodo (año de inicio-año de término), los datos obtenidos para el presente reporte son los que se informan del último año de seguimiento de la cohorte por cada grupo de niños con LLA. Lo anterior, habitualmente, corresponde con el promedio de supervivencia con respecto a los años analizados. La información se presenta en periodos de cinco años a fin de mostrar la tendencia, aunque en algunas publicaciones se describe la supervivencia con periodos que abarcaron hasta 25 años. Sin embargo, hubo casos en los que no fue posible obtener tendencias porque solamente se reportó un valor puntual. Esto ocurrió con mayor frecuencia en las publicaciones de países en vías en desarrollo. Cabe señalar que, aun cuando la mayor parte de los estudios incluidos documentaron la experiencia por país, algunos solamente reportaron la experiencia de un centro hospitalario, mientras que otros informaron la supervivencia desglosada de acuerdo con distintos esquemas terapéuticos o protocolos de manejo. También se integró la información de la supervivencia de acuerdo con los factores pronóstico ya mencionados. Por último, con el propósito de mostrar la tendencia anual global, se conjuntaron los datos de todas las publicaciones. Así, la información que se presenta corresponde al promedio y error estándar del porcentaje de supervivencia de todas las cohortes.
RESULTADOS
De la revisión de la literatura se obtuvo información de 23 países, desarrollados (Alemania, Austria, República Checa, Dinamarca, Estados Unidos de Norteamérica, Grecia, Israel, Italia, Japón, Reino Unido, Suiza y Taiwán)16-26 y en vías de desarrollo (Brasil, Costa Rica, Cuba, China, Filipinas, Guatemala, Honduras, India, Nicaragua, El Salvador y Tailandia).27-31 Los datos se registraron desde 1981 hasta el 2007. En total fueron 49,921 pacientes, la mayoría de países desarrollados (90.9%). Debido a que, en comparación con los países en vías de desarrollo, la información de los países desarrollados se documenta por periodos de más de cinco años, se decidió separarla.
Supervivencia global de niños con LLA
Se registraron los porcentajes de supervivencia de acuerdo con el año, el protocolo de tratamiento y el país. En general, en los países desarrollados, la supervivencia global mostró un incremento sustantivo durante la década de los ochenta (Figura 1), de un inicial aproximado de 54 a 70% a un final de hasta 85%. A partir de los noventa, a pesar que la supervivencia continuó incrementando, la variación fue menor, de 82 al 90% (Cuadro 1).

La información de los países en vías de desarrollo fue escasa, en comparación con la de los países desarrollados (Figura 2). La mayoría reportó la supervivencia de un solo periodo y a partir de los noventa (Cuadro 2). El único informe que reportó la supervivencia en los ochenta fue el de Kadan-Lottick y colaboradores —en una población hispana en EUA—, quienes mostraron una supervivencia inicial del 52 a 57%. A partir de 1991, este grupo informó una supervivencia del 70%.9 El resto de los países en desarrollo informó supervivencias de entre 30 y 68%, con un promedio de 50% durante los años noventa. Cabe mencionar que los países latinos, con excepción de El Salvador,13 reportaron la supervivencia a tres años y la calcularon junto con los pacientes con diagnóstico de linfoma.

Supervivencia libre de enfermedad de niños con LLA
Con respecto a la supervivencia libre de enfermedad, los datos también resultaron diferentes entre los países desarrollados y en vías de desarrollo (Cuadros 1 y 2). Como se observa, hasta mediados de la década 2000-2010, el incremento de la supervivencia libre de enfermedad ha sido paulatino en los países desarrollados (Figura 3). La supervivencia a mediados de los ochenta era de alrededor de 40 a 65%; durante los noventa, entre 60 a 80%. Afortunadamente, en los últimos cinco años no ha disminuido a menos de 75% en la mayoría de los países. La disminución de los periodos entre la supervivencia libre de enfermedad y la supervivencia global ha sido trascendental.

En los países en vías desarrollo de Asia (India, China, Filipinas y Tailandia) se han informado supervivencias de entre 30 a 60% a cinco años. En Latinoamérica solo se encontraron dos reportes. El de El Salvador, con una supervivencia libre de enfermedad para 1996 de 46% y el de Brasil, donde se presentaron los datos de tres periodos: los ochenta, con una supervivencia del 21%; el inicio de los noventa, con 47% y los últimos años de los noventa y principios de este siglo, de casi 60%. No se encontraron informes publicados en revistas indexadas o de difusión de lo que sucede en México al respecto (Figura 4).
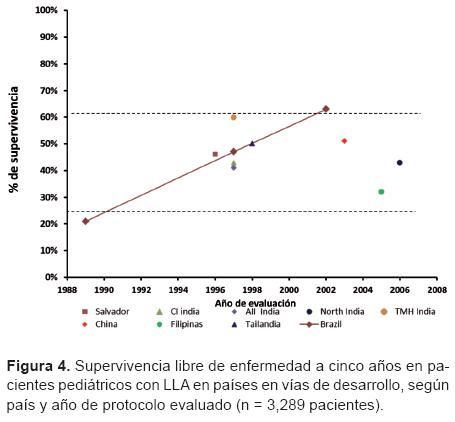
Supervivencia relacionada con los factores de riesgo
Actualmente, a pesar de considerarse nuevos factores pronóstico de riesgo, el análisis de los factores relacionados con la edad, el tipo celular (B o T) y la cuenta leucocitaria al diagnóstico continúan describiéndose en los reportes más recientes. Sin embargo, esta información solo pudo recabarse para los países desarrollados: se muestran los datos puntuales asociados a la supervivencia global (Cuadro 3) y libre de enfermedad según los factores pronóstico incluidos (Cuadro 4).
La supervivencia global y la supervivencia libre de enfermedad mostraron tendencias al incremento en ambos sexos, aunque al parecer es mayor para las mujeres (Figura 5).

Con respecto a la edad, los pacientes entre 1-9 años continúan con mejor pronóstico que el resto (Figura 6). En general, la supervivencia ha aumentado de 5 a 10% (desde los ochenta y hasta el 2005) en este grupo de edad. Por otro lado, en los pacientes mayores de 10 años, aun cuando la supervivencia también ha mejorado es proporcionalmente inferior a la del grupo de 1-9 años y con grandes variaciones entre los países.

Según el tipo celular, las leucemias de células B en todo momento han mostrado mejor pronóstico que las derivadas del linaje T (Figura 7). A pesar de esto, se ha observado un incremento en la supervivencia de hasta 20% en estas, en los últimos años. Conviene mencionar que en el año 1983 se observa una supervivencia alta en ambos tipos; sin embargo, esta cifra resultó sesgada, ya que se consideraron solamente a los pacientes de bajo riesgo.

Al parecer, el factor pronóstico de mayor importancia entre los evaluados hasta el momento ha sido la cuenta leucocitaria al diagnóstico. Los pacientes con cuentas menores a 10,000/mm3 son los que han presentado mejor supervivencia, tanto global (Figura 8) como libre de enfermedad (Figura 9). En ellos, incluso, la supervivencia ha alcanzado 90% de los pacientes. Los pacientes con peor pronóstico son los que han presentado cuentas por encima de 100,000/mm3. La supervivencia global y la libre de enfermedad muestran gran variabilidad entre los países y protocolos. En promedio, la primera se encuentra alrededor de 60%, mientras que la segunda está en 50%. Sin embargo, como se observó con otros factores pronósticos, también existe una tendencia hacia la mayor supervivencia en los años recientes.


DISCUSIÓN
El pronóstico de los pacientes pediátricos con LLA ha mejorado en forma significativa en las últimas tres décadas.32 Sin embargo, de acuerdo con los resultados de esta revisión, la mejoría en la supervivencia de este grupo de pacientes no ha mostrado la misma magnitud en los países desarrollados que en los países en vías de desarrollo. Además, estos últimos no cuentan con estudios multicéntricos ni con estadísticas completas. Las estrategias utilizadas para mejorar el pronóstico han sido el uso de esquemas de quimioterapia más intensivos y con múltiples drogas, así como una mejor clasificación de los pacientes para definir su riesgo de recaída. En este último aspecto, la estratificación de los pacientes (en bajo o alto riesgo) inicialmente se hacía con base en la edad, sexo y cuenta leucocitaria. Posteriormente, la citogenética marcó un gran avance para definir el pronóstico.15 Recientemente, la identificación de la enfermedad mínima residual. De esta forma, la clasificación de los pacientes de acuerdo con sus características ha permitido brindar terapias dirigidas, acordes con el pronóstico de cada paciente, para mejorar su efectividad y disminuir la toxicidad.4
En la década de los ochenta, la supervivencia de los pacientes pediátricos con LLA era de alrededor de 60%, y la mortalidad se asociaba principalmente con las infecciones y las recaídas.1,11 Posteriormente, para incrementar la supervivencia los protocolos de quimioterapia se enfocaron en el aumento de las dosis de los medicamentos y en la combinación de los mismos, para disminuir la resistencia. Sin embargo, la mortalidad asociada a una mayor toxicidad de los esquemas de quimioterapia incrementó. Por fortuna, los avances en cuanto al tratamiento de las complicaciones permitieron que los efectos adversos disminuyeran o tuvieran un mejor control, como ocurrió con las infecciones.58 Dos décadas después, la supervivencia reportada por grupos multicéntricos de países desarrollados, como el Pediatric Oncology Group32 y el BFM (Berlin-Frankfurt-Münster),21 entre otros, incrementó hasta alrededor de 80%. Esto se atribuyó al uso de esquemas más intensivos de quimioterapia, a la aparición de nuevos medicamentos y al mejor tratamiento de soporte, como la prevención y tratamiento eficaz de las infecciones, así como el apoyo transfusional. Actualmente, la estratificación de los pacientes de acuerdo con su pronóstico permite que aquellos pacientes catalogados como de bajo riesgo logren una supervivencia por arriba de 90%. En contraste, los pacientes en los grupos de alto riesgo, sobre todo los de muy alto riesgo (particularmente el grupo de adolescentes), aún permanecen con tasas de supervivencia bajas —alrededor de 60%—, razón por la cual los estudios actuales se enfocan en mejorar los tratamientos para este grupo de pacientes.32
Al mejorar la supervivencia, las preocupaciones son la toxicidad a largo plazo33 y el desarrollo de segundas neoplasias.34 La incidencia de segundas neoplasias en el sistema nervioso central (SNC) se incrementa con el uso de radioterapia profiláctica, por lo que, en estudios posteriores, se propuso seleccionar a los pacientes que debían recibirla e intensificar el uso de quimioterapia intratecal. Esta estrategia ha probado ser eficaz y segura, ya que no se han reportado incrementos en la tasa de recaídas en el SNC.5-8
Un punto importante para reflexionar es el contraste de la supervivencia alcanzada en pacientes pediátricos con LLA en países en vías de desarrollo. Los estudios muestran que la supervivencia no ha mejorado en forma tan importante como en los países desarrollados.12,13 Si bien en la India, El Salvador, Taiwan e, incluso, México,35 los protocolos de quimioterapia se basan en los grupos multicéntricos internacionales, existe la dificultad de ofrecer el apoyo de soporte que requieren este tipo de pacientes. Esto ha impedido que los protocolos puedan llevarse a cabo en forma estricta, por lo que han requerido modificaciones propias en cada país y, aun, en cada hospital. La supervivencia reportada en este tipo de países se encuentra alrededor del 40%, aunque hay países, como Honduras, que reporta tasas de supervivencia tan bajas como de 29%.12-14
En la actualidad, aún se discute si esta diferencia tan importante —en cuanto a la supervivencia en los países en desarrollo— se debe a aspectos étnicos o socioeconómicos asociados, al retraso en el diagnóstico y tratamiento, o bien, a riesgos particulares, como son los tipos de leucemias y el estado nutricional.36 En EUA han realizado análisis por etnias y han encontrando que la tasa de supervivencia en pacientes hispanos tratados en ese país es inferior a la de los pacientes caucásicos. Existen reportes similares para la población afroamericana. Esto sugiere que los factores socioeconómicos pueden estar implicados, aunque también los factores genéticos.1
Otro elemento que se debe considerar, a fin de identificar estrategias para mejorar el pronóstico, es el registro del momento en el que ocurren los fallecimientos. La mortalidad en la fase de inducción a la remisión en países desarrollados es de alrededor de 3%, mientras que en países en vías de desarrollo es de hasta 25% a pesar de que, con el tiempo, se ha observado una disminución de la tasa de mortalidad.32 Otro rubro que implica la supervivencia a largo plazo son los fallecimientos durante el periodo de remisión: en los países desarrollados la tasa es muy baja (menor al 3%) y en los países en vías de desarrollo se sitúa entre 5 y 10%.32 Un factor más que impacta en la supervivencia global son las recaídas. La tasa es más elevada en pacientes en países en vías de desarrollo, lo que habla de una menor efectividad de los regímenes de quimioterapia. En los países desarrollados, las tasas de recaída de hace 20 años eran de 20%; actualmente, de hasta 10%. En contraste, en la India se reportan tasas de recaída de 30% (aunque en Taiwan son de 10%).23-26,32
Es evidente que la supervivencia de niños con LLA no ha mejorado al mismo ritmo en los países en vías de desarrollo que en los desarrollados. Será necesario realizar investigaciones basadas en estudios multicéntricos en estos países con grupos grandes de pacientes, para comparar, por ejemplo, si los factores pronóstico establecidos en la población anglosajona tienen magnitudes similares, o bien, identificar factores propios de estas poblaciones. Otro punto importante es determinar si los regímenes de quimioterapia son igualmente efectivos y su frecuencia de toxicidad.
Financiamiento. El presente estudio recibió financiamiento por el Sistema de Protección Social en Salud.
REFERENCIAS
1. Gurney JG, Severson RK, Davis S, Robison LL. Incidence of cancer in children in the United States. Sex-, race-, and 1-year age-specific rates by histologic type. Cancer 1995;75:2186-2195. [ Links ]
2. Parkin DW, Stiller CS. Childhood cancer in developing countries: environmental factors. Int J Pediatr Hematol Oncol 1995;2:411-417. [ Links ]
3. Pérez-Saldívar ML, Fajardo-Gutiérrez A, Bernáldez-Ríos R, Martínez-Ávalos A, Medina-Sanson A, Espinosa-Hernández L, et al. Childhood acute leukemias are frequent in Mexico City: descriptive epidemiology. BMC Cancer 2011;11:355. doi:10.1186/1471-2407-11-355. [ Links ]
4. Gaynon PS, Angiolillo AL, Carroll WL, Nachman JB, Trigg ME, Sather HN, et al. Long-term results of the children's cancer group studies for childhood acute lymphoblastic leukemia 1983-2002: a Children's Oncology Group Report. Leukemia 2010;24:285-297. [ Links ]
5. Möricke A, Reiter A, Zimmermann M, Gadner H, Stanulla M, Dördelmann M, et al. Risk-adjusted therapy of acute lympho-blastic leukemia can decrease treatment burden and improve survival: treatment results of 2169 unselected pediatric and adolescent patients enrolled in the trial ALL-BFM 95. Blood 2008;111:4477-4489. [ Links ]
6. Mitchell CD, Richards SM, Kinsey SE, Lilleyman J, Vora A, Eden TO, et al. Benefit of dexamethasone compared with prednisolone for childhood acute lymphoblastic leukaemia: results of the UK Medical Research Council ALL97 randomized trial. Br J Haematol 2005;129:734-745. [ Links ]
7. Moghrabi A, Levy DE, Asselin B, Barr R, Clavell L, Hurwitz C, et al. Results of the Dana-Farber Cancer Institute ALL Consortium Protocol 95-01 for children with acute lymphoblastic leukemia. Blood 2007;109:896-904. [ Links ]
8. Veerman AJ, Kamps WA, van den Berg H, van den Berg E, Bökkerink JP, Bruin MC, et al. Dexamethasone-based therapy for childhood acute lymphoblastic leukaemia: results of the prospective Dutch Childhood Oncology Group (DCOG) protocol ALL-9 (1997-2004). Lancet Oncol 2009;10:957-966. [ Links ]
9. Kadan-Lottick NS, Ness KK, Bhatia S, Gurney JG. Survival variability by race and ethnicity in childhood acute lymphoblastic leukemia. JAMA 2003;290:2008-2014. [ Links ]
10. Tsurusawa M, Shimomura Y, Asami K, Kikuta A, Watanabe A, Horikoshi Y, et al. Long-term results of the Japanese Childhood Cancer and Leukemia Study Group studies 811, 841, 874 and 911 on childhood acute lymphobastic leukemia. Leukemia 2010;24:335-344. [ Links ]
11. Mitchell C, Richards S, Harrison CJ, Eden T. Long-term follow-up of the United Kingdom medical research council protocols for childhood acute lymphoblastic leukaemia, 1980-2001. Leukemia 2010;24:406-418. [ Links ]
12. Valsecchi MG, Tognoni G, Bonilla M, Moreno N, Baez F, Pacheco C, et al. Clinical epidemiology of childhood cancer in Central America and Caribbean countries. Ann Oncol 2004;15:680-685. [ Links ]
13. Bonilla M, Moreno N, Marina N, deReyes G, Shurtleff SA, Downing JR, et al. Acute lymphoblastic leukemia in a developing country: preliminary results of a nonrandomized clinical trial in El Salvador. J Pediatr Hematol Oncol 2000;22:495-501. [ Links ]
14. Laosombat V, Wongchanchailert M, Sattayasevana B, Wiriya-sateinkul A, Watana-Arepornchai S. The treatment of children with acute lymphoblastic leukemia in Thailand. Med Pediatr Oncol 2002;38 266-268. [ Links ]
15. Vrooman LM, Silverman LB. Childhood acute lymphoblastic leukemia: update on prognostic factors. Curr Opin Pediatr 2009;21:1-8. [ Links ]
16. Escherich G, Horstmann MA, Zimmermann M, Janka-Schaub GE, COALL study group. Cooperative study group for childhood acute lymphoblastic leukemia (COALL): long-term results of trials 82, 85, 89, 92 and 97. Leukemia 2010;24:298-308. [ Links ]
17. Stark B, Nirel R, Avrahami G, Abramov A, Attias D, Ballin A, et al. Long-term results of the Israeli National Studies in childhood acute lymphoblastic leukemia: INS 84, 89 and 98. Leukemia 2010;24:419-424. doi: 10.1038/leu.2009.254 [ Links ]
18. Tsuchida M, Ohara A, Manabe A, Kumagai M, Shimada H, Kikuchi A, et al. Long-term results of Tokyo Children's Cancer Study Group trials for childhood lymphoblastic leukemia, 19841999. Leukemia 2010;24:383-396. [ Links ]
19. Pui CH, Pei D, Sandlund JT, Ribeiro RC, Rubnitz JE, Raimondi SC, et al. Long-term results of St. Jude Total Therapy studies 11, 12, 13 A, 13B and 14 for childhood acute lymphoblastic leukemia. Leukemia 2010;24:371-382. doi: 10.1038/leu.2009.252 [ Links ]
20. Liang DC, Yang CP, Lin DT, Hung IJ, Lin KH, Chen JS, et al. Long-term results of Taiwan pediatric oncology group studies 1997 and 2002 for childhood acute lymphoblastic leukemia. Leukemia 2010;24:397-405. [ Links ]
21. Möricke A, Zimmermann M, Reiter A, Henze G, Schrauder A, Gadner H, et al. Long-term results of five consecutive trials in childhood acute lymphoblastic leukemia performed by the ALL-BFM study group from 1981 to 2000. Leukemia 2010;24:265-284. [ Links ]
22. Silverman LB, Stevenson KE, O'Brien JE, Asselin BL, Barr RD, Clavell L, et al. Long-term results of Dana-Farber Cancer Institute ALL Consortium protocols for children with newly diagnosed acute lymphoblastic leukemia (1985-2000). Leukemia 2010;24:320-334. [ Links ]
23. Conter V, Aricö M, Basso G, Biondi A, Barisone E, Messina C, et al. Long-term results of the Italian Association of Pediatric Hematology and Oncology (AIEOP) Studies 82, 87, 88, 91 and 95 for childhood acute lymphoblastic leukemia. Leukemia 2010;24:255-264. [ Links ]
24. Kamps WA, van der Pal-de Bruin KM, Veerman AJ, Fiocco M, Bierings M, Pieters R. Long-term results of Dutch Childhood Oncology Group studies for children with acute lymphoblastic leukemia from 1984 to 2004. Leukemia 2010;24:309-319. [ Links ]
25. Tzortzatou-Stathopoulou F, Papadopoulou AL, Moschovi M, Botsonis A, Tsangaris GT. Low relapse rate in children with acute lymphoblastic leukemia after risk-directed therapy. J Pediatr Hematol Oncol 2001;23:591-597. [ Links ]
26. Stary J, Jabali Y, Trka J, Hrusak O, Gajdos P, Hrstkova H, et al. Long term results of treatment of childhood acute lymphoblastic leukemia in the Czech Republic. Leukemia 2010;24:425-428. [ Links ]
27. Schmiegelow K, Forestier E, Hellebostad M, Heyman M, Kristinsson J, Söderhäll S, et al. Long-term results of NOPHO ALL-92 and ALL-2000 studies of childhood acute lymphoblastic leukemia. Leukemia 2010;24:345-354. [ Links ]
28. Gao YJ, Lu FJ, Wang HS. Treating childhood acute lym-phoblastic leukemia in a developing country 1998-2003: the experience of a single children's hospital in China. J Pediatr Hematol Oncol 2006;28:798-802. [ Links ]
29. Howard SC, Pedrosa M, Lins M, Pedrosa A, Pui CH, Ribeiro RC, et al. Establishment of a pediatric oncology program and outcomes of childhood acute lymphoblastic leukemia in a resource-poor area. JAMA 2004;291:2471-2475. [ Links ]
30. Magrath I, Shanta V, Advani S, Adde M, Arya LS, Banavali S, et al. Treatment of acute lymphoblastic leukemia in countries with limited resources; lessons from use of a single protocol in India over a twenty year period. Eur J Cancer 2005;41:1570-1583. [ Links ]
31. Kulkarni KP, Marwaha RK, Trehan A, Bansal D. Survival outcome in childhood ALL: experience from tertiary care centre in North India. Pediatr Blood Cancer 2009;53:168-173. [ Links ]
32. Salzer WL, Devidas M, Carroll WL, Winick N, Pullen J, Hunger SP, et al. Long-term results of the pediatric oncology group studies for childhood acute lymphoblastic leukemia 19842001: a report from the children's oncology group. Leukemia 2010;24:355-370. [ Links ]
33. Ness KK, Armenian SH, Kadan-Lottick N, Gurney JG. Adverse effects of treatment childhood acute lymphoblastic leukemia: general overview and implications for long-term cardiac health. Expert Rev Hematol 2011;4:185-197. [ Links ]
34. Fulbright JM, Raman S, McClellan WS, August KJ. Late effects of childhood leukemia therapy. Curr Hematol Malig Rep 2011;6:195-205. [ Links ]
35. Rizo-Ríos P, Sánchez-Cervantes F, González-Rivera A, Betancourt-Cravioto M, Meneses-García A, Mohar A, et al. Mortalidad por leucemias en menores de 20 años. México 1998-2002. Bol Med Hosp Infant Mex 2005;62:9-18. [ Links ]
36. Mejía-Aranguré JM, Fajardo-Gutiérrez A, Reyes-Ruíz NI, Bernáldez-Ríos R, Mejía-Domínguez AM, Navarrete-Navarro S, et al. Malnutrition in childhood lymphoblastic leukemia: a predictor of early mortality during the induction-to-remission phase of the treatment. Arch Med Res 1999;30:150-153. [ Links ]














