Introducción
El Bisfenol A [4’4’-dihidroxi-2,2-difenilpropano] (BFA) es un compuesto orgánico con dos grupos fenólicos, tiene una amplia gama de usos, es uno de los químicos de mayor producción a nivel mundial (Industry-Experts, 2018). En la industria este compuesto tiene una gran cantidad de aplicaciones, se utiliza como materia prima para la producción de diferentes tipos de plásticos, entre los que destacan los policarbonatos; es componente de resinas epóxicas de los recubrimientos interiores de latas de comida y se utiliza en la producción de diferentes partes de equipos eléctricos, electrónicos, automovilísticos, etc. (Mikolajewska et al., 2015). Con el paso del tiempo, el BFA es liberado al ambiente como parte de la contaminación ambiental que ocasionan los plásticos y puede ser absorbido o acumulado en organismos vivos a través de las cadenas tróficas (Wang et al., 2017; Mackay et al., 2018; Staples et al., 2018). En el caso de los seres humanos, la exposición se da vía inhalación, ingesta de alimentos empaquetados y a través de la dermis (Ribeiro et al., 2017; Li y Suh, 2019). Estudios recientes en roedores y humanos demostraron que el BFA afecta negativamente al sistema endocrino y con ello a la salud de estos y su descendencia, debido a su potente acción como disruptor endócrino (DE) (Adoamnei et al., 2018; Gómez-Mercado et al., 2018; Baralić et al., 2020; Gorini et al., 2020). Los DE son químicos o mezclas de ellos, exógenos al organismo que se encuentran en alimentos y productos destinados a los consumidores que muestran efectos adversos sobre el sistema endócrino (Nur et al., 2019; Yeung et al., 2019). El BFA es un compuesto aromático, químicamente resistente a la degradación, debido a la deslocalización de su energía y a las densas nubes de electrones presentes en ambos lados de la estructura de su anillo, lo que lo hace extremadamente resistente al ataque nucleofílico (Cajthaml, 2014). A pesar de esto, se han realizado diversos estudios para conocer su degradación y las enzimas que participan en dicho proceso principalmente, la participación de hongos de pudrición blanca (Baker et al., 2019). El BFA puede ser degradado por especies hongos ligninolíticos, tales como: Pleurotus ostreatus, Pleurotus eryngii, Phanerochaete chrysosporium, Trametes versicolor, Trametes villosa (Song et al., 2007; Martínková et al., 2016; Kresinová et al., 2018), Stereum hirsutum, Heterobasidium insulare y Grifola frondosa entre otros (Nitheranont et al., 2011; Traversa et al., 2012). Estos hongos excretan enzimas ligninolíticas como las lacasas y manganeso peroxidasas (Mn-P) que pueden descomponer total o parcialmente al BFA (Gassara et al., 2013; Escalona et al., 2014; Hou et al., 2014; Baker et al., 2019). Por lo que han recibido importante atención para el establecimiento de estrategias de biorremediación, debido a que catalizan la sustracción de un electrón de los grupos hidroxilo fenólicos (reacción acompañada de una desmetilación y formación de quinona) que genera la escisión del anillo (Husain y Qayyum, 2012). Una característica natural tecnológicamente útil para la degradación de diversos compuestos aromáticos. Además, el uso de hongos ligninolíticos producen mediadores de bajo peso molecular que amplían el espectro de contaminantes que son capaces de oxidar (Cajthaml, 2014; Ahuactzin-Pérez et al., 2018c). Sin embargo, existen pocos estudios que describen los parámetros cinéticos del crecimiento y producción enzimática de lacasas por P. ostreatus durante el proceso de degradación de BFA. Es por esto, que el propósito de este trabajo fue caracterizar el crecimiento y producción de enzimas lacasas durante el proceso de degradación de BFA por P. ostreatus cultivado en fermentación sumergida.
Materiales y métodos
Organismo de estudio e inóculo
En esta investigación se utilizó el hongo P. ostreatus, proveniente de cultivos industriales, depositado y conservado en el cepario del Laboratorio de Biología Experimental con la clave BE01, de la Facultad de Agrobiología de la Universidad Autónoma de Tlaxcala. Para la obtención del inóculo, el hongo se cultivó en Agar Papa Dextrosa (PDA) durante 7 d a 28 °C, los inóculos se obtuvieron de la periferia de las colonias con 10 mm de diámetro.
Medio y condiciones de cultivo
Se utilizaron tres medios de cultivo: 1) GYE (g/L): glucosa, 10 g; extracto de levadura, 5 g; KH2PO4, 0.9 g; K2HPO4, 0.6 g; CuSO4-5H2O, 0.3 g; Na2HPO4, 0.1 g; FeSO4-7H2O, 0.05 g; MnSO4, 0.05 g y ZnSO4-7H2O, 0.01 g). 2) GYE + 50 mg/L de BFA y 3) GYE + 75 mg/L de BFA. El pH del medio se ajustó a 6.5 con NaOH 0.1 M. El hongo se cultivó en fermentación sumergida utilizando matraces Erlenmeyer de 125 mL, a cada uno se les agregó 50 mL de medio de cultivo adicionado con la concentración correspondiente de BFA (50 y 75 mg/L), se esterilizaron (a 121 °C y 15 psi) y cada matraz se sembró con tres inóculos y fueron incubados en una incubadora orbital (PRENDO) a 120 rpm, durante 23 días a 28 °C. El hongo se desarrolló, bajo una fermentación sumergida.
Obtención del extracto crudo enzimático y determinación de la producción de biomasa
El extracto crudo enzimático (ECE) fue el sobrenadante de los cultivos y se obtuvo por filtración (decantación) y retención de biomasa en papel filtro Whatman No. 4. La biomasa retenida sobre el papel Whatman se secó hasta peso constante para la cuantificación del crecimiento fúngico empleando el método de peso seco (Ahuactzin-Pérez et al., 2014).
Las curvas de crecimiento fúngico se establecieron mediante la ecuación logística por la minimización del error cuadrático con la herramienta Solver de la hoja electrónica de Excel (Microsoft) (Viniegra-González et al., 2003; Ahuactzin-Pérez et al., 2018c)pectinases and tannases, by Aspergillus niger grown by SSF and SmF is reviewed. To do such a comparative study, logistic and Luedeking-Piret equations are used in order to estimate the values of the following coefficients: maximal specific growth rate (μM, como se muestra a continuación en la ecuación
Donde, µ corresponde a la velocidad específica de crecimiento obtenida y Xmáx a la biomasa máxima (o de equilibrio) producida cuando dX/dt = 0 para X > 0.
La solución de la Ec. (1) es la siguiente:
Donde, C = (X máx - X 0 )/X 0 ; cuando X = X 0 es el valor inicial de la biomasa.
Parámetros cinéticos de crecimiento y producción de enzimas lacasas
El rendimiento de la enzima con respecto a la biomasa (Y E/X ) se estimó como la relación entre la enzima máxima producida durante la fermentación (E máx ) (U/L) y la (X máx ) (g/L). Se calculó el rendimiento de la biomasa con respecto al sustrato (Y X/S ) empleando la X máx y la concentración inicial de la fuente de carbono. La productividad en el pico máximo de actividad (PRO) se calculó mediante la ecuación (PRO= E máx /tiempo de fermentación y por último, la tasa específica de formación de la enzima (qp) se determinó empleando la siguiente formula (qp=µ*Y E/X ) (Díaz et al., 2013).
Determinación del consumo de glucosa
El consumo de glucosa se cuantificó a través de la presencia de la cantidad de azúcares reductores por el método DNS (ácido dinitrosalicílico) y una curva de calibración con glucosa (0 - 100 mg/L de glucosa). La mezcla de reacción (50µL de ECE, 950 µL de agua destilada y 2 mL de solución DNS [NaOH 1 % , Na2SO3 0.05 % , fenol 0.2 % y DNS 1 %]) se calentó a punto de ebullición durante 5 min y la lectura de la absorbencia se realizó en un espectrofotómetro“METASH-UV6000” a 575 nm (Miller, 1959).
Perfiles de pH
Los perfiles del pH durante el crecimiento de P. ostreatus en medio líquido se obtuvieron con el método de potenciometría, con el equipo Hanna instruments HI 9811-5. El potenciómetro se calibró empleando bufers de referencia a un pH de 4, 7 y 10.
Actividad enzimática de lacasas
La actividad de lacasas se cuantificó con el sustrato 2,6-dimetoxifenol (SIGMA) 2 mM en buffer de acetatos 0.1 M y pH de 4.5. La mezcla de reacción (475 (L de sustrato, 50 (L de ECE) se incubó a 39 °C por 1 min. La reacción se detuvo por la adición de 475 (L de dimetil sulfóxido (SIGMA). La absorbancia se leyó a 468 nm en un espectrofotómetro “METASH-UV6000”. Una unidad de actividad de lacasas es la cantidad de enzima que provoca incrementos de 1.0 unidad en la absorbancia por minuto de incubación (Díaz et al., 2013).
Porcentaje y constante de biodegradación del BFA
Para la cuantificación de la biodegradación de BFA se realizó empleando una alícuota de 1 mL de ECE por cada réplica de la fermentación (3) y se sometió a shock térmico (a temperatura de ebullición) durante 1 minuto, se evaporó en un horno de secado a 50 °C durante 24 h. Posteriormente, para su cuantificación y análisis la alícuota se resuspendió en 2 mL de acetonitrilo. Los extractos se analizaron con un sistema HPLC Agilent 110 de fase inversa, equipado con una columna C18 y un detector de absorbencia UV de 245-360 nm en condiciones isocráticas en acetonitrilo:agua (90:10) y a un caudal de 1 mL/min.
La biodegradación de BFA se determinó midiendo su desaparición en el medio de cultivo. Se realizó una curva de calibración, en un intervalo de concentraciones de 0-100 ppm de BFA con el comportamiento de la Ec (2).
Donde, x es la concentración correspondiente a cada área bajo la curva de los días de fermentación. El porcentaje de biodegradación (% BD) en el intervalo de tiempo (h) se calculó mediante la
Donde:
C0 = concentración inicial del BFA en la solución de ensayo (mg/L).
Ct = concentración de BFA en la solución de ensayo en el tiempo t.
Se graficó el tiempo de fermentación en comparación con el logaritmo natural (ln) de la concentración de BFA, posteriormente se aplicó una regresión lineal. La pendiente de la regresión se consideró la constante de biodegradación de primer orden (k) expresada en h-1 (Ahuactzin-Pérez et al., 2016; Ahuactzin-Pérez et al., 2018c).
Análisis estadístico
Todos los experimentos se llevaron a cabo por triplicado, empleando un diseño experimental unifactorial completamente aleatorizado de tres niveles. Los datos se evaluaron mediante un ANOVA de una vía y una prueba post-hoc de Tukey con el programa The Graph Pad Prism® program (San Diego, CA, USA) (Córdoba-Sosa et al., 2014).
Resultados
Parámetros cinéticos de crecimiento
En el medio GYE se obtuvo un valor de 3.45 g/L para la X máx , el cual fue menor con respecto a los medios de cultivo con BFA. En el mismo medio se obtuvo un valor menor de µ con respecto a los tratamientos con BFA (Fig. 1). Sin embargo, el valor de X máx no fue significativamente diferente de los otros tratamientos. El hongo P. ostreatus presentó un valor de X máx de 4.9 g/L en el medio que contenía 50 mg/L de BFA y una µ de 0.01 h-1. En comparación con el medio con 75 mg/L de BFA en donde se presentó una X máx de 5.3 g/L y una µ 0.014 h -1 (Tabla 1,Fig. 1). No hubieron diferencias significativas entre las medias de los valores correspondientes a la X máx y a la µ en todos los tratamientos (p<0.05).
Tabla 1 Parámetros cinéticos de crecimiento de P. ostreatus cultivado sobre
BFA en fermentación sumergida
Table 1. Kinetic
growth parameters of P. ostreatus grown on BPA in
submerged fermentation
| Parámetro | Medio de cultivo BFA (mg/L) |
|||
|---|---|---|---|---|
| 0 | 50 | 75 | Valor de P | |
| µ (h-1) | 0.008 ± 0.0005c | 0.010 ± 0.0009b | 0.014 ± 0.0003a | 0.0051 |
| Xmáx (g/L) | 3.45 ± 0.104c | 4.9 ± 0.04b | 5.3 ± 0.01a | 0.0001 |
| Y(X/S) (gx/gs) | 0.34 ± 0.010c | 0.49 ± 0.004b | 0.52 ± 0.001a | 0.0002 |
X ± d.s. a, b, .c Literales diferentes en la misma fila indica diferencias significativas (p<0.05).

Figura 1 Crecimiento y producción de biomasa de P. ostreatus en medio GYE (●),
GYE/50 mg/L de BFA (◌) y GYE/75 (□) mg/L de BFA en fermentación
sumergida, determinado por el método de peso seco.
Figure 1. Growth and biomass production of
P. ostreatus in GYE (●), GYE/50 mg/L of BPA (◌)
and GYE/75 (□) mg/L of BPA medium in submerged fermentation,
determined by the dry weight method.
Consumo de glucosa
El hongo consumió el 100 % de la glucosa en el tratamiento testigo y en el medio con 75 mg/L de BFA después de 432 h de crecimiento (Fig. 2). Mientras que en el medio con 50 mg/L de BFA el consumo total de glucosa fue lento (transcurridas 480 h de crecimiento) (Fig. 2). En todos los tratamientos, el consumo de glucosa total correspondió con el inicio de la fase estacionaria de crecimiento de P. ostreatus

Figura 2 Consumo de glucosa por P. ostreatus en medio GYE (●), GYE/50 mg/L de
BFA (◌) y GYE/75 (□) mg/L de BFA en fermentación sumergida,
determinado por el método de DNS.
Figure 2. Glucose
consumption by P. ostreatus in GYE (●), GYE/50 mg/L
of BFA (◌) and GYE/75 (□) mg/L of BPA medium in submerged
fermentation, determined by the DNS method.
Perfiles de pH
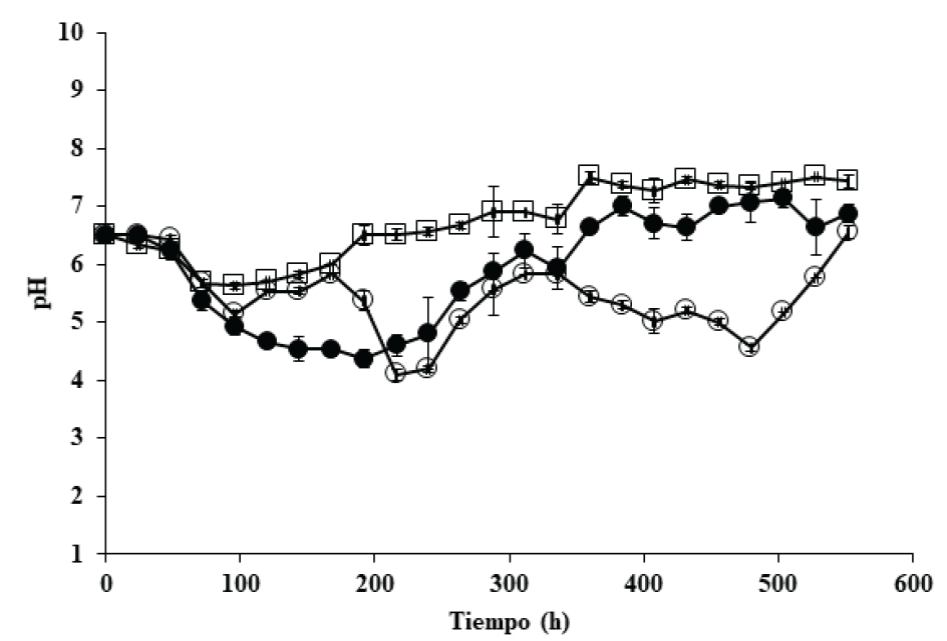
En el perfil de pH durante el crecimiento de P. ostreatus en el medio GYE se observó una disminución progresiva de 6.2 a 4.7 entre las 48 y 192 h (fase de adaptación y exponencial), respectivamente. Posteriormente, un aumento del pH hasta 7.4 a las 552 h se registró. En el medio con 50 mg/L de BFA se observó un intervalo de pH de 5.8 a 4.2 durante las primeras 336 h de crecimiento fúngico, hasta llegar a un pH de 6.5 al final de la fermentación. El perfil de pH en el medio con 75 mg/L de BFA mostró una disminución durante las primeras 96 h. Después, el pH alcanzó un valor de 6.3 que incrementó al finalizar la fermentación a 7.5 (Fig. 3).
Actividad enzimática de lacasas
La mayor actividad de enzimas lacasas se presentó en el medio con mayor concentración de BFA, con un valor de 238 U/L a las 336 h (Tabla 2, Fig. 4). Con respecto al medio con 50 mg/L de BFA, la producción de estas enzimas durante las primeras horas de crecimiento fue menor a 10 U/L. Sin embargo, las 159 U/L se alcanzaron a las 288 h (Fig. 4). La menor actividad enzimática se mostró en el medio GYE con un máximo de 33 U/L a las 192 h de crecimiento (Fig. 4).
Tabla 2 Parámetros cinéticos de producción de lacasas de P. ostreatus
cultivado sobre BFA en fermentación sumergida.
Table
2. Laccase production kinetic parameters of P.
ostreatus grown on BPA in submerged fermentation.
| Parámetro | Medio de cultivo | |||
|---|---|---|---|---|
| BFA (mg/L) | ||||
| 0 | 50 | 75 | Valor de P | |
| Emáx (U/L) | 33.17 ± 15.34c | 210 ± 10.83b | 238.24 ± 1.28a | 0.0008 |
| YE/X (U/gX) | 25 ± 11.56c | 65.93 ± 3.39a | 53.43 ± 0.29b | 0.0051 |
| PRO (UL/h) | 0.17 ± 0.08c | 0.63 ± 0.03a | 0.71 ± 0.003b | 0.0002 |
X ± d.s. a, b, .c Literales diferentes en la misma fila indica diferencias significativas (p<0.05).
Parámetros cinéticos de producción de lacasas
Con respecto a los parámetros de E máx , Y E/X , P RO y q p , se presentaron los valores mayores en el medio 75 mg/L de BFA. Valores significativamente diferentes de los obtenidos en el medio GYE (p< 0.05) (Tabla 2). El valor de YE/X para el medio GYE no presentó diferencia significativa (p< 0.05) con respecto a los medios que contienen BFA. Sin embargo, en el medio con 50 mg/L de BFA, el valor de YE/X fue significativamente diferente al que presentó el medio de crecimiento con la mayor concentración de BFA, mientras que el medio GYE fue el que mostró menor rendimiento (Tabla 2). Los valores de la Emáx , PRO y qp, mostraron diferencias significativas (p< 0.05) en el medio GYE y en los medios con BFA, estos parámetros no mostraron diferencia significativa (Tabla 2).
Porcentaje y constante de biodegradación del BFA
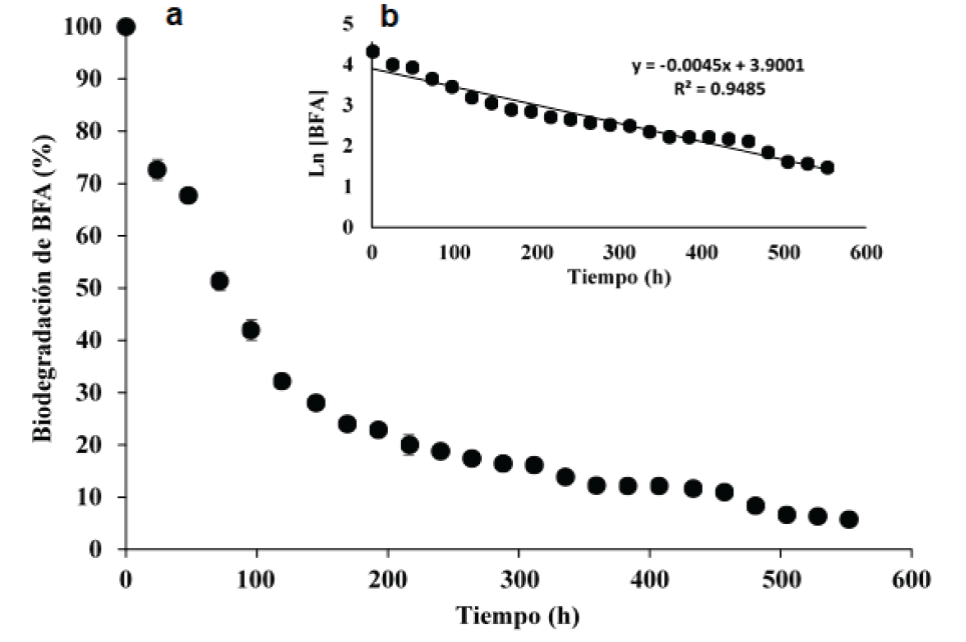
En el medio con 75 mg/L de BFA, después de 552 h de crecimiento en fermentación líquida, P. ostreatus degradó hasta un 94.3 % de dicho compuesto. Durante el inicio de la fase de adaptación (las primeras 48 h) el hongo degradó el 67.7 % de la concentración inicial (Fig. 6a). Para este medio se obtuvo un valor de k de 0.0045 h-1 (Fig. 6b). En el medio con menor concentración de BFA, P. ostreatus degradó más del 50% de la concentración inicial (50 mg/L) después de 96 h de incubación y alcanzó un 98.3 % de degradación a las 552 h, y un valor de k de 0.0051 h-1 (Fig. 5a,b).

Figura 5 Porcentaje de biodegradación de 50 mg/L de BFA (a) y constante de biodegradación (b).
Figure 5. Biodegradation percentage of 50
mg/L BFA (a) and biodegradation constant (b).
Discusión
En esta investigación se utilizó el modelo de la “ecuación logística” para explicar el crecimiento de P. ostreatus en fermentación sumergida. El criterio de selección del modelo fue que en las cinéticas de crecimiento fúngico mostró un coeficiente de correlación mayor a 99 %. Este modelo describió el comportamiento del crecimiento de este hongo bajo las condiciones evaluadas de fermentación. Ahuactzin-Pérez et al. (2018a) evaluaron la degradación de 500 y 1000 mg/L de di (2-etilhexil) ftalato (DEHF) (un compuesto fenólico plastificante en la industria de plásticos) por una cepa diferente de P. ostreatus. Ellos reportaron en tratamientos testigo y con concentraciones de DEHF la obtención de una X máx de 5.19, 6.53 y 7.69 g/L, respectivamente. Así como, una µ de 0.21, 0.022 y 0.018 h-1. Estos resultados son similares a los descritos en este trabajo. En la observación de que en los medios de cultivo adicionados con la mayor concentración de BFA se obtuvieron los mayores rendimientos (3.45, 4.9 y 5.3 g/L en los medios GYE, 50 y 75 mg/L de BFA) de X máx , pero una menor µ (0.0088, 0.01 y 0.014 h-1 respectivamente). Sin embargo, estos resultados difieren con los obtenidos por Tlecuitl-Beristain et al. (2008) , quienes reportan para esta especie después de 480 h de crecimiento en medio líquido sin la adición de algún xenobiótico; una µ y X máx superior de 0.02 h-1 y 7.8 g/L, respectivamente. Ahuactzin-Pérez et al. (2016) reportaron el consumo total de glucosa por el hongo Fusarium culmorum después de 290 y 240 h de crecimiento sobre 500 y 1000 mg/L de DEHF, respectivamente. En comparación con los datos obtenidos en esta investigación, el consumo total de glucosa en el medio GYE y con 75 mg/L de BFA por P. ostreatus se observó a las 432 h. Sin embargo, en el medio con 50 mg/L de BFA se prolongó hasta las 480 h.
En cuanto al efecto del pH en el crecimiento fúngico, en los tres medios se muestran cambios similares a los reportados por Ahuactzin-Pérez et al. (2016) . Mediante el ajuste del pH inicial a 6.5 en los tres tratamientos (GYE, 500 y 1000 mg/L de DEHF) se observó un pH final de 6.8, 6.4 y 4.5, respectivamente. En el presente trabajo se obtuvo un pH final de 6.8, 6.4 y 7.4 para los tratamientos testigo, con 50 y 75 mg/L de BFA, respectivamente. Con respecto a la actividad enzimática de lacasas, Ortega-Ávila (2015) describió el comportamiento de la producción de lacasas en el medio GYE adicionado con Cu como inductor, donde obtuvo una E máx de 120 y 119 U/L a las 312 y 336 h de crecimiento, respectivamente. La comparación de los resultados obtenidos en este trabajo, la actividad de lacasas fue menor a la reportado por Ortega-Ávila (2015). Sin embargo, los resultados indican que el BFA o los intermediarios de su degradación ejercen un efecto inductor sobre la producción de estas enzimas. Si bien, en esta investigación no se evaluó el efecto inductivo del BFA sobre los perfiles de enzimas lacasas, se conoce que estas enzimas son responsables de la degradación de este compuesto (Hou et al., 2014; Neiverth de Freitas et al., 2017; Kresinová et al., 2018). Díaz et al. (2013) mencionan que la mayor producción de enzimas lacasas para P. ostreatus se presenta con un pH inicial de crecimiento de 6.5 en el medio de cultivo y a un pH de actividad de 4.5, en medios sin presencia de BFA. Este comportamiento se observó en el medio testigo empleado en nuestra investigación, contrario a los medios adicionados con BFA, donde la actividad y parámetros cinéticos enzimáticos fueron mayores, por lo que nos permite sugerir que estos incrementos se deben a la presencia de BFA y no al pH.
Díaz et al. (2011) evaluaron diferentes parámetros cinéticos de producción (E máx , Y E/X , P y la q p ) en diversas cepas del género Pleurotus cultivado en medios de cultivo, con y sin la adicción de Cu++. La observación fue que la cepa de P. ostreatus ATCC32783 mostró valores mayores en los parámetros cinéticos de producción de la enzima lacasa en presencia de Cu++ en el medio de cultivo. En esta investigación se observó que P. ostreatus cultivado en los medios conteniendo BFA, obtuvo valores de los parámetros cinéticos de producción de la enzima menores a los obtenidos por Díaz et al. (2011).
Los hongos T. versicolor, P. ostreatus, Irpex lacteus y S. hirsutum han sido especies de hongos ligninolíticos que han degradado por arriba del 95 % de la concentración inicial (50 mg/L) en un lapso de 5 a 7 días crecidas en medios líquidos y sólidos en un rango de pH (4.5-5) y temperatura de (20-30 °C) (Song et al., 2007; Traversa et al., 2012). Por otro lado, Cajthaml et al. (2009) y Zhang et al. (2015) reportan la degradación de 10 mg/L de BFA por cepas de P. ostreatus. Los resultados mostraron una eficiencia de degradación del 99 % de la concentración inicial a los 3 y 7 días del crecimiento de P. ostreatus, respectivamente. Contrario a lo reportado por estos autores, en esta investigación se emplearon concentraciones 5 y 7.5 veces mayores a las reportadas por ellos. P. ostreatus degradó más del 50 % de la concentración inicial a partir de los primero 4 y 3 días, a una k de 0.0045 y 0.0051 h-1, respectivamente. Estos resultados sugieren que P. ostreatus logra degradar concentraciones superiores a las que se encuentran en diferentes muestras de agua que ponen en riesgo la salud pública (Nur et al., 2019; Petrie et al., 2019; Zhang et al., 2019).
Conclusiones
Durante el proceso de degradación de BFA en un sistema de fermentación sumergida, P. ostreatus logró incrementar sus parámetros cinéticos de crecimiento y producción de enzimas lacasas, parámetros, inversamente proporcionales a la degradación de BFA. P. ostreatus puede utilizar al BFA como fuente secundaria de carbono durante un cometabolismo, esto con base en el consumo total de la glucosa. P. ostreatus mostró valores de pH ácidos en el medio testigo e incrementaron en un rango neutro-básico en los medios que contenían BFA, lo que nos permitió inferir que el incremento en los valores de este parámetro es una medida indirecta de la degradación de este compuesto. Se sugiere que el BFA y algunos de sus subproductos podrían tener un efecto inductor en la producción de lacasas, mostrando una correlación positiva entre la concentración de BFA y la producción de estas enzimas. Esta cepa fúngica es eficiente en la biodegradación de BFA, ya que presentó un porcentaje de degradación mayor al 50 % durante los primeros 3 d de crecimiento y finalizó a los 21 d con más del 97 % de la concentración inicial más alta, concentración que hasta el momento no ha sido reportado por otros autores y que es superior a las reportadas en matrices ambientales que ponen en riesgo la salud humana.











 nueva página del texto (beta)
nueva página del texto (beta)