Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista mexicana de ciencias agrícolas
versión impresa ISSN 2007-0934
Rev. Mex. Cienc. Agríc vol.6 no.3 Texcoco abr./may. 2015
Notas de investigación
Respuesta de plántulas de Cedrela odorata a la inoculación con Rhizophagus intraradices y diferentes niveles de defoliación*
Response of Cedrela odorata seedlings to inoculation with Rhizophagus intraradices and different defoliation levels
Iván Oros-Ortega1,2, Alejandro Alonso-López1, Jesús Pérez-Moreno3, Jorge C. López-Collado1, Luis A. Lara-Pérez4, Sandra E. Martínez-Garza1, Laura Y. Solís-Ramos5 y Antonio Andrade-Torres4§
1 Colegio de Postgraduados-Campus Veracruz. Carretera Federal Veracruz-Xalapa, km 26.5 Predio Tepatates, Mpio. Manlio Fabio Altamirano, C. P. 91700, Veracruz, México.
2 Universidad Tecnológica de Gutiérrez Zamora. Gutiérrez Zamora, Prol. Dr. Miguel Patiño s/n. Colonia Centro, Gutiérrez Zamora, Veracruz, México.
3 Colegio de Postgraduados-Campus Montecillo, Carretera México-Texcoco, km 36.5, C. P. 56230, Montecillo, Estado de México, México.
4 INBIOTECA-Universidad Veracruzana, A. P. 250, C. P. 91000, Xalapa, Veracruz, México. CA-UVER-173 Ecología y Manejo de la Biodiversidad. §Autor para correspondencia: aandradet@gmail.com.
5 Escuela de Biología-Universidad de Costa Rica, San José, Costa Rica.
* Recibido: octubre de 2014
Aceptado: febrero de 2015
Resumen
Respuesta de plántulas de Cedrela odorata a la inoculación con Rhizophagus intraradices y diferentes niveles de defoliación ; el efecto de seis tratamientos (T) sobre la tasa de crecimiento en altura (TCA) , diámetro ( TCD ) , tasa de crecimiento relativo (TCR ) y peso fresco y seco de plántulas de C. odorata se evaluaron en un vivero. Se utilizó un diseño completamente al azar con arreglo factorial (2 x 3); TS consistió en una combinación de los factores: porcentaje de defoliación (0, 50 y 90) y la inoculación de R. intraradices (con y sin inoculación). Después de seis meses, las plántulas de TS con la inoculación, independientemente del porcentaje de defoliación aplicada, mostraron más TCD (F= 100.45, p< 0,001) que TS sin inoculación. Las TS inoculadas, con diferentes niveles de defoliación, mostró el mayor TCA (F= 556.57 p< 0,001) después de tres meses. Sin embargo los últimos tres meses la interacción de la inoculación/defoliación (50 y 90 %) indujo el mayor valor de TCA (F= 4.22 p< 0.01), y un crecimiento significativo en el peso fresco y seco de tallos, hojas y raíces. La inoculación produce altos niveles de micorrización en las raíces de C. odorata en el sexto mes. La defoliación al 90 % reduce significativamente la colonización de hifas y vesículas. Durante los tres primeros meses, las TS inoculadas mostraron el valor más alto de TCR, sin embargo, en los últimos tres meses los tratamientos sin inoculación y defoliación al 90% presentaron la mayor TCR. La interacción Inoculación / defoliación tiene efectos en el desarrollo de C. odorata, por lo que es conveniente considerar este tratamiento para la producción de plántulas en vivero.
Palabras clave: cedro español, micorrizas arbusculares, tasa de crecimiento relativo.
Abstract
Response of Cedrela odorata seedlings to inoculation with Rhizophagus intraradices and different defoliation levels; the effect of six treatments (T) on growth rate in height (TCA), diameter (TCD), relative growth rate (TCR) and fresh and dry weight of C. odorata seedlings were evaluated in a nursery. A completely randomized design with a factorial arrangement (2 x 3) was applied; the TS consisted of a combination of the factors: percentage of defoliation (0, 50 and 90) and inoculation of R. intraradices (with and without inoculation). After six months, the seedlings in TSs with inoculation, regardless of the percentage of defoliation applied, showed more TCD (F= 100.45, p< 0.001) than TSs without inoculation. The inoculated TSs, with different levels of defoliation, showed the highest TCA (F= 556.57 p< 0.001) after three months. However the last three months inoculation/defoliation interaction (50 and 90%) induced the highest value of TCA (F= 4.22 p< 0.01), and a significant growth in fresh and dry weight of stems, leaves and roots. Inoculation produces high levels of mycorrhizal colonization in roots of C. odorata at the sixth month. Defoliation at 90 % significantly reduces hyphae and vesicle colonization. During the first three months, inoculated TSs showed the highest value of TCR, however in the last three months the treatments without inoculation and defoliation at 90% showed the highest TCR. Inoculation/defoliation interaction has effects in the development of C. odorata, so it is convenient to consider this treatment for seedlings production in nursery.
Keyswords: arbuscular mycorrhizal, relative growth rate, Spanish cedar.
La especie Cedrela odorata (cedro amargo -Costa Rica-; cedro rojo -México-, Patiño, 1997; Gonzáles et al., 2013), es una especie maderable que se puede encontrar desde el norte de México, hasta el norte de Argentina, ya que tolera un rango variable de condiciones climáticas pero es más común en zonas con una época seca bien marcada y altitudes que van desde el nivel del mar hasta 1 200 m (Navarro et al., 2005; Patiño, 1997; Navarro et al., 2005, Gómez et al., 2007). Es un árbol caducifolio de hasta 45 m de altura con un diámetro a la altura del pecho de hasta 2 m, en general su tamaño varia según las condiciones ambientales en las que se encuentre (Patiño, 1997; Hernández, 2008). Esta especie está sujeta a protección especial en México (NOM-059-SEMARNAT-2010); sin embargo, su madera es considerada el segundo producto más valioso obtenido de bosques tropicales, lo que la hace una especie de gran interés económico, con alta demanda internacional y por lo tanto puede contribuir localmente al desarrollo económico y social en México, Costa Rica y otros países de Centro América (Patiño, 1997; Ramírez et al., 2012).
No obstante la rápida expansión del cultivo de cedro en el trópico, aun no existe un sistema de manejo adecuado para las plántulas, así como para otros puntos importantes en su desarrollo, lo cual influyen en la productividad de las plantaciones establecidas. Las investigaciones sobre C. odorata se han enfocado en el estudio de su diversidad genética, su filogenia y propagación in vitro (Pérez et al., 2002, García-Gonzáles et al., 2011). Pero muy pocas han tenido como objetivo el estudio de las relaciones simbióticas que establece con microorganismos del suelo, por lo tanto, es poco lo que se sabe sobre sus efectos en el desarrollo del cedro, sea en condiciones naturales o en plantaciones.
Tampoco se ha estudiado si la simbiosis puede ayudar en la respuesta o resistencia de esta especie al ataque de insectos como el barrenador de las meliáceas (Shi et al., 2006; Murata et al., 2013). En la mayoría de las plantaciones se utiliza planta producida en vivero, pero con baja calidad, susceptible a enfermedades y plagas. La micorriza arbuscular (MA) influye en un mejor desarrollo y crecimiento de las plantas tropicales durante los primeros meses de desarrollo (Alvarado et al., 2004; Souza et al., 2006). Algunas especies del género Cedrela son potencialmente formadoras de micorriza con los géneros Glomus y Acualospora, (Lovelock y Ewel, 2005; Souza et al., 2006).
Recientemente, Méndez-Cortés et al. (2013), obtuvieron alta colonización micorrízica al inocular plántulas de C. odorata con esporas nativas procedentes de selva alta perennifolia y selva mediana subperennifolia. No obstante, en la producción de plantas con fines productivos se ha ignorado la inoculación micorrízica. Por lo tanto es importante generar información del proceso de desarrollo de las plántulas bajo condiciones de invernadero así como realizar estudios sobre las interacciones simbióticas. Los resultados de estos estudios pueden contribuir a mejorar la productividad de las plantaciones.
Aunado a esto, por la naturaleza caducifolia de C. odorata la defoliación es otro factor que influye en el crecimiento de dicha especie (Rodgers, 1995; Gerhardt, 1998). Los carbohidratos producidos en una planta, a través del tiempo, se traslocan en diferentes proporciones a la parte aérea y radical, además si la planta es podada se balancea tal repartición entre los diferentes órganos (Poorter y Nagel, 2000). Cuando existe buena disponibilidad de agua y la parte aérea de plantas de C. odorata se daña o una porción se defolia, el almidón almacenado en la raíz se asigna al rebrote de hojas para reajustar la relación existente entre parte aérea/raíz (Rodgers et al., 1995; Poorter y Hayashida-Oliver, 2000); también es probable que en campo las reservas de almidón sean importantes durante la estación seca y el inicio del crecimiento vegetativo y reproductivo después que caen las hojas (Rodgers et al., 1995) y que la defoliación disminuya la presencia y el porcentaje de colonización micorrízica (Saito et al., 2004).
Sin embargo, el efecto de la interacción de la inoculación micorrízica y la defoliación pueden contribuir a obtener plantas con mejor calidad en vivero y alta supervivencia al transplantar a campo. El presente estudio evalúa el efecto de dichos factores en el desarrollo y tasas de crecimiento de plántulas de C. odorata en fase de vivero.
El experimento se desarrolló en vivero en el Colegio de Postgraduados en Ciencias Agrícolas, Campus Veracruz (19° 16’ latitud norte y 96° 16’ longitud oeste), a una altitud de 20 m. El clima es cálido subhúmedo, con una temperatura media de 26.5 °C y 1 230 mm de precipitación. Las lluvias se distribuyen entre los meses de mayo a octubre (García, 1988). Se germinaron semillas de diferentes árboles de C. odorata en suelo esterilizado (4 h a 125 °C y 1.5 kg cm-2 en autoclave). Las plántulas de ochenta días de edad se transplantaron a bolsas de plástico de 21 cm alto x 10 cm ancho, con 570 g de suelo seco estéril y se inocularon con una cepa de Rhizophagus intraradices, proporcionada por el Laboratorio de Microbiología del Colegio de Postgraduados en Ciencias Agrícolas.
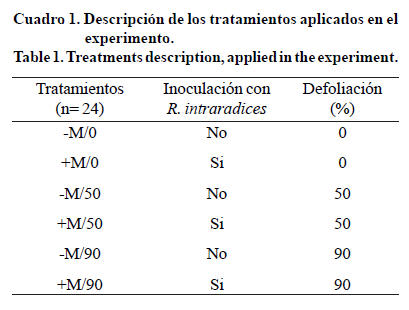
Las plantas permanecieron en vivero, a temperatura ambiente (promedio 27 °C, con máxima de 36.4 ºC), humedad relativa de 33 a 96%, y la intensidad de luz máxima fue de 805 lum/sqf (datos obtenidos con Data Loger Hobo H8 Pro Series RH). Se utilizó un diseño experimental completamente al azar, con un arreglo factorial para evaluar los factores defoliación e inoculación (3 x 2 respectivamente) (Cuadro 1). Para determinar los porcentajes de defoliación, se estimó el área foliar total de las plántulas utilizando el programa Adobe Photoshop Cs3 Extended y se procedió con el corte de hojas para cada tratamiento.
Se evaluó: 1) tasa de crecimiento en diámetro (TCD) (Villar et al., 2004); 2) tasa de crecimiento en altura (TCA) (Villar et al., 2004); 3) peso seco total en gramos (PST); 4) peso seco de raíz en gramos (PSR); 5) área foliar; 6) porcentaje de colonización micorrízica (Phillips y Hayman (1970) modificado por Kormanik et al., 1980); y 7) tasa de crecimiento relativo (TCR) (Poorter, 1989) y tasa de asimilación neta (TAN) (Evans, 1972). El suelo utilizado como substrato se analizó al inicio del experimento: a) textura del suelo: arena 52.8%, arcilla 10% y limo 37.2%; b) pH: 6.24; c) materia orgánica (2.96 %); d) nitrógeno inorgánico: 24.5 ppm; e) fósforo (13 ppm); f) potasio rico (ppm); g) capacidad de campo (29.65%); y h) punto de marchitez permanente: 16.12%. Para determinar diferencias significativas entre tratamientos Las variables de las variables TCD, TCA, TAN.
Se aplicó un análisis de varianza y separación de medias con la prueba de Tukey (p≤ 0.05). Los datos de porcentaje de colonización micorrízica fueron modificados a la transformación angular o arco seno. Las variables peso seco total y tasa de crecimiento relativo se compararon con el análisis no paramétrico de la varianza Kruskal Wallis, con un nivel de significancia de 5%. Se utilizó el paquete Statistica (Stat Soft, Inc. 2011).
A los seis meses la TCD fue mayor en los tratamientos con micorriza y no se observaron efectos por la defoliación para ninguno de los tratamientos (F= 100.45, p< 0.001) (Figura 1-A). La TCA fue mayor en los tratamientos con micorriza (+M/0, +M/50 y +M/90), en comparación con los tratamientos -M/0 y -M/50. Se observó que la defoliación a 90% incrementa la TCA con diferencia significativa en ausencia de micorriza. Sin embargo, la interacción de los factores micorriza/defoliación al 50% (+M/50) producen mayor TCA con diferencia significativa (F= 4.34, p< 0.01) (Figura 1-C). Los tratamientos con micorriza (+M) presentaron mayor peso seco comparados con los tratamientos sin micorriza; sin embargo, solo el tratamiento +M/50 presentó diferencia significativa (F= 209.24 p< 0.001) (Figura 1-B). Tanto para la TCR y la TAN los tratamientos con micorriza presentaron los mejores valores, no se encontraron efectos por la interacción defoliación/micorriza entre tratamientos (Figura 1-D, E). Se observó que la defoliación tiene un efecto negativo en el porcentaje de colonización por hifas y vesículas, no afecta el porcentaje de colonización por arbúsculos (Figura 1-F).
La inoculación micorrízica, bajo las condiciones de este estudio, es el factor principal para promover el crecimiento vegetal. Lone y Khan (2007), encontraron que defoliar plantas de Brassica juncea a 50% antes y después de la floración (40 y 60 días de siembra), mejora la eficiencia fotosintética en las hojas restantes e incrementa la biomasa seca. Este incremento es atribuido al aumento en la asimilación de CO2 debido a las altas tasas de fotosíntesis por las hojas jóvenes (Lone y Khan, 2007). Las plantas de C. odorata tuvieron mejor crecimiento cuando se defoliaron al 50%, se observa una rápida recuperación después del corte.
Cuando se aplican defoliaciones de menor intensidad en Acacia mangium se favorece el crecimiento de la raíz (principal fuente de carbohidratos de reserva), esto puede ser resultado de la división y elongación celular activadas para reponer tejidos removidos (Rodríguez-Pettit y Razz, 2003). Medhurst et al. (2006) evaluaron el efecto de la defoliación en la tasa fotosintética de Acacia melanoxylon de 5 años de edad creciendo bajo Pinus radiata, observaron un incremento de 50% en la capacidad fotosintética entre las 2 y 6 semanas en plantas defoliadas respecto al control, estos aumentos son promovidos principalmente por la asignación de carbono.
Lovelock et al. (1999) encontraron que la defoliación de plántulas del árbol tropical Copaifera aromatica, incrementa la fotosíntesis en niveles normales de CO2, la defoliación también incrementó el área foliar, no obstante después de 41 días las plantas defoliadas no compensaron el tejido perdido por la defoliación. Honkanen et al. (1994) consideran que cuando las hojas jóvenes son defoliadas se incrementa la concentración de auxinas o de carbohidratos. Niveles altos de TAN pueden ser resultado de una alta tasa fotosintética, esto requiere una gran cantidad de luz y enzimas, lo cual disminuye las tasas de crecimiento (Poorter, 1989).
Existe, por tanto, un compromiso para la planta entre una mayor asignación de biomasa a hojas, con la consecuente mayor capacidad para captar luz y dióxido de carbono, redundando en su mayor tasa de crecimiento o bien, en una mayor asignación de biomasa a las raíces, consiguiendo así captar más agua y nutrientes minerales del suelo, pero a expensas de un menor crecimiento (Villar et al., 2004).
En esta captación de nutrimentos es importante la presencia de micorriza y se ve reflejado en las diferencias significativas en el crecimiento de los diferentes tratamientos. Méndez-Cortés et al. (2013) obtuvieron alto porcentaje de colonización en plántulas de C. odorata aplicando suelo rizosférico con hifas y esporas como fuente de inóculo natural. En este trabajo, la inoculación de R. intraradices en cedro indujo altos porcentajes de colonización micorrízica, no obstante que se considera que la defoliación disminuye la colonización micorrízica (Allsop, 1998; Cortés, 2008), por lo tanto es claro que el cedro rojo es una especie micorrízica tal como lo propusieron Wang y Qiu (2006) en su revisión mundial de distribución filogenética y evolución de la micorriza.
Los resultados encontrados del efecto positivo de la inoculación micorrízica en el crecimiento de planta de cedro contrastan con lo hallado por Cortés (2008) en ilama (Annona diversifolia Saff.) donde encontró en campo mayor colonización total, porcentaje de arbúsculos y vesículas en época de lluvias cuando las plantas tenían hojas.
También encontró altos porcentajes de micorrización (41-70%) inoculando R. intraradices, Aucalospora delicata, y el consorcio Zack 19 (constituido por Glomus albidum, G. claroides y G. diaphanum) pero no observó efecto en el crecimiento de las plantas. No obstante, encontró que plantas con follaje e inoculadas con Zack 19, presentaron significativamente mayor porcentaje de colonización total respecto a plantas sin follaje. En el presente estudio se observó que la defoliación a 90% disminuye significativamente el porcentaje de colonización por hifas. Estos resultados contrastan con el hecho de que se ha encontrado que las estructuras micorrízicas funcionalmente importantes se recuperan más rápido de la defoliación que el promedio de colonización total en la raíz (Klironomos et al., 2004; Ilmarinen et al., 2007).
Saito et al. (2004) observaron en Miscanthus, que la colonización micorrízica por Glomus-Ac y Glomus-Ad fue significativamente reducida por la defoliación, mientras que en Zoysa no es afectada por la defoliación. El hongo micorrízico arbuscular R. intraradices se ha probado en diferentes cultivos, en los cuales se ha demostrado que tiene una exitosa colonización; fue evaluado in vitro en raíces de Agave salmiana Otto transformadas genéticamente y se observó que tuvo 70% de colonización (Rodríguez et al., 2007).
La mayoría de los estudios han reportado que la defoliación reduce las tasas de colonización por hongos MA en las raíces de las plantas (Gehring y Whitham, 1994). Lovelock et al. (1999) mencionan que los niveles nutrimentales en el suelo también pueden influenciar la respuesta de la planta a la defoliación, por ejemplo bajos niveles de nutrimentos que no son rápidamente translocables (Ej. calcio) puede restringir el potencial de la fotosíntesis compensatoria y crecimiento después de la defoliación.
Se ha estudiado poco la caracterización y porcentaje de colonización micorrízica en especies de planta tropicales (Lovelock, 1999; Alvarado et al., 2004; Ewel y Lovelock, 2005; Chable, 2007; Cortés, 2008). Existen además pocos trabajos relacionados con el efecto de la defoliación en la presencia de hongos micorrízicos arbusculares, los cuales son importantes ya que estos hongos consumen una proporción substancial de los compuestos carbonados producidos por la planta (Smith y Read, 1997).
Conclusión
Este trabajo demuestra que la interacción de los factores micorriza/defoliación produce plantas de C. odorata con mayor tasa de crecimiento. Combinando estos resultados con lo reportado por Méndez-Cortés et al. (2013), es muy probable que se pueda encontrar un método simple y económico para producir plantas de C. odorata en vivero con mayor desarrollo y calidad de planta, mediante la aplicación de suelo rizosférico en bajo porcentaje y defoliación al 50%, lo cual puede favorecer el establecimiento y el desempeño de las plantas en campo al estar inoculadas con cepas nativas.
Agradecimientos
Al CONACYT por la beca de posgrado (204524) del primer autor. Al PROMEP por el proyecto PROMEP/103.5/13/6998 (UV-EXB-491).
Literatura citada
Allsop, N. 1998. Effect of defoliation on the arbuscular mycorrhizas of three perennial pasture and rangeland grasses. Plant Soil. 202:117-124. [ Links ]
Alvarado, A.; Chavarria M.; Guerrero R.; Boniche, J. y Navarro J. N. 2004. Características edáficas y presencia de micorrizas en plantaciones de teca (Tectona grandis L. f.) en Costa Rica. Agron. Costarric. 28 (1):89-100. [ Links ]
Chable, C. O. 2007. Inoculación micorrízica arbuscular y uso de vermicomposta en la producción de plantas de cedro (C. odorata L.) en vivero. Tesis Maestría en Ciencias. Colegio de Postgraduados en Ciencias Agrícolas- Campus Campeche. Programa en Agricultura Tropical. Campeche, México. 79 p. [ Links ]
Cortés, J. 2008. Dinámica de microorganismos rizosféricos y filosféricos de Annona diversifolia Saff. como respuesta a la estacionalidad, fenología y defoliación en el trópico seco. Tesis de maestría. Colegio de Postgraduados en Ciencias Agrícolas- Campus Montecillo, Montecillo, Texcoco, México, 71 p. [ Links ]
Diario Oficial de la Federación (DOF). 2010. Norma Oficial Mexicana NOM-059-SEMARNAT; Diario Oficial 2010. Secretaría de Medio Ambiente y Recursos Naturales. México D. F. [ Links ]
Evans, G. C. 1972. The quantitative analysis of plant growth. Blackwell Scientific Publications, Oxford. 734 p. [ Links ]
García, E. 1988. Modificaciones al sistema de clasificación climática de Köeppen (para adaptarlo a las condiciones de la República Mexicana). Instituto de Geografía. Universidad Autónoma de México (UNAM). México, D. F. 252 p. [ Links ]
García-Gonzáles, R. G.; Delgado, M.; Gonzales, Y.; Gonzales, A.; Garriga, M.; Caligari, P.; Carrasco, B. and Quiroz, K. 2011. In vitro propagation of cedar (Cedrela odorata) from juvenile shoots. Chilean journal of agricultural research. 71(3):376-382. [ Links ]
Gehring, C. A. and Whitham, T. G. 1994. Interaction between aboveground herbivores and the mycorrhizal mutualists of plants. Tree. 9:251-255. [ Links ]
Gerhardt, K. 1998. Leaf defoliation of tropical dry forest tree seedlings - implications for survival and growth. Trees. 13:88-95. [ Links ]
Gómez, J.; Monterroso, A. y Tinoco, A. 2007. Distribución del cedro rojo en el estado de Hidalgo bajo condiciones actuales y escenarios de cambios climáticos. Madera y Bosques. 13(2):299-49. [ Links ]
Hernandez, L. 2008. Genetic diversity and mating system analysis of Cedrela odorata L. (Meliaceae) populations under different human dominated landscape and primary forests. Tesis Mageister Scientiae, CATIE, Turrialba, Costa Rica. 74 p. [ Links ]
Honkanen, T.; Haukioja, E. and Suomela, J. 1994. Effects of simulated defoliation and debudding on needle and shoot growth in Scots pine (Pinus sylvestris): implications of plant source/sink relationship for plant-herbivore Studies. Funct. Ecol. 8:631-639. [ Links ]
Ilmarinen, K.; Mikola, J. and Vestbergb, M. 2008. Do interactions with soil organisms mediate grass responses to defoliation? Soil Biol. Biochem. 40:894-905. [ Links ]
Klironomos, J. N.; McCune, J. and Moutoglis, P. 2004. Species of arbuscular mycorrhizal fungi affect mycorrhizal responses to simulated herbivory. Appl. Soil Ecol. 26:133-141. [ Links ]
Kormanik, P. P.; Bryan, W. C. and Schultz, R. C. 1980. Procedures and equipment for staining large numbers of plant root samples for endomycorrhizal assay. Can. J. Microbiol. 26:536-538. [ Links ]
Lone, N. A. and Khan, N. A. 2007. The effect of rate and timing of N fertilizer on growth, photosynthesis, N accumulation and yield of mustard (Brassica juncea) subjected to defoliation. Environ. Exp. Bot. 60:318-323. [ Links ]
Lovelock, E.; Posada, J. and Winter, K. 1999. Effects of elevated CO2 and defoliation on compensatory growth and photosynthesis of seedlings in a tropical tree Copaifera aromatica. Biotropica. 31(2):279-287. [ Links ]
Lovelock. E. and Ewel, J. 2005. Link between tree species, symbiotic fungal diversity and ecosystem functioning in simplified tropical ecosystems. New Phytol. 167:219-228. [ Links ]
Medhurst, J. L; Pinkard, E. A.; Beadle, C. L. and Worledge, D. 2006. Photosynthetic capacity increases in Acacia melanoxylon following form pruning in a two-species plantation. Forest Ecol. Manag. 233:250-259. [ Links ]
Méndez-Cortés, H.; Marmolejo-Monsiváis, J. G.; Cantú-Ayala, C.; Olalde-Portugal, V.; Estrada-Castillón, E. and Posadas-Leal, C. 2013. Respuesta de Cedrela odorata L. a diversos inoculantes micorrízicos procedentes de dos ecosistemas tropicales. Madera y Bosques. 19(3):23-34. [ Links ]
Mikola, J.; Nieminen, M.; Ilmarinen K. and Vestberg, M. 2005. Belowground responses by AM fungi and animal trophic groups to repeated defoliation in an experimental grassland community. Soil Biol. Biochem. 37:1630-1639. [ Links ]
Murata, H.; Yamada, A.; Maruyama, T.; Endo, N.; Yamamoto, K.; Ohira, T. and Shimokawa, T. 2013. Root endophyte interaction between ectomycorrhizal basidiomycete Tricholoma matsutake and arbuscular mycorrhizal tree Cedrela odorata, allowing in vitro synthesis of rhizospheric "shiro". Mycorrhiza. 23:235-242. [ Links ]
Navarro, C.; Cavers, S.; Pappinen, A.; Tigerstedt, P.; Lowe, A. J.; and Merila, J. 2005. Contrasting quantitative traits and neutral genetic markers for genetic resource assessment of Mesoamerican Cedrela odorata. Silvae Genetica. 54(6):281-292. [ Links ]
Patiño, F. 1997. Recursos genéticos de Swietenia y Cedrela en los neotrópicos. Propuestas para Acciones Coordinadas. Organización de las Naciones Unidas para la Agricultura y la Alimentación (FAO). Roma-Italia. 58 p. [ Links ]
Pérez, J.; Mesen, F.; Hilje, L. and Aguilar, M. 2002. Desarrollo de un método de micropropagación aplicable a genotipos selectos de Cedrela odorata. Rev. Forest. Centroame. 30:67-71. [ Links ]
Phillips, J. M. and Hayman, D. S. 1970. Improved procedures for cleaning roots and staining parasitic and vesicular arbuscular mycorrhizal fungi for rapid assessment of infection. Trans. Br. Mycol. Soc. 55:158-161. [ Links ]
Poorter, H. 1989. Interspecific variation in relative growth rate: on ecological causes and physiological consecuences. In: Lambers, H.; Cambridge, M. L.; Konings, H. and Pons, T. L. (Eds.). SPB Academic Publishing, The Hague. Causes and consequences of variation in growth rate and productivity of higher plants. 45-68 pp. [ Links ]
Poorter, L. and Hayashida-Oliver, Y. 2000. Effects of seasonal drought on gap and understorey seedlings in a Bolivian moist forest. J. Trop. Ecol. 16(4):481-498. [ Links ]
Poorter, H. and Nagel, O. 2000. The role of biomass allocation in the growth response of plants to different levels of light, CO2, nutrients and water: a quantitave review. Aust. J. Plant Physiol. 27:595-607. [ Links ]
Rodgers, H. L.; Brakke, M. P. and Ewel, J. J. 1995. Shoot damage effects on starch reserves of Cedrela odorata L. Biotropica. 27(1):71-77. [ Links ]
Rodríguez, G.; Morales, F.; Gutiérrez, R.; Aguilar, S. y Pérez, E. 2007. Generación de raíces transformadas de Agave salmiana Otto y su colonización por Glomus intraradices. Rev. Fitotec. Mex. 30(3):215-222. [ Links ]
Rodríguez-Petit, A.; Clavero, T. y Razz, R. 2003. Características de crecimiento de Acacia mangium Willd en condiciones de bosque seco tropical. Arch. Latinoam. Prod. Anim. 5(1):60-62. [ Links ]
Saito, K.; Suyama, Y. and Sato, A. 2004. Defoliation effects on the community structure of arbuscular mycorrhizal fungi based on 18S rDNA sequences. Micorrhiza. 14:363-373. [ Links ]
Shi, Z. Y.; Chen, Y. L.; Feng, G.; Liu, R. J.; Chritie, X. P. and Li, L. 2006. Arbuscular mycorrhizal fungi associated with the Meliaceae on Hainan island, China. Mycorrhiza. 16(2):81-87. [ Links ]
Smith, S. E. and Read, D. J. 1997. Mycorrhizal Symbiosis. Second edition. Academic Press. San Diego California, USA. 605 p. [ Links ]
Souza, O. F.; Saggin J. O. J.; Ribeiro da Silva, E. M. e Luís de Lima, W. 2006. Dependencia e resposta de mudas de cedro a fungos micorrízicos arbusculares. Pesq. Agropec. Bras. 41(1):77-84. [ Links ]
StatSoft, Inc. 2011. Statistica (Data analysis software system), version 10. www.statsoft.com. [ Links ]
Villar, R.; Ruiz-Robleto, J.; Quero, J. L.; Poorter, H.; Valladares, F. y Marañón, T. 2004. Tasas de crecimiento en especies leñosas: aspectos funcionales e implicaciones ecológicas. In: Valladares, F. Ecología del bosque mediterráneo en un mundo cambiante. Ministerio de Medio Ambiente, EGRAF, S. A., Madrid. 191-227 pp. [ Links ]
Wang, B. and Qiu, Y. L. 2006. Phylogenetic distribution and evolution of mycorrhizas in land plants. Mycorrhiza. 16: 299-363. [ Links ]














