I. Introducción
El término alimento funcional se define como “Alimentos que por virtud de la presencia de componentes alimentarios fisiológicamente activos proveen beneficios a la salud más allá de su valor nutritivo” (Academy of Nutrition and Dietetics, 2013). Algunos alimentos lácteos fermentados poseen diversos componentes con propiedades funcionales, que abarcan desde péptidos bioactivos, aminoácidos libres, ácidos orgánicos y vitaminas, hasta microorganismos probióticos (Melini et al., 2019). Estos últimos constituyen uno de los principales componentes funcionales contenidos en alimentos elaborados artesanalmente, que representan una forma accesible a la población de diversos países (Akabanda et al., 2014; Gallegos-Acevedo et al. 2019).
De acuerdo con la FAO/OMS (2002) el término probiótico define a “microorganismos vivos, que cuando son consumidos en cantidades adecuadas como parte de un alimento confieren beneficios al huésped”. El género Lactobacillus incluye más de 200 especies distribuidas en 15 grupos, clasificados de acuerdo con sus características genotípicas y fenotípicas; que destacan en importancia debido a sus capacidades metabólicas y su adaptabilidad a diferentes hábitats (Duar et al., 2017). Las pruebas de funcionalidad en este tipo de cepas son variables entre los diferentes estudios, sin embargo, en términos generales incluye: resistencia a pH y bilis, adhesión a células intestinales, producción de ácidos orgánicos, inhibición del crecimiento de bacterias patógenas, asimilación de prebióticos, entre otras (Vinderola et al., 2011).
Existe una gran diversidad de cepas de Lactobacillus disponibles en el mercado y algunas han sido evaluadas como probióticos en el tratamiento de diversas patologías, como: intolerancias alimentarias, inflamación, infecciones intestinales, diabetes, obesidad, entre otras; caracterizadas por un desbalance de las microbiota intestinal debido a alteraciones intestinales específicas de cada patología o de las modificaciones nutricionales particulares, que resultan en alteraciones inmunológicas, fisiológicas y metabólicas del huésped (Heeney et al., 2018; Wilkins et al., 2019). Se reporta que la suplementación de algunas cepas de Lactobacillus reduce los síntomas de estas enfermedades y mejora en la calidad de vida del individuo (Yu-Ling et al., 2019).
El uso de probióticos se ha extendido a la industria láctea como cultivos adjuntos, donde su participación metabólica secundaría al cultivo iniciador o dominante contribuye en la proteólisis de las proteínas de la leche, con efecto positivo en el incremento de aminoácidos libres y producción de compuestos volátiles durante la fermentación (Smit et al., 2005; Radeljević et al., 2013). Este proceso es realizado por un complejo sistema proteolítico cepa-específico, cuyas variantes fenotípicas en sus componentes comprende proteasas ancladas a pared celular, transportadores de aminoácidos y péptidos, así como peptidasas intracelulares, lo cual refleja en el impacto tecnológico de las cepas durante la producción de lácteos fermentados (Tagliazucchi et al. 2019). Sin embargo, a pesar la gran diversidad de cepas de Lactobcillus comerciales, los estudios que reportan el impacto metabólico durante la fermentación láctea son limitados a cierto número de cepas (Bintsis, 2018; Li et al. 2017; Linares et al., 2017; Zhou et al., 2019).
Debido a las aplicaciones antes señaladas, existen diversos criterios para evaluar el potencial funcional y tecnológico de las cepas, que abarca desde estudios in vitro, in vivo en modelos animales y humanos, hasta experimentos de escalamiento en planta piloto (Allam et al., 2016; Kumar et al., 2015; Rao et al., 2015). A pesar de que estos últimos representan una opción más acertada al comportamiento de microorganismos en un entorno real, los estudios in vitro proporcionan información preliminar sobre el potencial de las cepas bajo condiciones simuladas, representando una opción económica y confiable para la selección de cepas con potencial clínico y tecnológico.
El objetivo de este estudio fue evaluar propiedades tecnológicas y funcionales de cuatro cepas probióticas comerciales del género Lactobacillus, en términos de producción de aminoácidos libres totales, perfil de acidificación, consumo de glucosa y células viables, así como actividad antibacteriana contra patógenos Gram negativos, compatibilidad con cepas probióticas y asimilación de prebióticos.
II. Materiales
2.1 Microorganismos y condiciones de crecimiento
Las cepas de este estudio proceden de la colección American Type Culture Collection (ATCC), e incluye: una cepa de Lactobacillus acidophilus ATCC 4356 y tres pertenecientes al grupo L. casei: Lactobacillus casei ATCC 393, Lactobacillus paracasei ATCC 25302 and Lactobacillus rhamnosus ATCC 53103. Previo al estudio se evaluó compatibilidad entre cepas.
Para la prueba de actividad antimicrobiana se usó: Salmonella enterica subsp. enterica serovar Cholerasuis ATCC 10708, Salmonella entérica subsp. enterica serovar Enteritidis ATCC 1045 y Shiegella flexnerii ATCC 12022. En la prueba de compatibilidad con cepas probióticas se usó: Bifidobacterium adolescentis ATCC 15703, Bifidobacterium animalis ATCC 27530, Bifidobacterium bifidum ATCC 29521, Bifidobacterium breve ATCC 15700 y Bifidobacterium infantis ATCC 15707.
En todos los casos se usaron cultivos stock, los cuales se elaboraron a partir de cultivos axénicos de cada cepa colectados durante la fase exponencial. A partir de alícuotas de estos cultivos se obtuvo el paquete celular por centrifugación a 6000 rpm durante 5 min a 4 °C y se resuspendió al volumen inicial con medio líquido al 30 % de glicerol (v/v) (Sigma, USA), se almacenó a -80 °C para posteriores análisis. Para las cepas probióticas los medios empleados fueron agar y caldo De Man Rogosa and Sharpe (MRS; BD, USA). Para las cepas patógenas, se utilizó agar y caldo Nutritivo (BD, USA).
III. Métodos
3.1.1.1 Inóculo
Preinóculos de cada cepa de Lactobacillus fueron preparados colocando 10 ml de caldo MRS con 1 % (v/v) de cultivo stock e incubando a 37 °C bajo condiciones anaeróbicas hasta fase estacionaria. Posteriormente, el inóculo se preparó en 10 ml de caldo MRS con 1 % (v/v) del pre-inoculo e incubando a las mismas condiciones. A continuación, el paquete celular se sometió al lavado en dos ocasiones consecutivas con solución de fosfatos pH 7.0, se resuspendió al mismo volumen y se ajustó a 106 UFC.
3.1.1.2 Condiciones de fermentación
250 ml de caldo MRS modificado (se reemplazó la proteosa peptona por peptona de caseína; BD, USA) se esterilizaron por filtración con el uso de una membrana de 0.25 µm (Merck Millipore, USA) de acuerdo con Lee et al., (2014). Posteriormente se inoculó y se incubó a 37 °C bajo condiciones anaerobias y estáticas por 96 h. El experimento fue realizado por triplicado con tomas de muestras a 0, 12, 24, 48, 72 y 96 h.
3.1.2 Tratamiento de muestras
Para la determinación de aminoácidos, carbohidratos y ácidos orgánicos, se partió de las muestras fermentadas libres de células, tomando como control el medio sin fermentar. Para esto, se tomaron alícuotas de 1 ml de muestra y se trataron con igual volumen de acetonitrilo (Sigma, USA), con reposo de 12 h a 4 °C y posterior centrifugado a 13000 rpm por 5 min, de acuerdo con el procedimiento reportado por Polson et al. (2003). Posteriormente las muestras se liofilizaron y se resuspendieron al volumen inicial con agua ultrapura.
3.1.3 Determinación de aminoácidos libres totales
Las muestras se sometieron previamente a derivatización usando el kit Pico Taq (Waters Corp., Milford, MA, USA) de acuerdo con las recomendaciones del fabricante. La cuantificación se realizó con la determinación de los derivados de fenilisotiocianato generados a partir de los aminoácidos libres (Bidlingmeyer et al. 1984). La determinación se realizó mediante un cromatógrafo Agilent Technologies 1200 acoplado a un detector UV, con una columna C18 Pico-Tag (3.9 x 150 mm, 5 µm de tamaño de partícula; Waters, USA). Las condiciones de operación fueron: velocidad de flujo de 1.0 ml/min. Como disolvente A se usó ácido acético (Sigma, USA) 0.14 M pH 6.5 (Sigma, USA); como solvente B se usó acetonitrilo (Sigma, USA) en proporción 60:20 (v/v) en agua ultra-pura. La elución se realizó usando 96 % de A y 4 % de B durante 10 min. Posteriormente se lavó con 100 % de B. El volumen de inyección fue de 4 µl de las muestras. Para la cuantificación se empleó una mezcla estándar de aminoácidos H-estándar (Waters Corp., Milford, MA, USA), realizando una curva de calibración en concentraciones de 0, 50, 100, 200, 300, 400 y 500 pmol. La determinación se realizó a una longitud de onda de 240 nm. Los resultados se expresan en mg/l.
3.1.4 Perfil de acidificación
El perfil de acidificación consistió en determinar el pH y el contenido de ácidos orgánicos de cada muestra. La determinación de pH se realizó directamente en las muestras no tratadas, mientras que para la determinación de ácidos orgánicos se partió de alícuotas de 50 µl de muestra tratada, diluyendo en una proporción de 1:20 con agua ultra pura. Se determinó el contenido de ácido acético, propiónico, butírico y láctico mediante HPLC de acuerdo con el método propuesto por Al-Tamimi et al. (2006). El procedimiento incluyó una columna Aminex HPX-87H de intercambio iónico (300 x 7.8 mm, 9 µm de tamaño de partícula; Bio-Rad, Watford, Herts, UK) y como fase móvil H2SO4 5 mM previamente desgasificado. La velocidad de flujo utilizada fue de 0.6 ml/min, a temperatura de operación de 50 °C. La cuantificación se realizó con un detector UV a 220 nm, calibrando con los estándares en concentraciones entre 1-100 mM. El volumen de inyección fue de 10 µl. Los resultados se reportan en g/l.
3.1.5 Determinación del contenido de hexosas totales
El contenido de carbohidratos totales se realizó con el método propuesto por Trevelyan and Harrison (1956). Las muestras se diluyeron a 1 ml en proporción 1:50 en agua ultrapura, se adicionaron 5 ml de solución de antrona (5 % alcohol absoluto, 0.2 % de antrona, aforado con solución de ácido sulfúrico al 75 %) y se mantuvieron a 0 °C por 10 min. Posteriormente, las muestras se colocaron a 80 °C en baño maría durante 10 min, para finalmente almacenarlos a 0 °C. La cuantificación de carbohidratos totales se determinó mediante una curva de calibración utilizando soluciones de glucosa en concentraciones de 0, 20, 40, 60, 80, 100 µg/ml a 625 nm. Los resultados se reportan en g/l.
3.1.6 Determinación de células viables
Las células viables se determinaron realizando una serie de diluciones 1/10 (10-1 hasta 10-6) en solución de fosfatos pH 7.0. Se procedió a inocular 0.1 ml de cada una de las diluciones en placas con agar MRS (BD, USA), que se incubaron a 37 °C por 48 h. Los resultados se reportan en unidades formadoras de colonias por volumen de medio fermentado (UFC/ml).
3.2.1 Actividad antibacteriana
La prueba contra cepas patógenas Gram negativas se realizó de acuerdo con Vinderola et al. (2008). Para esto, cultivos axénicos en fase estacionaria de las cepas S. choleraesuis ATCC 10708, S. enteritidis ATCC 1045 y S. flexnerii ATCC 12022 se desarrollaron en Caldo Nutritivo (BD, USA) y se inocularon en agar Mueller-Hinton (BD, USA) a una temperatura de 45-50 °C, homogeneizando y vertiendo la suspensión celular en cajas de petri de 100 mm de diámetro, con ajuste del contenido celular a 106 UFC/ml. Posteriormente, se realizaron cuatro pozos de 9 mm de diámetro en cada placa de agar y fueron sellados en el fondo con 5 µl de agar estéril. Cultivos axénicos en fase estacionaria de cada cepa de Lactobacillus fueron centrifugados a 12000 rpm durante 5 min y se recuperó el sobrenadante. Cada muestra de sobrenadante libre de células se dividió en dos porciones, una fue neutralizada (con NaOH 5 M) y ambas fueron esterilizadas por filtración empleando una membrana de 0.25 µm. Volúmenes de 50, 100, 150, 200, 250 y 300 µl de cada sobrenadante fueron adicionados en los pozos en las cajas de petri inoculadas con cada cepa patógena. Como control se empleó caldo MRS estéril pH 6.5. Las condiciones de incubación fueron 37 °C, en anaerobiosis por 24 h y los halos de inhibición fueron registrados en mm posterior a la incubación.
3.2.2 Compatibilidad con cepas probióticas
La prueba se realizó por medio del ensayo por gota en agar suave MRS (0.7 % de agar) como reporta Ismail et al. (2016). Después de la solidificación del agar, gotas de 5 µl de cultivo axénico en fase estacionaria de cada cepa de Lactobacillus (106 UFC/ml) fueron depositadas sobre la superficie del agar previamente inoculado con cultivo axénico en fase estacionaria de cada una de las cepas probióticas (106 UFC/ml), las cuales se incubaron a 37 °C bajo condiciones anaeróbicas por 24 h. El efecto se evaluó después de la incubación, a través de la medición de las zonas de inhibición alrededor de la marca de crecimiento, los resultados son expresados subjetivamente en términos de capacidad inhibitoria a través de una escala hedónica de cuatro niveles de acuerdo con el diámetro de inhibición generado.
3.2.3 Capacidad de asimilación de prebióticos
Para esta prueba se evaluó la capacidad de asimilación de cuatro carbohidratos usados como prebióticos: rafinosa (Sigma, USA), lactulosa (Regulact, México), fructooligosacáridos (FOS, Raftilose_P95; Sigma, USA) e inulina de agave (Producto comercial, México), con el uso de glucosa como control. Se determinó el crecimiento mediante densidad óptica (OD600 nm) de muestras de caldo MRS modificado, con el reemplazo de la glucosa por el correspondiente prebiótico al 1 % (p/v). Posteriormente se inoculó al 1 % (v/v) de cultivo axénico en fase estacionaria de las cepas en estudio, sometidas a dos lavados consecutivos con solución de fosfatos pH 7 y se incubo a 37 °C bajo condiciones anaeróbicas. El crecimiento se determinó a intervalos de 3 h durante las primeras 24 h y posteriormente cada 24 h hasta alcanzar 96 h. Los datos se ajustaron a un modelo logístico no lineal y se determinó la velocidad específica de crecimiento (µ) (Likotrafiti et al., 2013).
3.3 Presentación de resultados y análisis estadísticos
Todos los resultados se expresaron como los valores promedio ± desviación estándar. En todos los análisis, se evaluó la normalidad de los datos y homogeneidad de varianza mediante las pruebas Shapiro y Levene respectivamente. Una vez cumplidas estas pruebas, se procedió al uso de la prueba paramétrica Análisis de Varianza (ANOVA) y comparación de medias por método de Tukey con α=0.05 con el uso del programa R (R: A lenguaje and environment for statistical computing Core Team 2013).
IV. Resultados y discusión
4.1 Propiedades tecnológicas
Todas las cepas alcanzaron la máxima población a las 24 h de fermentación, con una reducción de células viables en los tiempos posteriores (Figuras 1 a-d). La cepa L. casei presentó la mayor viabilidad al término de la fermentación (96 h) con 2.43 x 107 UFC/ml, una unidad logarítmica mayor respecto a L. paracasei ATCC 25302 y L. rhamnosus ATCC 53103, y dos unidades logarítmicas respecto a L. acidophilus ATCC 4356 (p < 0.05).

Figura 1. Variables cinéticas evaluadas en fermentación de medio MRS modificado incubado bajo condiciones anaeróbicas por 12, 24, 48, 72 y 96 h. Los valores iniciales de los parámetros cinéticos (tiempo 0) fueron: 105 - 106 UFC/ml, 20 g/l de glucosa, 0.88 g/l de ácido láctico, pH=6.5 y 980.74 mg/l de aminoácidos libres totales. Las cepas evaluadas fueron: a) L. acidophilus ATCC 4356, b) L. casei ATCC 393, c) L. paracasei ATCC 25302 y d) L. rhamnosus ATCC 52103. La información representa el promedio ± desviación estándar de tres experimentos independientes.
En los parámetros de consumo de glucosa y perfil de acidificación las cepas del grupo L. casei presentaron un patrón similar, con reducción total del contenido de glucosa a las 24 h de fermentación en contraste a L. acidophilus ATCC 4356, que presentó esta condición hasta las 96 h (p < 0.05). El perfil de acidificación generado por las cepas del grupo L. casei destacó con una máxima producción de ácido láctico (21 - 28 ± 0.7 g/l) y reducción de pH (3.5-3.6) posterior a las 24 h de fermentación (p < 0.05) (Figuras 1 a-d). Este comportamiento similar entre las cepas del grupo L. casei está determinado por la estrecha relación filogenética de las cepas de este grupo (Toh et al., 2013). Además, la reducción del contenido total de glucosa en el medio a las 24 h de fermentación y el incremento del contenido de ácido láctico se debe a su capacidad para catabolizar aminoácidos libres para obtención de energía (Liu et al., 2012). Adicionalmente, la cantidad de ácido láctico producido por las cepas del grupo L. casei superó en un 40-43 % a L. acidophilus ATCC 4356, así como a cepas de Lactococcus lactis subsp. lactis usadas en maduración de quesos bajo condiciones de fermentación in vitro similares a este estudio (Serna, 2006), y con similitud a cepas de L. casei, L. plantarum y L. delbrueckii aisladas a partir de diferentes fuentes (Sheeladevi and Ramanathan, 2011).
En la producción de aminoácidos libres totales (Figura 1a-d) la mayor producción estuvo representada por L. casei ATCC 393 y L. paracasei ATCC 25302, con un comportamiento similar al tiempo de 12 h (1180.7±24.4 - 1285.2±28.4 mg/l), lo cual representa un incremento del 17.1 - 23.9 % respecto al control (p < 0.05) (Figuras 1b-c). L. acidophilus ATCC 4356 registró in incremento constante durante el tiempo de fermentación, con un incremento máximo del 11.4 % (1103.5±29.6 mg/l) al término del proceso (p < 0.05) (Figura 1a). L. rhamnosus ATCC 53103 fue la cepa con menor producción (p < 0.05) (Figura 1d). La diferencia en la cantidad de aminoácidos producidos durante la fermentación podría explicarse por variaciones en los componentes de su metabolismo proteolítico, donde el tipo peptidasas intracelulares y sus mecanismos de regulación, así como las necesidades nutricionales debidas a las auxotrofías para los diferentes aminoácidos propios de cada cepa influyen en su liberación al medio (Altermann et al., 2005; Mozzi et al., 2010; Sasaki et al., 1995). El patrón similar entre las cepas L. casei ATCC 393 y L. paracasei ATCC 25302 sugiere la relación filogenética más estrecha (Toh et al., 2013).
Con excepción de L. rhamnosus ATCC 53103, cuya producción de aminoácidos libres fue constante a partir de las 12 h de fermentación, las demás cepas presentaron un incremento después de las 48 h, lo cual se relaciona con la lisis celular y liberación de peptidasas intracelulares, así como baja utilización de los aminoácidos del medio para crecimiento del cultivo debido a las condiciones desfavorables del medio. Este fenómeno es común en el proceso de maduración de quesos en donde la proteólisis secundaria por efecto de las peptidasas bacterianas libres favorece la liberación de aminoácidos a partir de los péptidos generados por la plasmina, al incrementar el tiempo de maduración (Hynes et al., 2003; Nateghi, 2012; Radeljević et al., 2013).
Por otra parte, en los perfiles de aminoácidos libres L. casei y L. paracasei presentaron la mayor producción a las 12 h de fermentación para los aminoácidos esenciales: Ile (85.6 ± 1.5 - 88.5 ± 2.1 m/l), Leu (194.9 ± 4.7 - 208.9 ± 5.1 mg/l), Lys (71.3 ± 3.1 mg/l), Met (37.2 ± 0.7 - 40.2 ± 1.3 mg/l), Phe (132.2 ± 3.4 - 141.3 ± 2.9 mg/l), Val (15.1 ± 0.9 - 15.8 ± 0.7 mg/l) e His (20.5 ± 0.7 - 21.9±0.6 mg/l), así como para los aminoácidos no-esenciales: Ala (61.7 ± 0.5 - 66.1 ± 1.3 mg/l), Arg (62.4 ±1.2 - 66.8±0.7 mg/l), Asp (67.3 ± 1.3 - 72.9 ± 0.5 m/l), Glu (104.7 ± 1.8 m/l), Tyr (61.8 ± 07 mg/l) (p ˂ 0.05). L. rhamnosus presentó la mayor producción para el aminoácido Gly (64.4 ± 1.2 - 70.6 ± 0.5 mg/l) entre las 24 y 72 h de fermentación, así como para el aminoácido Ser (39.6 ± 0.2 mg/l). Adicionalmente, esta cepa presentó alta producción para Lys (56.5 ± 1.6 mg/l) y Thr (83.6 ± 3.6 mg/l) a las 12 h de fermentación (p < 0.05). L. acidophilus incrementó la producción a las 96 h de fermentación para los aminoácidos Tyr (61.0 ± 0.9 mg/l), Ser (38.9 ± 0.5 mg/l) e Ile (75.6 ± 2.8 mg/l) (p < 0.05). Finalmente, todas las cepas presentaron incremento de Pro al término de la fermentación, destacando L. casei y L. acidophilus (156.7 ± 2.8 - 158.2 ± 1.9 mg/l) (p < 0.05) (Tabla 1 y 2). Los contrastes cuantitativos encontrados entre los perfiles de aminoácidos libres, se debe a variaciones en componentes del sistema proteolítico cepa-específico como reporta Settachaimongkon et al. (2014) para cepas de Streptococcus y Lactobacillus. El incremento en la disponibilidad de los aminoácidos esenciales: Ile, Leu, Val, Phe, Trp y Met, favorece la formación de α-ceto ácidos, alcoholes, aldehídos, ácidos carboxílicos y ésteres, cuyo perfil cualitativo y cuantitativo impactan las características distintivas a los productos lácteos fermentados (Smit et al., 2005). Así mismo, se reporta que la disponibilidad de Glu incrementa la eficiencia de reacciones de transaminación por la enzima glutamato deshidrogenasa presente en lactobacilli, lo cual favorece la formación de compuestos de sabor y aroma (Williams et al., 2006). Esto sugiere que las cepas de L. casei y L. paracasei evaluadas en este estudio presentan potencial uso como cultivos adjuntos, como se reporta para otras cepas de Lactobacillus en la producción de queso (Aljewicz et al., 2014; Peralta et al., 2016; Stefanovic et al., 2018).
Tabla 1. Perfil de aminoácidos esenciales producidos durante la fermentación de medio líquido MRS modificado incubado bajo condiciones anaerobias a 37°C por 96 h.
| Tiempo (h) | Cultivo | Contenido de aminoácidos (mg/l) | ||||||||
| Ile | Leu | Lys | Met | Phe | Thr | Trp | Val | His | ||
| 0 | C | 70.0±4.5bc | 168.5±11.8bc | 28.8±0.8hi | 36.3±1.7ab | 131.3±5.5bc | 53.1±2.5ef | 40.2±1.6ef | 12.3±0.7cd | 17.1±1.3de |
| 12 | LA | 67.6±0.5c | 160.6±3.5bc | 33.4±1.2gh | 31.6±0.4bc | 107.7±1.5cd | 45.7±0.8g | 35.9±1.7fg | 11.9±0.6cd | 14.7±0.8e |
| LC | 88.5±2.1a | 208.9±5.1a | 71.3±3.1a | 40.2±1.3a | 141.3±2.9a | 59.4±1.2de | 49.3±1.8cd | 15.1±0.9ab | 21.9±0.6a | |
| LP | 85.6±1.5ab | 194.9±4.7ab | 38.5±1.2ef | 37.2±0.7ab | 132.2±3.4ab | 55.5±1.6ef | 46.0±1.4de | 15.8±0.7a | 20.5±0.7ab | |
| LR | 66.9±1.3c | 166.2±4.9bc | 56.5±1.6b | 25.8±0.3cd | 102.9±1.9de | 83.6±3.6a | 56.5±2.5a | 10.8±0.3cd | 20.2±0.9ab | |
| 24 | LA | 69.0±1.3c | 160.4±3.8bc | 38.7±1.0ef | 31.4±1.8ab | 101.7±3.3ef | 42.8±1.3g | 34.7±1.4fg | 11.9±0.6cd | 13.3±0.6f |
| LC | 64.8±1-6c | 146.1±2.0c | 48.1±1.4bc | 23.2±0.7g | 89.2±1.6h | 60.4±1.9de | 47.2±0.9cd | 10.5±0.4d | 17.7±0.7cd | |
| LP | 70.1±1.1bc | 155.0±2.5c | 21.3±0.5k | 34.2±1.1ab | 128.3±4.3bc | 50.7±0.3fg | 36.3±0.9fg | 10.9±0.7cd | 17.2±0.2de | |
| LR | 66.2±1.4c | 143.3±1.7c | 52.5±1.2bc | 25.2±0.7ef | 98.9±2.9gh | 67.8±2.1b | 57.2±2.2a | 10.5±0.5d | 20.8±0.9ab | |
| 48 | LA | 70.5±1.8bc | 162.3±4.9bc | 35.9±1.2fg | 33.2±0.8b | 111.8±2.8cd | 47.5±1.5g | 35.5±0.9fg | 12.4±0.9bc | 15.5±0.6e |
| LC | 72.0±2.2bc | 140.7±3.2c | 35.3±1.4fg | 25.8±0.7cd | 100.2±1.5fg | 68.2±1.7b | 35.3±0.4fg | 10.9±0.7cd | 19.3±0.9bc | |
| LP | 68.3±1.6c | 136.8±2.5c | 22.1±0.7k | 30.9±0.9bc | 124.9±1.7bc | 49.7±0.6fg | 34.8±1.2fg | 11.3±0.5cd | 19.3±0.2bc | |
| LR | 64.9±2.5c | 152.5±3.8c | 45.2±0.9cd | 24.8±0.5ef | 101.3±2.5ef | 67.1±1.6b | 51.2±1.1bc | 10.5±0.9d | 19.2±0.8bc | |
| 72 | LA | 69.0±2.5c | 154.7±2.1c | 38.9±0.7ef | 32.3±1.1bc | 105.7±3.4de | 44.4±0.9g | 32.5±1.2fg | 12.2±0.6cd | 15.5±0.6e |
| LC | 72.8±1.7bc | 156.6±2.0c | 42.2±0.5de | 26.2±0.3cd | 103.1±2.6de | 64.8±1.3bc | 51.1±0.9bc | 11.1±0.4cd | 20.5±0.7ab | |
| LP | 69.1±0.9c | 154.4±2.5c | 25.9±1.1jk | 31.7±0.8bc | 127.2±1.6bc | 49.4±0.8fg | 41.8±0.6ef | 11.6±0.2cd | 19.6±0.8bc | |
| LR | 63.0±1.1c | 144.8±3.5c | 36.7±1.2ef | 24.1±0.7ef | 100.4±1.9fg | 62.8±1.5cd | 52.3±1.4ab | 10.2±0.3d | 19.2±0.5bc | |
| 96 | LA | 75.6±2.8bc | 153.8±2.4c | 27.3±1.5ij | 34.9±1.1ab | 131.7±3.8bc | 50.0±1.7fg | 40.4±1.1ef | 13.5±0.4bc | 17.7±0.8cd |
| LC | 71.3±2.6bc | 155.5±1.5c | 39.0±1.4de | 26.0±1.5cd | 98.2±2.7h | 62.5±2.3cd | 48.3±1.2cd | 11.3±0.7cd | 17.8±0.5cd | |
| LP | 69.2±1.7c | 154.2±2.9c | 20.6±0.7k | 32.5±0.9bc | 127.6±2.9bc | 49.8±1.4fg | 31.7±0.8g | 11.1±0.2cd | 19.9±0.4ab | |
| LR | 64.4±1.5c | 150.4±1.9c | 43.4±1.3cd | 25.5±1.4de | 97.0±2.6h | 64.1±1.2bc | 51.2±1.3bc | 10.5±0.5d | 18.8±0.7cd | |
† C: caldo MRS modificado sin fermentar (control), LA: L. acidophilus ATCC 4356, LC: L. casei ATCC 393, LP: L. paracasei ATCC 25302 y LR: L. rhamnosus ATCC 53103.
§ Los valores expresan el valor promedio ± desviación estándar de tres experimentos independientes. Diferentes superíndices indican diferencias significativas entre los valores promedios para cada cepa patógena evaluada a p < 0.05 mediante la prueba de Tukey.
Tabla 2. Perfil de aminoácidos no-esenciales producidos durante la fermentación de medio líquido MRS modificado incubado bajo condiciones anaerobias a 37°C por 96 h.
| Tiempo (h) | Cultivo | Contenido de aminoácidos no esenciales (mg/l) | ||||||||
| Ala | Asn | Arg | Asp | Gly | Glu | Pro | Tyr | Ser | ||
| 0 | C | 46.4±0.9 | 19.0±0.4ab | 53.1±1.1cd | 62.3±1.7cd | 40.5±0.7gh | 64.5±1.4f | 47.7±0.9k | 59.0±0.9bc | 27.6±0.6f |
| 12 | LA | 49.3±0.7bc | 16.6±0.3b | 46.6±0.1de | 25.5±0.8k | 33.8±0.4h | 76.2±0.5de | 81.3±2.1j | 48.7±0.8d | 31.4±1.4de |
| LC | 66.1±1.3a | 7.4±1.2de | 66.8±0.7a | 72.9±0.5a | 59.4±1.1cd | 104.7±1.8a | 115.6±1.5fg | 61.8±0.7a | 35.5±0.6cd | |
| LP | 61.7±0.5a | 12.9±0.1c | 62.4±1.2ab | 67.3±1.3ab | 55.4±0.7ef | 96.1±1.8cd | 107.9±2.3gh | 57.7±0.5bc | 33.1±0.1de | |
| LR | 55.1±0.1ab | 9.8±0.4d | 44.4±0.9e | 42.3±0.7hi | 52.6±0.2fg | 81.8±0.5de | 81.1±1.7j | 48.8±0.6d | 39.6±0.2a | |
| 24 | LA | 47.0±1.1bc | 19.3±0.6ab | 50.1±0.9de | 24.7±1.2k | 35.9±1.1h | 76.3±0.8de | 88.4±1.1j | 47.7±0.2d | 32.4±0.7de |
| LC | 44.3±0.2bc | 5.6±0.4ef | 39.8±0.6e | 39.4±0.9ij | 51.2±0.7fg | 91.3±0.3cd | 121.7±2.9de | 44.8±1.1d | 30.1±0.4de | |
| LP | 42.4±0.2c | 5.9±0.1e | 56.6±0.5bc | 50.5±1.8gh | 57.3±1.0de | 79.3±2.3de | 117.7±1.3ef | 54.4±2.4cd | 29.4±0.4de | |
| LR | 46.8±1.3 | 9.8±0.2d | 53.9±0.4cd | 65.8±1.3bc | 70.6±0.5a | 97.9±0.7bc | 93.7±2.8ij | 44.4±1.3d | 31.1±0.5de | |
| 48 | LA | 45.2±0.1bc | 20.3±1.0a | 56.3±0.6bc | 26.1±0.2k | 42.5±1.2gh | 79.8±1.3de | 106.4±3.2hi | 52.6±0.5cd | 36.8±1.6cd |
| LC | 46.1±0.5bc | 2.4±0.1h | 47.7±0.9de | 49.9±0.5gh | 61.0±0.2cd | 103.1±0.6a | 135.7±1.4b | 51.1±0.8cd | 34.3±0.7cd | |
| LP | 40.5±0.9c | 5.8±0.2ef | 56.5±0.3bc | 43.1±0.4hi | 59.6±0.2cd | 79.1±0.5de | 124.5±2.3cd | 54.2±0.6cd | 29.9±0.7de | |
| LR | 46.7±0.3bc | 9.3±0.1d | 50.5±0.6de | 54.8±0.5de | 64.4±1.2bc | 97.9±1.1bc | 102.1±1.4hi | 48.0±0.5d | 32.2±0.8de | |
| 72 | LA | 48.3±0.4bc | 20.1±0.6a | 52.2±0.2cd | 29.6±0.3jk | 45.7±0.1gh | 89.0±0.6cd | 110.2±2.7gh | 50.6±0.4cd | 37.5±0.4bc |
| LC | 45.0±0.7bc | 3.0±0.1fg | 48.0±0.5de | 58.1±0.7de | 68.2±0.4ab | 101.2±0.3ab | 154.0±2.9a | 53.5±1.2cd | 34.1±0.5cd | |
| LP | 44.5±0.7bc | 8.0±0.3de | 50.7±1.6de | 50.7±0.1gh | 61.7±0.8cd | 98.7±1.3bc | 130.8±1.7bc | 60.2±0.1ab | 31.1±0.9de | |
| LR | 45.2±1.1bc | 9.8±0.4d | 51.1±1.0de | 55.0±0.3de | 67.0±0.9ab | 97.5±1.1bc | 107.5±3.2gh | 47.2±0.4d | 31.9±0.7de | |
| 96 | LA | 46.0±0.5bc | 21.2±0.3a | 54.6±1.9cd | 32.4±0.1jk | 52.8±1.6fg | 93.5±1.8cd | 158.2±1.9a | 61.0±0.9a | 38.9±0.5ab |
| LC | 45.7±0.7bc | 2.8±0.1gh | 48.5±0.4de | 53.4±0.9fg | 61.8±1.1cd | 108.8±1.0a | 156.7±2.8a | 50.8±1.2cd | 35.2±0.6cd | |
| LP | 44.9±0.6bc | 7.9±0.1de | 51.4±0.7de | 50.2±0.9gh | 62.4±0.1cd | 100.1±0.6bc | 129.2±3.6bc | 55.6±0.4cd | 31.5±0.4de | |
| LR | 47.2±0.5bc | 9.7±0.4d | 48.5±1.2de | 54.5±0.5ef | 61.4±0.4cd | 95.7±1.4cd | 111.2±1.5gh | 45.0±1.2d | 31.9±0.9de | |
† C: caldo MRS modificado sin fermentar (control), LA: L. acidophilus ATCC 4356, LC: L. casei ATCC 393, LP: L. paracasei ATCC 25302 y LR: L. rhamnosus ATCC 53103.
¶ El aminoácido Gln no fue detectado, mientras que para Cys el contenido fue 0 en todas las muestras.
§ Los valores expresan el valor promedio ± desviación estándar de tres experimentos independientes. Diferentes superíndices indican diferencias significativas entre los valores promedios para cada cepa patógena evaluada a p < 0.05 mediante la prueba de Tukey.
4.2.1 Actividad antibacteriana y compatibilidad con cepas probióticas
La evaluación de la capacidad antagónica de las cepas de Lactobacillus contra patógenos Gram negativos reveló que el sobrenadante libre de células neutralizado no presentó efecto inhibitorio, mientras que el sobrenadante no neutralizado libre de células presentó el mayor efecto inhibitorio a volúmenes ≥ 200 µl. L. paracasei ATCC 25302 presentó la mayor inhibición contra S. cholerasuis and S. flexnerii (p < 0.05), mientras que L. rhamnosus ATCC 53103 contra S. enteritidis (p < 0.05) (Tabla 1). Estos resultados coinciden con los reportados para otros estudios, donde revelan que la producción de ácidos orgánicos representa el mecanismo principal de inhibición de patógenos y corresponde al mecanismo principal de regulación de la microbiota intestinal (Belicová et al., 2013; Naidu et al., 2012; Zhang et al., 2011). Así mismo, el efecto letal de los ácidos orgánicos radica en su forma no disociada, la cual difunde pasivamente a través de la membrana, alterando el gradiente electroquímico y permeabilidad de la membrana celular, y cuya concentración depende del pH del medio, lo cual correlaciona con el sobrenadante no neutralizado libre de células (Bae and Lee, 2015).
Tabla 3. Actividad antimicrobiana contra bacterias Gram negativas de sobrenadante libre de células de medio MRS fermentado por cultivos axénicos de cepas de Lactobacillus.
| Volumen (µL) | Diámetro de zonas de inhibición (mm) | |||||||||||
| L. acidophilus | L. casei | L.paracasei | L. rhamnosus | |||||||||
| SF | SE | SC | SF | SE | SC | SF | SE | SC | SF | SE | SC | |
| 50 | 0g | 0i | 0f | 0g | 0i | 0f | 0g | 0i | 0f | 0g | 0i | 0f |
| 100 | 0g | 0i | 0f | 0g | 0i | 0f | 0g | 0i | 0f | 0g | 0i | 0f |
| 150 | 0g | 0i | 0f | 0g | 0i | 0f | 12.1±0.2d | 10.6±02g | 10.9±06e | 10.1±0.3g | 12.1±04e | 0f |
| 200 | 0g | 0i | 0f | 12.1±0.1d | 11.2±01f | 0f | 12.4±0.1cd | 13.0±06e | 11.4±02d | 12.1±0.1d | 14.9±01c | 11.6±03de |
| 250 | 0g | 10.4±04h | 11.6±0.2d | 12.8±0.6c | 13.8±04d | 0f | 14.6±0.3b | 14.5±04c | 14.8±03b | 14.3±0.3b | 15.7±02b | 11.5±02de |
| 300 | 10.9±2e | 10.5±03h | 11.9±0.1d | 14.1±0.2b | 14.9±01c | 10.9±2e | 15.5±0.4a | 14.6±02c | 15.9±01a | 14.4±0.4b | 16.5±01a | 13.2±01c |
† SF: Shigella flexnerii ATCC 12022; SE: Salmonella enteritidis ATCC 1045; SC: Salmonella cholerasuis ATCC 10708.
¶ pH y contenido de ácido láctico de sobrenadante libre de células no neutralizado (mg/100 µL): caldo MRS sin fermentar (control) pH=6.5 y 0.08±0.00; L. acidophilus ATCC 4356 pH=4.27 y 1.02±0.01; L. casei ATCC 393 pH=3.82 y 1.90±0.01; L. paracasei ATCC 25302 pH=3.72 y 2.12±0.01; L. rhamnosus ATCC 53103 pH=3.71 y 2.18±0.01.
§ Los valores expresan el valor promedio ± desviación estándar de tres experimentos independientes. Diferentes superíndices indican diferencias significativas entre los valores promedios para cada cepa patógena evaluada a p < 0.05 mediante la prueba de Tukey.
Por otra parte, la prueba de compatibilidad entre cepas probióticas reveló que las cepas de Lactobacillus son compatibles entre ellas y con cepas probióticas del género Bifidobacterium, con ausencia de halos de inhibición en el agar MRS, lo cual debe a mecanismos de ambos géneros bacterianos que involucran: recambio de lípidos con incremento en la rigidez e impermeabilidad de membrana citoplasmática, excreción de protones por medio de ATPasas, producción intracelular de aminoácidos de cadena ramificada (Ile, Leu y Val) y amonio (Papadimitriou et al., 2016; Ruíz et al., 2011). Esto resalta su potencial en aplicaciones clínicas y tecnológicas debido a que Lactobacillus y Bifidobacterium forman parte de la microbiota intestinal normal del ser humano, lo cual representa bajo riesgo en mecanismos inhibitorios o de competencia contra cepas comensales del huésped (Mueller et al., 2015). Adicionalmente, la compatibilidad entre cepas podría sugerir su aplicación como cultivos mixtos en la producción de alimentos lácteos fermentados (Rosa do Carmo et al., 2017).
4.2.2 Asimilación de prebióticos
De las cepas evaluadas, L. acidophilus ATCC 4356 presentó la mayor capacidad de asimilación de prebióticos, con velocidades específicas de crecimiento de 0.68, 1.01 y 0.61 para lactulosa, rafinosa y FOS respectivamente (p < 0.05) (Figura 2a y Tabla 4). El pH resultante de la fermentación de estos sustratos fue similar al control y osciló entre 4.2 y 4.3 al término de la fermentación (96 h) (p < 0.05). Las cepas L. casei ATCC 393, L. paracasei ATCC 25302 y L. rhamnosus ATCC 53103 mostraron baja densidad óptica y ligero cambio de pH en los prebióticos mencionados (p < 0.05) (Figuras 2b-d y Tabla 2). Estos resultados corresponden a los reportados por Altermann et al. (2005) y Figueroa-González et al. (2019) que refieren baja capacidad de asimilación de lactulosa y FOS por cepas de L. casei y L. rhamnosus, en contraste a L. acidophilus. El medio con inulina de agave comercial produjo baja densidad óptica y escasa acidificación para todas las cepas de Lactobacillus (p < 0.05) (Figuras 2a-d y Tabla 4), lo cual indica escasa asimilación del carbohidrato, que es contrario a lo reportado por Kaplan and Hutkins (2000), Cai et al. (2007) y Velázquez-Martínez et al. (2014) para cepas de L. casei y L. paracasei, pero similar respecto a L. acidophilus y L. rhamnosus. Es importante destacar que las variaciones metabólicas observadas están determinadas por sus características genotípicas específicas particulares de cada cepa, las cuales están determinadas por las condiciones ambientales del hábitat del microorganismo (Altermann et al., 2005). Finalmente, la importancia de la asimilación de prebióticos radica en el diseño de productos simbióticos comerciales (probiótico + prebiótico), en los cuales se incluye el sustrato para promover el crecimiento del probiótico específico. Esto sugiere que la cepa L. acidohilus evaluada en este estudio presenta versatilidad los sustratos utilizados, lo cual sugiere una ventaja competitiva contra microorganismos comensales y patógenos dentro del tracto gastrointestinal, representando un mecanismo de acción importante en los microorganismos probióticos (Dicks and Botes, 2010).
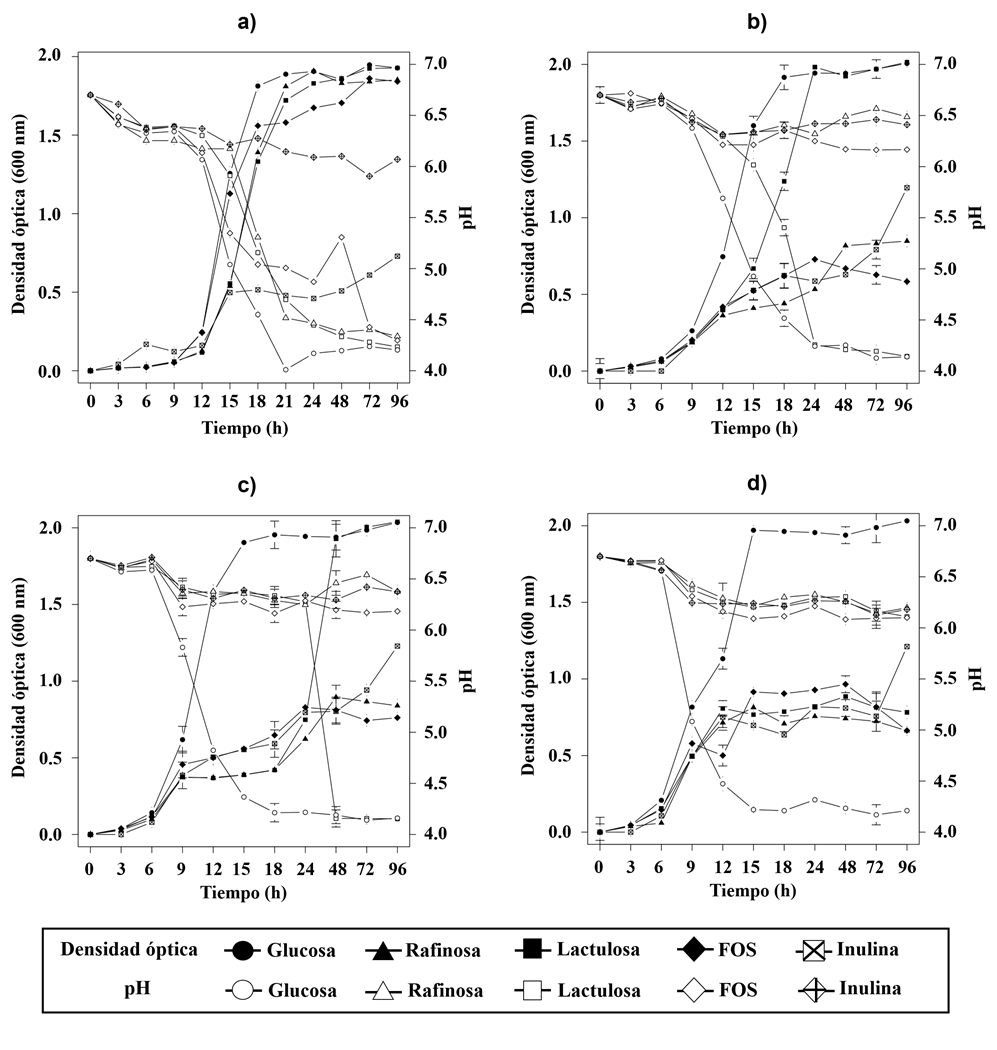
Figura 2. Cinética de crecimiento y cambio de pH de las cepas: a) L. acidophilus ATCC 4356, b) L. casei ATCC 393, c) L. paracasei ATCC 25302 y d) L. rhamnosus ATCC 52103, durante la fermentación de medio MRS modificado (reemplazo de glucosa por prebiótico al 1 % (p/v) incubado a 37 °C durante 96h. Los símbolos rellenos corresponden a la medición de la absorbancia y los símbolos vacíos a las mediciones de pH. Los valores expresan el valor promedio ± desviación estándar de tres experimentos independientes.
Tabla 4. Velocidad específica de crecimiento de cepas de Lactobacillus determinadas en fermentación de MRS modificado suplementado con prebióticos.
| Cepas | Prebióticos | ||||
| Glucosa | Rafinosa | Lactulosa | FOS | Inulina | |
| µ (h-1) | µ (h-1) | µ (h-1) | µ (h-1) | µ (h-1) | |
| LA | 0.45±0.01 | 1.01±0.00* | 0.68±0.03* | 0.61±0.03* | 0.40±0.03 |
| LC | 0.69±0.02 | 0.14±0.01 | 0.11±0.00 | 0.29±0.01 | 0.19±0.00 |
| LP | 0.83±0.02 | 0.64±0.01 | 0.57±0.00 | 0.70±0.02 | 0.26±0.02 |
| LR | 0.58±0.03 | 0.15±0.00 | 0.35±0.01 | 0.41±0.00 | 0.25±0.01 |
† LA: L. acidophilus ATCC 4356, LC: L. casei ATCC 393, LP: L. paracasei ATCC 25302, LR: L. rhamnosus ATCC 52103.
* Indica significancia en la velocidad específica de crecimiento (µ) respecto al control a p < 0.05 aplicando la prueba de Tukey. Los valores indican el promedio ± desviación estándar de tres experimentos independientes.
V. Conclusión
Los resultados obtenidos sugieren que las cepas evaluadas presentan potencial aplicación como cultivos adjuntos en la elaboración de alimentos lácteos fermentados con propiedades funcionales. La cepa L. casei y L. paracasei destacaron en la producción de aminoácidos libres con incremento en la disponibilidad de aminoácidos esenciales, los cuales favorecerían en valor nutrimental y propiedades sensoriales del alimento fermentado. Así mismo, estas cepas junto con L. rhamnosus presentaron mayor efecto antibacteriano contra patógenos Gram negativos, lo cual proveería al consumidor un efecto protector contra infecciones intestinales y agregaría al producto la propiedad funcional. Finalmente, L. acidophilus, resultó en mayor capacidad de asimilación de prebióticos, que podría resultar en una ventaja tecnológica en el diseño de productos simbióticos. Finalmente, todas las cepas fueron compatibles con cepas probióticas de Bifidobacterium, que podría representar una ventaja en el diseño de cultivos mixtos.











 nueva página del texto (beta)
nueva página del texto (beta)


