Introducción
La peritonitis secundaria es una afección frecuente en la práctica quirúrgica general1. Resulta sumamente difícil hacer una estimación de la incidencia anual de la sepsis abdominal por la gama tan amplia de patologías que pueden llegar a desarrollarla (apendicitis, úlceras gástricas, enfermedad diverticular complicada, etc.). Dicha diversidad en enfermedades hace que el abordaje quirúrgico y terapéutico carezca de uniformidad2.
Una vez practicada una laparotomía para resolver el foco séptico, se presenta uno de los principales retos: ¿el proceso séptico está controlado?, ¿será necesaria una nueva laparotomía? Por lo anterior, es indispensable contar con estrategias que permitan responder estas incógnitas con el objetivo de disminuir la morbilidad y la mortalidad asociadas a la sepsis grave y al choque séptico de origen abdominal, optimizar los medios de tratamiento disponibles (resultando en una disminución de los costos para las instituciones de salud) y finalmente tratar de homogeneizar cuándo y en qué paciente debe plantearse una nueva intervención quirúrgica por persistencia o desarrollo de un evento de sepsis abdominal3. Las dos principales estrategias de reintervención en la sepsis de origen abdominal son la laparotomía exploradora a demanda y la programada. Aunque ninguna de las dos ha llevado a una disminución en la mortalidad general de dichos pacientes, cuando se opta por una estrategia en la que el deterioro clínico o la falta de mejoría del individuo en cuestión normará la conducta quirúrgica (a demanda) sí impacta de manera positiva en los costos institucionales, los días de estancia en terapia intensiva, la duración de la ventilación mecánica asistida y el número de intervenciones. Sin embargo, algunas intervenciones resultarán blancas (sin hallazgos que justifiquen el procedimiento quirúrgico), por lo que es importante definir que parámetros clínicos y paraclínicos deben tomarse en cuenta para normar la decisión de reintervenir quirúrgicamente a un paciente, con la máxima sensibilidad y especificidad posibles para disminuir los falsos positivos, impactando principalmente en la mortalidad de esta patología4.
Van Ruler, et al.5 informaron en 2008 los resultados de un cuestionario que pedía a los cirujanos que clasificaran la importancia de 21 variables clínicas en su decisión de volver a operar en pacientes con peritonitis secundaria. Descubrieron que la extensión difusa de la contaminación abdominal, la localización del foco infeccioso (tracto gastrointestinal superior, incluido el intestino delgado) y el recuento de leucocitos extremadamente bajo o alto predijeron de forma independiente una nueva laparotomía. Estas variables solo tenían una moderada precisión predictiva. Los resultados del cuestionario demostraron que no hubo consenso entre los cirujanos sobre qué variables son importantes en el proceso de toma de decisiones para la nueva laparotomía. La decisión final de realizar una nueva operación en un paciente en la configuración bajo demanda suele basarse en la respuesta séptica generalizada de los pacientes y en la falta de mejoría clínica5.
En México y en el mundo no existe un consenso o índice predictivo para los cirujanos que pueda determinar la necesidad de realizar una relaparotomía en pacientes operados que desarrollan sepsis abdominal. Esta investigación pretende aplicar un modelo de variables basado en la escala propuesta por Kiewiet-Van Ruler para la necesidad de una nueva laparotomía en pacientes mexicanos con diagnóstico de sepsis de origen abdominal sometidos a una laparotomía como parte de su manejo.
Método
Estudio retrospectivo, observacional, correlacional, analítico, transversal, en pacientes operados por la clínica de urgencias de sepsis del Hospital General de México Dr. Eduardo Liceaga entre enero de 2013 y mayo de 2015, con diagnóstico de sepsis de origen abdominal, que fueron sometidos a laparotomía exploradora. La muestra es de 109 pacientes que se reoperaron, ya sea a demanda o programados, de los que se contaba con los datos de las seis variables del modelo de Kiewiet-Van Ruler posterior a la primera cirugía, tomando como controles a aquellos pacientes que no tuvieron hallazgos significativos en la segunda cirugía y como casos a todos los pacientes con hallazgos de importancia, es decir, aquellos en los que era absolutamente necesaria una nueva intervención para el control del foco infeccioso.
Resultados
De la muestra total de 109 pacientes que contaban con las seis variables posoperatorias del modelo de Kiewiet-Van Ruler, 63 (57.8%) eran de sexo masculino y 46 (42.2%) de sexo femenino. El 83.5%, correspondiente a 91 pacientes, se mantuvieron con vida y presentaron mejoría, mientras que 18 (16.5%) fallecieron durante el periodo estudiado. Todos los pacientes de la muestra fueron reintervenidos. En 98 pacientes (90.7%) se realizó la nueva intervención con la modalidad a demanda, mientras que en 11 (10.2%) se realizó la modalidad programada. Los órganos lesionados con mayor frecuencia en la primera intervención fueron el apéndice (41%), el intestino delgado (22%), el colon (15.6%) y la vía biliar (8.3%). La presencia de líquido purulento fue predominante en los hallazgos quirúrgicos, con un 59.6% (65 casos), seguido del intestinal en el 19.3% (21 casos) y del seroso en el 11% (12 casos); solo en el 7.3% (8 casos) no se evidenció líquido libre. El tiempo medio para buscar atención médica fue de 4.85 días (desviación estándar: 5.06).
El 88.9% de los pacientes que requirieron aminas en el posoperatorio necesitaron reoperación, mientras que el 31% de los pacientes que no emplearon aminas precisaron reoperación. Al aplicar a estos datos la prueba exacta de Fisher se obtuvo un valor de p = 0.001. Al estudiar la estimación del riesgo se obtuvo un valor de razón de momios (OR) de 17.806, con un intervalo de confianza del 95% (IC 95%) de 2.13 a 148,58, lo que representa un factor de riesgo (Fig. 1).

Figura 1 Relación entre el puntaje de Kiewiet-Van Ruler y las aminas. En el gráfico se aprecia que los casos que requirieron aminas tuvieron puntajes de Kiewiet-Van Ruler más altos.
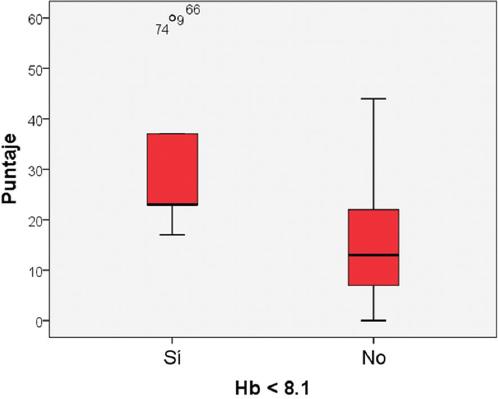
En cuanto al descenso de la hemoglobina posoperatoria, lo presentaron 15 pacientes, y de estos el 40% requirieron reoperación, mientras que de los casos que no mostraron descenso de la hemoglobina requirieron reoperación el 35.1%. Al aplicar la prueba estadística ji al cuadrado a estos datos se obtuvo un valor de p = 0.713 (Fig. 2).
En relación a la taquicardia (frecuencia cardiaca > 90 latidos por minuto) y la reoperación, se observó que, de 77 pacientes que presentaron taquicardia en el posoperatorio, el 42.9% requirieron reoperación, mientras que de los pacientes sin taquicardia el 18.8% necesitaron reoperación. Al aplicar la prueba ji al cuadrado se obtuvo un valor de p = 0.017, y al evaluar la OR para estos datos se obtuvo un valor de 3.25 (IC 95%: 1.20-8.79) (Fig. 3).
Respecto de la obstipación (falta de evacuaciones intestinales) posoperatoria y la necesidad de reoperación, de 19 casos que presentaron obstipación el 63.2% requirieron reoperación, mientras que de 90 casos que no presentaron obstipación el 30% necesitaron reoperación. Lo anterior, sometido a la prueba ji al cuadrado, arroja un valor de p = 0.06, y al evaluar la OR para estos datos se obtiene un valor de riesgo de 4 (IC 95%: 1.42-11.26) (Fig. 4).
El cuadro de peritonitis difusa o generalizada es un caso especial en la positividad de la variable, pues es la única en que se hace mención a los hallazgos transoperatorios en la primera cirugía, y se presentó en 79 casos; de estos, el 44.3% requirieron reoperación, mientras que de los 30 casos que no tuvieron peritonitis difusa el 13.3% necesitaron reoperación. Al aplicar la prueba exacta de Fisher se obtuvo un valor de p = 0.03, estadísticamente significativo, mientras que al evaluar la OR se obtuvo un valor de 5.17 (IC 95%: 1.65-16.20) (Fig. 5).

Figura 5 Relación entre el puntaje Kiewiet-Van Ruler y el hallazgo de peritonitis difusa o generalizada en la cirugía inicial.
Al estudiar la asociación entre las variaciones de la temperatura en el posoperatorio se aprecia que, de 35 casos que tuvieron alteraciones de la temperatura, el 54.3% requirieron reoperación, mientras que el 20% de los que no tuvieron alteración de la temperatura necesitaron reoperación. La prueba de ji al cuadrado arroja un valor de p = 0.006, y al evaluar la OR para estos datos se obtiene un valor de 3.20 (IC 95%: 1.38-7.42) (Fig. 6).
Al construir la curva ROC para el puntaje de la escala Kiewiet-Van Ruler, considerando la necesidad de reoperación, obtuvimos un área bajo la curva de 0.733, estadísticamente significativa (0.001; IC 95%: 0.637-0.828). Se estableció el mejor punto de corte en 15 puntos, con una sensibilidad del 60% y una especificidad del 64.3% (Fig. 7).
Al evaluar la asociación del puntaje de Kiewiet-Van Ruler, con un corte a 20 puntos, con la necesidad de reoperación, se observó que de 41 casos que presentaron un puntaje > 20 el 53.7% requirieron reoperación, mientras que de los 68 que tuvieron puntajes < 19 el 25% necesitaron reoperación. Al someter estos datos al estadístico ji al cuadrado se obtuvo un valor de p = 0.002, y al evaluar la OR para estos datos se obtuvo un valor de 3.47 (IC 95%: 1.52-7.91) (Tabla 1).
Tabla 1 Puntaje de Kiewiet-Van Ruler>20 y reoperación
| Sí | Reoperación | Total | |
|---|---|---|---|
| Sí | No | ||
| Puntaje | |||
| > 20 | 22 | 19 | 41 |
| 53.7% | 46.3% | 100.0% | |
| < 19 | 17 | 51 | 68 |
| 25.0% | 75.0% | 100.0% | |
| Total | 39 | 70 | 109 |
| 35.8% | 64.2% | 100.0% | |
Tomando como punto de corte 40 puntos para la escala de Kiewiet-Van Ruler observamos que, de cinco pacientes que presentaron un puntaje > 40, el 100% requirieron reoperación, mientras que de 104 casos con puntajes < 39 necesitaron reoperación el 32.7%. Al someter estos datos a la prueba exacta de Fisher se obtuvo una p = 0.005, estadísticamente significativa, y al evaluar la OR se obtuvo un valor de 3.059 (IC 95%: 2.322-4.030) (Tabla 2).
Discusión
En el estudio realizado por Kiewiet-Van Ruler, et al.6 se propone un índice de seis variables con resultados esperanzadores para la predicción de la necesidad de relaparotomía. En los pacientes que obtuvieron más de 40 puntos, el valor predictivo negativo para la relaparotomía fue del 42%, mientras que los que obtuvieron 60 puntos presentaron un 83% de posibilidad de relaparotomía. Al aplicar el modelo a nuestra población se obtuvieron resultados similares: en el corte de 20 puntos la sensibilidad mostrada fue del 53% y la especificidad fue del 61%, con un valor predictivo negativo aceptable, el cual aumenta conforme disminuye el puntaje; sin embargo, los pacientes que se ubicaron entre 20 y 40 puntos se encuentran en una situación incierta, pues los valores predictivos positivo y negativo del índice no resultaron significativos, por lo que, en concordancia con los autores del modelo ya comentado, sugerimos la complementación del protocolo con un estudio tomográfico, con la finalidad de incrementar tanto la sensibilidad como la especificidad diagnóstica, evitando así la realización de laparotomías blancas o el retraso de la atención quirúrgica7.
La decisión basada en la clínica y en estudios de gabinete para reintervenir a un paciente tiene una tasa poco aceptable, siendo que uno de cada tres pacientes podría no haber requerido el evento quirúrgico. Hutchins, et al.8 realizaron una comparación del tiempo de demora para identificar a pacientes que requieren una reintervención mediante la clínica contra la identificación utilizando el índice ARPI (Abdominal Reoperation Predictive Index) propuesto por Pusajo, et al., y obtuvieron resultados interesantes, ya que el tiempo de atención se redujo de 7.9 días en promedio con diagnóstico clínico a 5.7 días en promedio utilizando la escala de ARPI9.
La utilidad del modelo propuesto por Kiewiet-Van Ruler en población mexicana se comprobó de forma satisfactoria, resultando en un aceptable valor de predicción para relaparotomía, pero aún lejos de la sensibilidad y la especificidad ideales, motivo por el cual es de gran importancia recalcar que este modelo no planea sustituir al actual método de referencia, como la tomografía contrastada y la evaluación clínica del paciente; sin embargo, el nomograma realizado puede ayudar a elegir adecuadamente a aquellos pacientes en los que se realizarán estudios de extensión.
De acuerdo con los resultados obtenidos, también se propone el uso de este modelo como un primer paso en la valoración posoperatoria de los pacientes con sepsis abdominal, de manera que si se obtienen menos de 15 puntos en el modelo podemos concluir que la probabilidad de que el paciente requiera una segunda intervención es baja (63% de especificidad), fenómeno que varía notablemente si incrementamos el punto de corte a 40 puntos, perdiendo sensibilidad y especificidad. Debido a esto, es de interés para investigaciones a futuro realizar una comparativa del modelo de Kiewiet-Van Ruler aunado a estudios de imagen u otras escalas de falla orgánica, como ARPI, SOFA (Sequential Organ Failure Assessment) y APACHE II (Acute Physiology And Chronic Health Evaluation II), entre otras, lo cual idealmente incrementaría el sustento estadístico de este modelo en puntajes elevados, pero también perdería la facilidad de reproducción y los pocos recursos utilizados para la evaluación, que son objetivo clave en el apoyo al modelo. Como segunda medida, para aquellos pacientes con puntajes entre 20 y 40 puntos se puede recalcular la escala 12 horas después de la evaluación inicial, con lo cual la variación de los puntajes indicaría la conducta más correcta a seguir tomando en consideración que con estos valores se pueden obtener hasta un 25-34% de laparotomías negativas si no se realiza ningún estudio de extensión.
Por último, debido a que el modelo de Kiewiet-Van Ruler fue creado específicamente para predecir la necesidad de relaparotomía en pacientes operados de sepsis abdominal, al igual que el índice ARPI, sería de gran interés e importancia clínica a futuro el poder comparar dichos modelos y así aplicarlos de manera sistemática en la atención de la peritonitis secundaria.
Conclusión
La utilidad del modelo propuesto por Kiewiet-Van Ruler resulta en un aceptable valor de predicción para la relaparotomía, lo que junto con la evolución clínica, el criterio quirúrgico y los exámenes de gabinete permite una decisión más acertada, evitando cirugías innecesarias y permitiendo intervenciones en tiempos óptimos, mejorando la morbilidad y la mortalidad. En nuestra población, el mejor punto de corte se sitúa en 15 puntos.











 nueva página del texto (beta)
nueva página del texto (beta)