Introducción
El glicocálix endotelial se observó por primera vez por Luft utilizando microscopia electrónica. Desde su descubrimiento, surgió el interés de descubrir su papel fisiológico. Comenzó con la observación de glicocálix en hematocrito a través de un tubo capilar hasta modernas técnicas actuales de reconstrucción en tercera dimensión y el uso de diferentes técnicas de microscopia electrónica; desde entonces, múltiples hallazgos indican una variedad de funciones fisiológicas endoteliales y su participación activa en las patologías vasculares. Esta revisión proporciona información sobre la composición y funciones del glicocálix endotelial y su participación en diversas enfermedades como diabetes, isquemia/reperfusión, aterosclerosis, con especial énfasis en la sepsis.
Estructura del glicocálix
El glicocálix endotelial es una estructura compleja rica en proteoglicanos y glicoproteínas que recubre el endotelio vascular, el endocardio y los vasos linfáticos. El glicocálix está formado por componentes del plasma relacionados entre sí de una manera directa o a través de proteoglicanos y/o glucosaminoglicanos. La eliminación enzimática de cualquiera de sus constituyentes afecta drásticamente las propiedades del glicocálix, por lo que es de gran importancia considerar la interacción sinérgica de todos sus componentes. Cuando existe degradación del glicocálix, se altera la permeabilidad endotelial y el flujo sanguíneo microcirculatorio.1
Los constituyentes del glicocálix son los siguientes:
1) Proteoglicanos
Los proteoglicanos son generalmente considerados la «columna vertebral» del glicocálix. Se componen de un núcleo proteico al que una o más cadenas de glucosaminoglicanos están vinculadas. Los proteoglicanos como sindecán, glipicán y perlecán son los principales componentes de esta columna vertebral a la cual se unen las cadenas de glucosaminoglicanos; esto conduce a la producción de proteoglicanos solubles, que residen en el glicocálix.2
Hay cinco proteoglicanos solubles que se encuentran en esta red: sulfato de heparán, sulfato de condroitina, sulfato de dermatano, sulfato de queratán y ácido hialurónico, que son polímeros lineales de disacáridos con longitudes variables modificados por sulfatación y/o acetilación. Los disacáridos están compuestos cada uno de un ácido hialurónico y una hexosamina; su clasificación depende de su integración con ácido hialurónico, hexosamina y sulfatación.3
El heparán sulfato representa aproximadamente 50-90% de la cantidad total de proteoglicanos presentes en el glicocálix; el segundo glucosaminoglicano más común en el glicocálix es el sulfato de condroitina, que se encuentra en una relación 4:1 con heparán sulfato en el endotelio vascular.4 Otro glucosaminoglicano importante en el glicocálix es el ácido hialurónico, cuya característica estructural es una molécula polimérica larga (104 kDa); difiere de otros glucosaminoglicanos porque no se une a una proteína núcleo. Su relación exacta con la membrana celular es desconocida; se presume un enlace al receptor CD44 y una unión por proteínas (hialuronanosintasas) que se encuentran en el citosol de la membrana celular. Otras uniones se han identificado como Cdc37 y P32. El heparán sulfato, el sulfato de condroitina y el sulfato de dermatán se sintetizan en el retículo endoplásmico y aparato de Golgi de la célula endotelial, produciendo una traducción de proteína ribosomal; una xilosiltransferasa transferirá xilosa (Xyl) de uracildifosfato xilosa a residuos específicos de serina (Ser) en la proteína del núcleo.5,6
Las cadenas de glucosaminoglicanos contienen múltiples sitios de unión para proteínas derivadas del plasma; pequeñas modificaciones pueden tener grandes consecuencias funcionales.7 La diversidad de los patrones de sulfatación de glucosaminoglicanos, el efecto sobre proteína de unión específica y la modulación de la función de las proteínas sugieren que las condiciones que disminuyen el espesor del glicocálix regulan los patrones de sulfatación de glucosaminoglicanos específicos de proteínas, susceptibles de modificar la permeabilidad vascular y alterar la proteína específica de unión y su actividad.8,9
2) Glicoproteínas
Además de los proteoglicanos, con sus largas cadenas laterales lineales, ciertas glicoproteínas también se consideran parte de la «columna vertebral» del glicocálix. Este grupo de glicoproteínas endoteliales se caracterizan por un número relativamente pequeño (2-15 residuos de azúcar) y cadenas laterales de hidratos de carbono ramificadas. Su principal función es el reclutamiento celular desde el torrente sanguíneo y la señalización celular. Las tres familias de moléculas de adhesión de células presentes en los glicocálix endoteliales son la familia de selectinas, integrinas y las inmunoglobulinas. Las glicoproteínas de la familia de las selectinas contienen dominio en el citoplasma, un dominio transmembrana (dominio similar al factor epidérmico) y un dominio de lectina terminal, que es el principal responsable de la unión de grupos carbohidrato a proteínas glicosiladas o lípidos.10
La E-selectina y P-selectina se encuentran en el endotelio vascular; ambas están implicadas en interacciones endoteliales, almacenando cuerpos de Weibel-Palade de las células endoteliales, y determinan la exocitosis de cuerpos de Weibel-Palade inducida por estímulos tales como la trombina y la histamina, permitiendo una rápida translocación de P-selectina en la superficie celular.11,12 E -selectina no se almacena en gránulos, pero requiere de novo de ARNm y la síntesis de proteínas que se expresa en la superficie celular. La estimulación endotelial celular por citocinas como la interleucina-1, factor de necrosis tumoral α y lipopolisacárido expresan E-selectina.13 En algunos tejidos como la piel aparecen P y E-selectina, que se expresan constitutivamente en las células endoteliales.14
Las integrinas son moléculas heterodiméricas que poseen dos subunidades (α y β). Se han identificado 18 diferentes subunidades α y β, lo que significa que cada integrina se caracteriza por la combinación específica de sus subunidades.15 Las integrinas se encuentran en muchos tipos de células, incluyendo las células endoteliales, leucocitos y plaquetas. En las membranas luminales de células endoteliales se expresan integrinas v3, que son importantes mediadores de la interacción de células endoteliales-plaquetarias. Las integrinas (α2β1, α5β1 y α6β1) se unen a la matriz extracelular, responsables de las interacciones con laminina, fibronectina y colágeno. Muchos estudios se han centrado en las interacciones entre estas integrinas y la matriz subendotelial durante la angiogénesis.16,17
La superfamilia de las inmunoglobulinas de glicoproteínas se caracteriza por su dominio transmembrana, citoplasmático y un número variable de dominios de inmunoglobulina a nivel luminal. Los ejemplos más conocidos son molécula de adhesión intercelular 1 y 2 (ICAM-1 y 2), molécula de adhesión celular vascular 1 (VCAM-1) y moléculas de adhesión celular endotelial a plaquetas 1 (PECAM-1), que actúan como ligando para las integrinas en leucocitos y plaquetas, siendo mediadores cruciales de leucocitos al endotelio. ICAM-1 y 2 y PECAM-1 tienen una expresión lineal, mientras que la VCAM-1 se expresa tras la estimulación de células endoteliales por citocinas, que también aumenta la expresión de ICAM-1. El papel de ICAM-2 en la inflamación todavía no está claro; recientemente, se demostró que la ICAM-2 se involucra en la regulación de la angiogénesis.18,19
Además de las moléculas de adhesión celular, el glicocálix alberga glicoproteínas con funcionalidad en la coagulación, la fibrinólisis, y la hemostasia. Un buen ejemplo es el complejo glicoproteína Ib-X-V, que se expresa en células endoteliales y plaquetas. Se compone de cuatro glicoproteínas: Ibα, Ibβ, IX y V, que son polipéptidos. Las glicoproteínas Ibα y Ibβ se unen covalentemente a través de un grupo disulfuro, mientras que IX y V se unen de forma no covalente al heterodímero Ib. El complejo Ib-IX-V se une al factor de von Willebrand (vWF). Además, el complejo se une también a P-selectina, mediando la interacción de las plaquetas con las células endoteliales activadas. Al igual que las plaquetas, las células endoteliales expresan todos los componentes del complejo Ib-IX-V, que permiten la unión sulfato y fvW al subendotelio y hacen posible la unión de cuerpos de Weibel-Palade a células endoteliales activadas.20
3) Componentes solubles
Existen componentes solubles de diversos tipos dentro de los componentes de proteoglicanos y glicoproteínas, tales como proteínas y proteoglicanos solubles; éstos se obtienen del endotelio o desde el torrente sanguíneo (albúmina y orosomucoide); son clave en la preservación de la selectividad (carga) en la permeabilidad de la barrera. Los componentes solubles del glicocálix contribuyen en gran medida a su importancia funcional, organización estructural y estabilidad luminal. Aun así, el glicocálix es una capa delicada, y la eliminación de un componente concreto puede resultar en pérdida de la función total (Figura 1).21,22
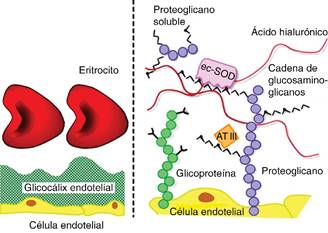
Figura 1: Representación gráfica del glicocálix mostrando sus componentes principales. Del lado izquierdo observamos la célula endotelial y cómo el glicocálix forma esta red que protege del contacto con los eritrocitos. Del lado derecho de la figura se observan los componentes estructurales del glicocálix, los proteoglicanos, con sus cadenas unidas de glucosaminoglicanos y glicoproteínas, además de componentes solubles unidos como la antitrombina III (ATIII) y proteínas extracelulares, ácido hialurónico y superóxido dismutasa (ec-SOD).
Importancia funcional
El glicocálix endotelial es un determinante importante de la permeabilidad vascular; es capaz de limitar el acceso de ciertas moléculas de la membrana celular endotelial, como se ha demostrado en las pequeñas arterias mesentéricas de rata con el uso de dextranos marcados con fluorescencia de varios pesos moleculares, mostrando el aumento de permeabilidad de moléculas más pequeñas. El glicocálix media transportes enzimáticos y funciona como barrera permeable.23
El modelo conocido como «cruce-break» aplica el mecanismo de Starling sobre el glicocálix y describe sus efectos sobre los solutos y el transporte de agua a través del endotelio. La importancia del glicocálix endotelial en el control de la extravasación de coloides y líquidos se hizo evidente por los estudios de Rehm y colaboradores, que identificaron deterioro de la función endotelial después de la degradación del glicocálix en un modelo de corazón no perfundido; sin embargo, después de 20 minutos de isquemia aguda, sólo la albúmina impidió la fuga vascular.24,25
Además de su capacidad para restringir moléculas, influye en la interacción de la pared de los vasos mediando células rojas, plaquetas y leucocitos, albergando moléculas de adhesión y atenuando las mismas. Por lo tanto, en condiciones normales, las cadenas de glucosaminoglicanos y los componentes solubles del glicocálix parecen proteger la adhesión molecular. Los estímulos que degradan el glicocálix o inducen una integración en su estructura más abierta, tales como enzimas, citocinas, isquemia y reperfusión, aumentan las moléculas de adhesión, que a su vez, permiten interacción celular con el endotelio, alterando las microvellosidades del glicocálix y su membrana.26
La presencia de un glicocálix endotelial relativamente grueso in vivo tiene ventajas para la reología, especialmente en la microvasculatura. En esta parte de la circulación, la viscosidad de la sangre local y el hematocrito parecen estar modulados por el glicocálix. Con el uso de un modelo físico basado en mediciones de hematocrito en microvasculatura in vivo, Pries y Secomb demostraron recientemente que la incorporación de estimaciones del glicocálix a nivel mesentérico aumenta al doble la viscosidad.1,27
1) Glicocálix endotelial como mecanotransductor
El endotelio se expone a fuerzas mecánicas inducidas por el flujo sanguíneo. Desde hace tiempo, se ha reconocido que estas fuerzas, en particular, el estrés y fuerzas de cizallamiento, determinan la morfología y funcionalidad de células endoteliales. Las células endoteliales expuestas a tensión producen óxido nítrico (ON), que es un determinante importante del tono vascular. Sin embargo, las moléculas responsables de la traducción de fuerzas biomecánicas en señales bioquímicas (mecano-transductores) no han sido identificadas aún. Recientemente, el glicocálix ha sido añadido a la lista de posibles candidatos.28
De acuerdo con estudios experimentales, se ha determinado que el heparán sulfato y hialuronato parecen jugar un papel en la detección y amplificación de las fuerzas de cizallamiento inducidas por el flujo. A partir de estos datos, parece probable que el glicocálix determine un papel importante en la mecanotransducción. Los diferentes componentes del glicocálix probablemente operan juntos, lo que significa que el glicocálix, como un todo, es responsable de su papel como mecanotransductor. Recientemente, Tarbell y Pahakis proponen conceptos actuales sobre mecanotransducción por glicocálix y llegan a la conclusión de que las proteínas del núcleo glicocálix son responsables de la transmisión de las señales de estrés y cizallamiento en los procesos específicos de señalización celular, por ejemplo, la producción de ON y la reorganización del citoesqueleto; al mismo tiempo, la tensión de cizallamiento se transmite a otras regiones de las células endoteliales, así como en uniones intercelulares y placas de adhesión.29,30
2) Glicocálix endotelial como centro de control para el microambiente
Los proteoglicanos en el glicocálix contribuyen en gran medida a su importancia funcional. El acoplamiento de moléculas derivadas del plasma puede influir en el medio ambiente local de varias maneras: 1) la unión de receptores enzimáticos y sus ligandos al glicocálix endotelial induce un aumento de la concentración de estas sustancias, permitiendo la señalización adecuada o modificación enzimática mediada por factor de crecimiento de fibroblastos (FGF); 2) la unión de moléculas derivadas del plasma puede llevar a una concentración local de gradiente, que se ve a menudo en el gen del factor de crecimiento, regulando procesos de transcripción y desarrollo; 3) importantes mediadores anticoagulantes pueden unirse al glicocálix, tales como la antitrombina III, el cofactor de heparina II, trombomodulina y el factor inhibidor del factor tisular (FIFT). La antitrombina III es un fuerte inhibidor de las enzimas procoagulantes como la trombina y los factores IX y X activados (FIXa y FXa). Se sabe que se unen a regiones específicas de heparán sulfato, con lo que mejora su actividad anticoagulante. La trombomodulina es una proteína que contiene sulfato de condroitina expresado por células endoteliales, capaz de convertir trombina a partir de un procoagulante a un activador de la vía de la proteína C. FIFT es un inhibidor potente de FVIIa y FXa. Se cree que el FIFT se une al glicocálix a través de heparán sulfato. Todas estas moléculas anticoagulantes presentes en el glicocálix contribuyen a la naturaleza tromborresistente del endotelio sano. El glicocálix endotelial también modula las respuestas inflamatorias de las citocinas y su unión, atenuando las mismas para receptores de superficie celular.31,32,33
Otro aspecto de la función vasculoprotectora del glicocálix endotelial es su capacidad para unirse a inactivadores de radicales de oxígeno, tales como la superóxido dismutasa extracelular (SOD). Estas enzimas ayudan a reducir el estrés oxidativo y mantener la biodisponibilidad de ON.34
Fisiopatología
En los vasos sanos, el glicocálix endotelial determina la permeabilidad vascular, atenúa interacciones en las paredes celulares, media la tensión, señalización y cumple un papel vasculoprotector. Cuando se interrumpen, modifican o pierden estas propiedades, tiene un papel decisivo en diversas enfermedades caracterizadas por grave disfunción endotelial, de las que destacan la diabetes mellitus, isquemia/reperfusión, aterosclerosis y la sepsis.
1) Diabetes
Recientemente, se demostró que el volumen de glicocálix en voluntarios sanos, tal como se evaluó mediante la comparación de la distribución intravascular del glicocálix, se redujo a la mitad (en un periodo de seis horas) tras la inducción de hiperglucemia aguda. Usando la misma metodología, el volumen de glicocálix sistémico en diabéticos tipo 1 se encontró disminuido en relación con controles sanos, mostrando aun más reducción en diabéticos con microalbuminuria. En el mismo estudio, los niveles plasmáticos de ácido hialurónico y hialuronidasa fueron elevados en los pacientes con diabetes, lo que refleja el aumento de la síntesis y excreción de ácido hialurónico bajo condiciones de hiperglucemia. Ambos trabajos muestran que la hiperglucemia aguda y crónica se asocia con reducción profunda de dimensiones del glicocálix. Se requiere de más estudios para investigar si la disrupción del glicocálix es responsable de complicaciones en la microvasculatura en la diabetes.1,35
2) Isquemia/reperfusión
El daño a los tejidos durante un periodo de disminución de flujo (isquemia total o parcial) puede ser paradójicamente amplificado por la restauración del flujo sanguíneo (reperfusión). Aunque la gravedad de los daños resultantes de la isquemia/reperfusión varía entre los tejidos, un componente común de este proceso patológico para todos los órganos es la disfunción microvascular. Las células endoteliales sufren un aumento del estrés oxidativo, especialmente en vénulas postcapilares, generando adhesión leucocitaria y aumentando la permeabilidad vascular. Los efectos endoteliales de la isquemia/reperfusión alteran de manera directa el glicocálix endotelial y, por lo tanto, la función del mismo.31,36,37
Mulivor y Lipowsky demostraron recientemente que la isquemia/reperfusión intestinal lleva a una significativa reducción del espesor del glicocálix en vénulas mesentéricas en ratas debido a lesión de las cadenas de glucosaminoglicanos. Los efectos de la isquemia/reperfusión en el glicocálix podrían ser atenuados mediante el bloqueo de la xantina-oxidorreductasa, que es una especie de oxígeno reactivo endógeno (ROS), enzima unida a la producción de dominios de heparán sulfato en el glicocálix. De esta manera, juega un papel central (ROS) en la interrupción de agresión al glicocálix en la isquemia/reperfusión. La infusión de ácido hialurónico exógeno para restaurar el glicocálix o la administración de la toxina de la tosferina inhiben la proteína G, que resulta en lesión de las cadenas de glucosaminoglicanos.4,38
3) Aterosclerosis
La aterosclerosis es una enfermedad de arterias de gran calibre; típicamente se requieren altos niveles plasmáticos de LDL para su desarrollo. Se caracteriza por perfiles de flujo alterados, retención subendotelial de lipoproteínas aterogénicas y respuestas inflamatorias posteriores conduciendo a formación de placas subendoteliales. Se ha demostrado en estudios experimentales que a través de infusiones intravenosas de LDLOx en ratas se genera una disminución de 60% del diámetro del glicocálix. Igualmente, en estas especies se han estudiado regiones más susceptibles a la aterosclerosis, como la bifurcación de la carótida -que posee un glicocálix más delgado-, a diferencia de la carótida común, que tiene un menor potencial de lesión. Estos datos sugieren que el glicocálix endotelial está involucrado en el inicio y progresión del proceso aterosclerótico.8,39,40,41
4) Sepsis
La sepsis es una de las principales causas de ingreso a las unidades de terapia intensiva, alcanzando tasas de mortalidad de 50%. Se considera una respuesta compleja a la infección que involucra alteraciones microcirculatorias, inflamatorias y metabólicas que de no revertirse evolucionan a disfunción orgánica múltiple. El conocimiento del glicocálix y el endotelio, y su relación con la respuesta inflamatoria, es fundamental en el manejo del paciente séptico.
La respuesta inflamatoria en la sepsis se caracteriza por una activación endotelial sostenida y un desequilibrio entre mediadores pro- y antiinflamatorios. Las células endoteliales activadas cambian de un fenotipo quiescente (anticoagulante, antiadhesivo, vasodilatador) a uno activado (procoagulante, proadhesivo, vasoconstrictor), donde ocurren cambios estructurales y funcionales que tienen como fin eliminar al agente patógeno, pero que contribuyen simultáneamente al desarrollo de disfunción orgánica al generar daño en otros tejidos.
Al activarse las células endoteliales, disminuyen la síntesis de trombomodulina, del activador de plasminógeno tisular y de heparán sulfato. Al mismo tiempo, se presenta un incremento en la expresión del factor tisular en la superficie de macrófagos que lleva a la activación de la vía extrínseca de la cascada de coagulación y su posterior amplificación por la vía intrínseca. La activación de esta última incrementa la producción de citocinas y aumenta la expresión de moléculas de adhesión. Por otra parte, se presenta una marcada disminución de la actividad anticoagulante (proteína C, antitrombina III y trombomodulina), lo que favorece el perfil procoagulante del estado séptico. Estos mecanismos fisiopatológicos son amplificados por el proceso de isquemia/reperfusión (Figura 2).
Las citocinas proinflamatorias favorecen la permeabilidad endotelial y la pérdida de la función de barrera del endotelio mediante la degradación del glicocálix. El adelgazamiento de éste por activación de proteasas, como metaloproteinasas de la matriz (MMP), expone moléculas de adhesión en la superficie de las células endoteliales que permiten la migración de leucocitos, el reclutamiento de plaquetas y la amplificación de la respuesta inflamatoria.42,43,44
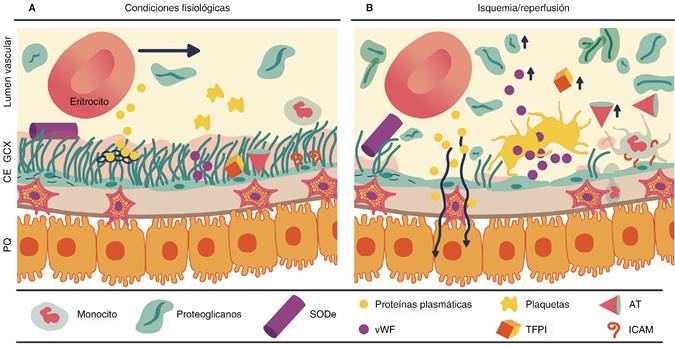
Figura 2: El glicocálix (GCX) en condiciones fisiológicas y fisiopatológicas inducidas por isquemia/reperfusión. A) Funciones protectoras del GCX, que incluyen: mantener la homeostasis y el tono vascular, regulando fuerzas mecánicas como el estrés y cizallamiento que conducen a la liberación de óxido nítrico (ON) por las células endoteliales; actuar como barrera antioxidante al unirse a la enzima superóxido dismutasa extracelular (SODe), limitar el acceso de macromoléculas a través de la membrana endotelial, inhibir vías procoagulantes mediante la antitrombina (AT) y el inhibidor de la vía del factor tisular (TFPI), y contrarrestar la inflamación al inhibir la expresión de ligandos de leucocitos como las moléculas de adhesión vascular (VCAM) y las moléculas de adhesión intercelular (ICAM). B) Degradación oxidativa del GCX: durante la isquemia/reperfusión, se transforma el endotelio en una superficie proinflamatoria. Se altera la producción de ON, lo que resulta en vasoconstricción y daño oxidativo. Se pierde el balance oncótico por la extravasación de macromoléculas, y ocasiona edema. Se exponen moléculas de adhesión VCAM/ICAM y factor de von Willebrand (vWF), que inducen agregación plaquetaria y migración leucocitaria. PQ = parénquima; CE = células endoteliales.
Varios estudios han evaluado la degradación de los componentes del glicocálix (vía heparinasa dependiente del factor de necrosis tumoral alfa) y, con esto, los niveles plasmáticos de sindecano-1 y glucosaminoglicanos (heparán sulfato) en pacientes sépticos, demostrando una relación directamente proporcional entre la concentración de éstos y la severidad de la sepsis. En uno de estos trabajos, se encontró que los individuos con sepsis grave tenían niveles de sindecano-1 más elevados que los grupos control y que esto correlacionaba con el incremento de marcadores inflamatorios como la interleucina-1 y las moléculas de adhesión.45,46
La evidencia clínica y experimental ha demostrado que la integridad del glicocálix endotelial se deteriora bajo condiciones inflamatorias, lo que sugiere su preservación como objetivo terapéutico. Si bien el pronóstico de los enfermos con sepsis ha mejorado durante las últimas décadas, las estrategias terapéuticas continúan limitándose a un adecuado soporte hemodinámico y al control microbiológico de los sujetos. Hasta el momento, ninguna intervención ha demostrado influir en el proceso de disfunción endotelial que fundamentalmente caracteriza a la sepsis.47,48
Al igual que las intervenciones encaminadas a mejorar la función endotelial en sepsis han sido fútiles, tampoco se ha impactado de manera significativa en la estructura y función del glicocálix. Los esteroides, al disminuir la respuesta inflamatoria, pudiesen mejorar la función del endotelio y su glicocálix. Esto se ha inferido de investigaciones en donde se ha demostrado que disminuyen la microalbuminuria que se presenta en la sepsis, lo que puede ser representativo de una mejor función del endotelio y glicocálix glomerular. Otras alternativas que se han explorado como preservadoras del glicocálix son la antitrombina y la proteína C activada, pero no causaron impacto en los estudios clínicos controlados, por lo que su actividad para preservar la estructura del glicocálix se vio rebasada. Un trabajo mostró que los efectos antioxidantes de la N-acetilcisteína pueden evitar la lesión del glicocálix y preservar la función endotelial. A pesar de los intentos realizados, se requieren más estudios que evalúen otras estrategias para mantener la función del glicocálix en sepsis.35,49
Conclusión
El glicocálix es fundamental para mantener la integridad de la función endotelial. Sus modificaciones estructurales y disfunción impactan en la perfusión microcirculatoria y la función del endotelio. En el enfermo grave, diferentes mecanismos fisiopatológicos alteran esta importante estructura, lo que se traduce en incremento de la permeabilidad capilar y disfunción microcirculatoria y celular.











 nueva página del texto (beta)
nueva página del texto (beta)


