Introducción
Existen distintas opciones de programas de entrenamiento en las que se enseñan a los profesionales de la salud las destrezas necesarias para llevar a cabo reanimación cardiopulmonar avanzada; uno de los más conocidos es el curso ACLS impartido por la American Heart Association (AHA).
Recientemente han sido publicadas las actualizaciones a las guías del 2015 en las que se destaca la trascendencia de realizar compresiones efectivas con una frecuencia de al menos 100 por minuto, pero menos de 120, con una profundidad de 5 centímetros, permitiendo la relajación completa del tórax y minimizando las interrupciones. Así mismo, se hace énfasis en distinguir entre ritmos desfibrilables (fibrilación ventricular, taquicardia ventricular sin pulso) y no desfibrilables (asistolia y actividad eléctrica sin pulso, AESP); la desfibrilación es el manejo de la primera categoría, mientras que en la segunda, éste se basa en RCP de alta calidad, administración temprana de adrenalina e identificación de la causa del paro.1
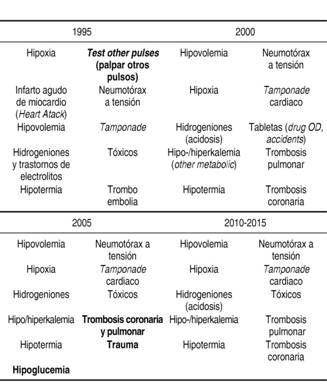
Para facilitar el abordaje de la etiología del paro, Kloeck propuso en 1995 la mnemotecnia de las H y T,2 que ha sido modificada a través de los años de acuerdo a las guías que son publicadas cada cinco años por la AHA (Cuadro I).
El objetivo del presente artículo es hacer una revisión sobre cuándo sospechar, cómo diagnosticar y cómo tratar cada una de las causas de asistolia y actividad eléctrica sin pulso. Es indiscutible que la historia clínica del paciente y la exploración física previa al paro son de suma importancia para sospechar alguna causa. Sin embargo, no siempre el paro cardiorrespiratorio es presenciado. De esta manera, abordaremos factores que deben ser investigados durante el paro y acciones a tomar en los cuidados postparo.
Hipovolemia
La disminución del volumen intravascular conduce a trastorno de la difusión y entrega de oxígeno, lo que es igual a hipoperfusión tisular; de no ser identificada y tratada de manera temprana, llevará a falla circulatoria irreversible.3
En caso de hemorragia masiva externa, es fácil identificar hipovolemia como causa del paro. Las decisiones de brindar RCP en un paciente de trauma se abordan en programas como PHTLS o ATLS.4 Por otro lado, puede coexistir hipovolemia asociada a otros cuadros clínicos y no siempre es sencillo identificarla. La depleción de volumen resulta de pérdida de sodio y agua de alguno de los siguientes sitios anatómicos:5
Gastrointestinal: vómito, diarrea, sangrado del tubo digestivo o drenajes en pacientes postquirúrgicos.
Pérdidas renales: diuréticos, diuresis osmótica, nefropatías perdedoras de sal e hiperaldosteronismo.
Pérdidas tegumentarias: sudoración intensa, quemaduras.
Pérdidas a tercer espacio: oclusión intestinal, lesión por aplastamiento, fracturas y pancreatitis aguda.
Dentro de los datos clínicos que se pueden evidenciar antes del paro se encuentran turgencia de piel disminuida, hipotensión ortostática, cambio postural en la frecuencia cardiaca (> 30 lpm), disminución del tono ocular, sequedad de las mucosas.6 En cuanto a laboratorios, podemos encontrar elevación de la cifra de creatinina, BUN, hiper- o hiponatremia, hiper- o hipokalemia, acidosis metabólica o alcalosis metabólica. Cuando la hipovolemia es muy severa, se presentará estado de choque, manifestado comúnmente con taquicardia, hipotensión, taquipnea, oliguria, diaforesis, estado neurológico alterado.7
Durante las maniobras de RCP se puede realizar un reto de líquidos administrando de 500 a 1,000 cm3 de solución cristaloide.8 En estos casos, el uso de un acceso intraóseo es de suma importancia, ya que durante el paro no se recomienda colocar accesos vasculares centrales y, por otro lado, canalizar una vía periférica de buen calibre (14-16 fr) es sumamente complicado, mientras que a través de un calibre pequeño (20-22 fr) no es posible administrar líquidos con una adecuada velocidad.
En la etapa de cuidados postparo nos podemos valer de herramientas de monitoreo hemodinámico donde variables como presión venosa central (PVC), variabilidad del volumen sistólico, variabilidad de presión de pulso, gasto cardiaco, índice cardiaco, entre otras, son de suma utilidad para sospechar déficit de líquidos.9 Así mismo el ultrasonido con ventana cardiaca o de vena cava brindará más datos para identificar hipovolemia y valorar si el individuo es respondedor a líquidos (Figura 1).

Figura 1: Esquemas de hallazgos por USG en hipovolemia, tamponade y TEP. Nótese que el esquema está diseñado para ultrasonido. Si se utiliza ecocardiograma, la imagen se deberá visualizar en espejo. (Traducido y publicado con la autorización de Antonios Likourezos, uno de los autores de “CAUSE: Cardiac arrest ultra-sound exam. A better approach to managing patients in primary non arrythmogenic cardiac arrest”).41
Hipoxia
Fisiológicamente, son cinco los mecanismos que condicionan hipoxia:10
Disminución de la presión inspiratoria de oxígeno: esto ocurre en hipoxemia de grandes alturas o en ambiente con FiO2 menor al 21%, como en espacios confinados.
Hipoventilación: depresión respiratoria del tronco encefálico (fármacos, síndrome de hipoventilación alveolar central), neuropatía periférica (síndrome de Guillain Barré), debilidad muscular (hipofosfatemia, miastenia grave).
Trastornos de la difusión: alteración en la membrana alveolocapilar. Ocurre en casos como asbestosis, sarcoidosis, fibrosis intersticial, neumonía intersticial, esclerodermia, enfermedades reumatológicas con repercusión pulmonar como lupus eritematoso sistémico o enfermedad de Wegener.
Desequilibrio de la relación V/Q: incremento del espacio muerto en casos de enfisema, gasto cardiaco bajo o hiperdistensión alveolar.
Aumento de los cortocircuitos pulmonares: ocupación alveolar por secreciones o agua (neumonía o edema agudo pulmonar), colapso alveolar como en caso de atelectasias masivas.
Para la sospecha de hipoxia se debe indagar acerca del estado anterior del sujeto para asociar el cuadro clínico previo con alguna de las condiciones mencionadas. Dentro de las herramientas más utilizadas para valorar la oxigenación se encuentra la oximetría de pulso; sin embargo, tiene sus limitaciones, como son desplazamiento de la curva de disociación de la hemoglobina, dishemoglobinemias, estado de hipoperfusión, anemia, esmalte de uñas, artefactos por movimiento, entre otras.11 Por lo anterior, debemos recalcar que la utilidad de la oximetría de pulso durante el paro cardiorrespiratorio es totalmente obsoleta: lo recomendable es utilizar la monitorización de onda de capnografía.
El manejo de la ventilación durante las maniobras de RCP debe ser siempre con oxígeno a altos flujos. La intubación endotraqueal se recomienda sólo si no se logra adecuada expansión torácica abriendo la vía aérea con mecanismos manuales o supraglóticos. Sin embargo, si existe un experto en el equipo de reanimación, se debe realizar la intubación cuanto antes.8
En los cuidados postparo se deberá llevar a cabo una minuciosa exploración física, se solicitará gasometría arterial y radiografía de tórax; con esto se valorará de manera más estrecha el estado pulmonar y de oxigenación para tomar decisiones de los parámetros ventilatorios, requerimiento de FiO2 o necesidad de realizar maniobras de reclutamiento alveolar para mejorar la oxigenación.12
Hidrogeniones
Para citar los motivos más frecuentes de acidosis, primero debemos clasificarlos en brecha aniónica elevada y brecha aniónica normal. Dentro del primer grupo encontramos como causas cetoacidosis diabética, acidosis urémica y acidosis láctica, así como tóxicos (metanol, etanol acetaldehído, salicilatos). Dentro de las razones de brecha aniónica normal se encuentra la acidosis hiperclorémica, que comúnmente se asocia a pérdidas extrarrenales de bicarbonato, como en caso de evacuaciones diarreicas abundantes.13
Para el abordaje de los trastornos ácido-base será indispensable contar con una gasometría, que durante la RCP puede ser tomada de la arteria femoral. Una de las intervenciones a llevar a cabo es reposición de bicarbonato, que está indicada con niveles de pH menores a 7.2 o bicarbonato menor a 8 meq/L. El déficit de bicarbonato se calculará con la fórmula 0.4 × peso × (24-HCO3).14 Cada frasco de bicarbonato cuenta con 50 meq y el ámpula con 8.9 meq.
En el estado postparo se deberá realizar nuevamente gasometría para evaluar el estado ácido-base; además de valorar la necesidad de administrar una cantidad mayor de bicarbonato, se deberá determinar la causa de la acidosis e iniciar el tratamiento. En caso de acidosis metabólica refractaria, se deberá interconsultar con un nefrólogo, pues la terapia sustitutiva renal con hemodiálisis será la intervención indicada.15
Hipo-/hiperkalemia
El potasio corporal total es predominantemente intracelular, su homeostasis se mantiene principalmente por la bomba Na-K.ATPasa. El incremento en la actividad de esta bomba o alteraciones en el transporte del potasio ocasionarán hipokalemia debido al aumento en la entrada desde el espacio extracelular. Lo anterior ocurre en casos de altas dosis de insulina, activad beta-adrenérgica, alcalosis metabólica. Por otro lado, la pérdida de líquidos por vía digestiva (ya sea vómito, diarrea, uso de laxantes) se relaciona con hipokalemia. Desde el punto de vista renal, las causas más frecuentes de pérdidas renales son uso de diuréticos e incremento en la actividad de mineralocorticoides. También se pueden presentar en casos de sudoración excesiva, personas en tratamiento con terapia renal sustitutiva y plasmaféresis.16
En caso de hipokalemia, se debe iniciar cuanto antes la administración de cargas de potasio, lo que será imposible si sólo contamos con una vía periférica. Nuevamente, tener acceso intraóseo será trascendente para el manejo en caso de que no haya un acceso venoso central ya colocado. La tasa de corrección de potasio siempre causa incertidumbre. La dosis máxima de administración es 20 mmol/h; sin embargo, en casos de paro cardiorrespiratorio, se indica administración más agresiva, con infusión de 2 mmol/min en 10 minutos, seguidos de 10 mmol a pasar en cinco a 10 minutos.17
En contraste, la hiperkalemia también es una causa de paro cardiorrespiratorio. La liberación de potasio desde las células (debido a un incremento de la liberación o entrada disminuida) puede causar una elevación transitoria de potasio sérico. Para que el trastorno sea persistente, se requiere de alteración en la excreción de potasio. Esto se relaciona con una reducción en la secreción de aldosterona o la respuesta a ésta, lesión renal aguda, enfermedad renal crónica y/o descenso en la entrega de sodio y agua al sitio distal de secreción de potasio. La hiperkalemia secundaria a ingesta alta de potasio (suplementos en tabletas) no es una causa frecuente, pero su presentación es aguda. Dentro de algunos motivos de aumento en la liberación de potasio intracelular se encuentran pseudohiperkalemia, acidosis metabólica, hiperglucemia, hiperosmolaridad, catabolismo tisular elevado, uso de betabloqueadores.18
De contar con un electrocardiograma previo al paro cardiorrespiratorio, podemos identificar datos que sugieren hiperkalemia (Figura 2). De otra manera, durante las maniobras de RCP, la toma de gasometría venosa también brindará la cifra del nivel de potasio. El manejo se puede iniciar durante el paro administrando solución polarizante (solución dextrosa 5% 50 cm3 + 15 U insulina + 20 meq bicarbonato). El gluconato de calcio tiene su papel como estabilizador de membrana. En el estado postparo se pueden administrar otras medidas antikalémicas como kayexilate o salbutamol nebulizado.19
Hipotermia
Se considera hipotermia cuando la temperatura corporal se encuentra por debajo de 35 oC; se clasifica en leve (32 a 35 oC), moderada (28 a 32 oC) y severa (menos de 28 oC). La mayoría de los termómetros sólo refieren temperatura mínima de 34 oC,9 por lo que el método ideal para conocer la cifra real es con un termómetro esofágico. Dentro de las causas de hipotermia encontramos exposición ambiental, inmersión en agua, condiciones médicas (por ejemplo, hipotiroidismo o sepsis), tóxicos (etanol), medicamentos (hipoglucemiantes orales, sedantes).20
El cuadro clínico se manifiesta desde confusión, taquicardia, temblor (hipotermia leve), letargo, bradicardia, arritmias, ausencia de reflejos pupilares y disminución del temblor (hipotermia moderada) hasta coma, hipotensión, arritmias, edema pulmonar y rigidez (hipotermia severa). La evaluación con exámenes de laboratorio se puede asociar a acidosis láctica, rabdomiólisis, coagulopatía e infección.21
El manejo se enfoca en recalentar al paciente con medios físicos: remover ropa mojada, administrar soluciones intravenosas tibias, colocar sábanas calientes, aplicar calor radiante, acondicionar la temperatura del área de trabajo, realizar lavado gástrico con agua tibia y, como medida de recalentamiento más eficaz, el uso de circulación con membrana extracorpórea.22
Durante las maniobras de RCP se deben continuar las acciones antes mencionadas: la desfibrilación y los medicamentos serán inefectivos durante la hipotermia, por lo que las maniobras de RCP se deberán continuar hasta que se alcance una temperatura de 30 a 32 oC. "Nadie se declara muerto hasta que se encuentre caliente y muerto". Existen reportes de tiempos de reanimación hasta de seis horas con 52 minutos, con evolución neurológica favorable.23
En el estado postparo, la hipotermia es una recomendación para disminuir las secuelas neurológicas, por lo que la temperatura recomendada es de 32 a 36 oC y se deberá iniciar sólo hasta que el individuo se encuentre en el hospital, de preferencia en la unidad de cuidados intensivos.24
Neumotórax a tensión
El neumotórax es, en mayor frecuencia, de origen traumático. Cuando su presentación es espontánea, se clasifica como primario cuando no se relaciona a enfermedad pulmonar o secundario cuando se vincula a una comorbilidad como EPOC, fibrosis quística, cáncer pulmonar, neumonía necrotizante, tuberculosis, etcétera. Por otro lado, en el ámbito intrahospitalario, el neumotórax es resultado de una complicación posterior a un procedimiento como colocación de accesos vasculares centrales.25
Las manifestaciones clínicas dependerán de la cantidad de aire que se encuentra en el espacio pleural, la velocidad de acumulación, la edad del sujeto y la reserva respiratoria. Se presentará tos, disnea y dolor torácico. En la exploración física se evidenciará hipoventilación ipsilateral, disminución de las vibraciones vocales y timpanismo a la percusión.26
Dependiendo de la cantidad de aire acumulado, el neumotórax puede ser simple o a tensión, siendo el último la causa que puede precipitar un paro cardiorrespiratorio previa presentación de choque obstructivo.
Durante la RCP debemos obtener la historia clínica de la persona para sospechar del cuadro. La exploración física será complicada y el diagnóstico mediante radiografía de tórax o tomografía imposible durante el paro cardiorrespiratorio. Es aquí donde el ultrasonido pulmonar (USGP) puede ser una herramienta de gran utilidad y que se puede realizar durante las maniobras de RCP. La ausencia de deslizamiento pleural en el USGP tiene 70% de sensibilidad de un neumotórax (Figura 3).27

Figura 3: USG de pulmón. Se aprecia la línea que marca la pleural en la que la ausencia de deslizamiento resulta en 70% de probabilidad de neumotórax.
En caso de identificar datos de neumotórax durante las maniobras, la descompresión pleural mediante punción en el segundo espacio intercostal a la altura de la línea media clavicular está indicada. En caso de paro cardiorrespiratorio asociado a trauma, se puede realizar una punción torácica bilateral antes de detener las maniobras de reanimación y declarar la muerte. En el estado postparo se deberá colocar una sonda endopleural como manejo definitivo.28
Tamponade cardiaco
La cantidad de líquido normal en el espacio pericárdico es de 20 a 50 mL. Sin embargo, el tamponade no depende de la cantidad de volumen acumulado sino de la presión intrapericárdica; ésta, a su vez, depende de la relación entre volumen, velocidad de acumulación y distensibilidad del pericardio. De esta manera, la acumulación súbita de 150 a 200 mL ocasionará un pico en la presión intrapericárdica y resultará en tamponade, mientras que el derrame pericárdico crónico puede tolerar hasta un litro de volumen, ya que el tejido se torna más distensible y la presión es menor.29
Las causas de tamponade pueden ser infecciosas (viral, bacteriana, fúngica, etcétera), metabólicas (uremia, mixedema), autoinmunes (lupus, artritis reumatoide, fiebre reumática), neoplásicas (primarias y metastásicas), sobrecarga de volumen (insuficiencia cardiaca crónica), radioterapia, reacciones adversas a medicamentos, disección aórtica, postinfarto agudo de miocardio y traumatismo.30
Las manifestaciones clínicas se integran con la tríada de Beck (ingurgitación yugular, hipotensión, disminución de ruidos cardiacos). El electrocardiograma se observará con alternancia eléctrica. En el momento del paro cardiorrespiratorio, es un reto distinguir clínicamente esta entidad, por lo que nuevamente la ultrasonografía E-FAST, el ecocardiograma de emergencia, es de suma utilidad (Figura 4).31
Una vez identificado el derrame pericárdico, se debe realizar pericardiocentesis para posteriormente continuar con las maniobras de reanimación cardiopulmonar. En los cuidados postparo se deberá solicitar valoración por un cirujano cardiotorácico para valorar la necesidad de intervención quirúrgica.
Tóxicos
Dentro de los principales agentes cardiotóxicos que se relacionan con paro cardiorrespiratorio encontramos opiáceos, benzodiacepinas, betabloqueadores, antagonistas de los canales de calcio, digoxina, cocaína, antidepresivos tricíclicos, monóxido de carbono. Los efectos y manifestaciones clínicas de cada uno de estos agentes son sumamente amplios, por lo que no se abordarán en este artículo.
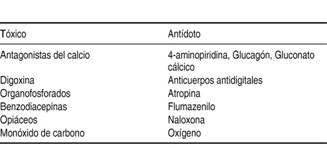
El manejo de las intoxicaciones durante el paro cardiorrespiratorio se basa en RCP de alta calidad y administración de antídotos de ser posible, aunque no existe evidencia de su eficacia ni modificación en la mortalidad.32 Algunos se muestran en el Cuadro II.
En caso de sospecha de intoxicación por opiáceos, se recomienda la administración de 2 mg de naloxona intranasal o 0.4 mg intramusculares, repitiendo la dosis a los cuatro minutos.33
Trombosis pulmonar
La tromboembolia pulmonar masiva puede desencadenar cuadro de choque obstructivo que, de no recibir tratamiento oportuno, ocasionará colapso cardiovascular y paro cardiorrespiratorio.
La etiología que con mayor frecuencia se relaciona con la trombosis pulmonar es trombosis venosa profunda. Otros factores de riesgo son:34
Riesgo alto: fractura de fémur, hospitalización por insuficiencia cardiaca o fibrilación auricular, prótesis de cadera o rodilla, politrauma, infarto agudo de miocardio, lesión de médula espinal.
Riesgo intermedio: artroscopia de rodilla, enfermedades autoinmunes, transfusiones, colocación de catéter venoso central, quimioterapia, falla cardiaca, falla respiratoria, uso de eritropoyetina, terapia de reemplazo hormonal, infecciones, cáncer, anticonceptivos orales, evento vascular cerebral, estado postparto, trombofilias.
Riesgo bajo: reposo en cama mayor a tres días, diabetes mellitus, hipertensión arterial sistémica, edad avanzada, obesidad, embarazo, venas varicosas.
Dentro de las manifestaciones clínicas se presentarán disnea, tos, ansiedad, dolor torácico. Así mismo, podemos identificar fiebre, hemoptisis, síncope y datos de trombosis venosa profunda; taquicardia sinusal en 40% de los casos.35
De no contar con diagnóstico preciso mediante angiotomografía pulmonar previo al paro cardiorrespiratorio, la ecocardiografía es de suma utilidad: reporta una sensibilidad de 60% para realizar el diagnóstico. En caso de TEP como causa de paro, usualmente se asocia que al menos dos tercios del lecho vascular pulmonar se encuentran obstruidos. El incremento en la postcarga del ventrículo derecho (VD) ocasionará dilatación de la cavidad mencionada (Figura 5). Esto se detecta midiendo el diámetro del VD > 30 mm en el eje paraesternal o como un incremento en el área del VD comparado con el ventrículo izquierdo mayor a 90% en el eje apical de cuatro cámaras.36

Figura 5: Ventana apical cuatro cámaras donde se identifica crecimiento de las cavidades derechas en un paciente con tromboembolismo pulmonar masivo.
En caso de identificar datos que correlacionen TEP masiva con el paro, se ha observado un aumento en la supervivencia administrando trombolíticos (81% versus 43%).37 No existe consenso en la dosis ideal en caso de TEP asociada a paro. La recomendación es utilizar 50 mg de alteplasa en bolo y repetir la dosis después de 15 minutos. Cabe mencionar que se deben tener en cuenta las contraindicaciones para administrar trombolíticos: antecedente de evento vascular cerebral isquémico en los últimos seis meses, hemorragia cerebral independientemente del tiempo, neoplasias o lesiones en el sistema nervioso central, traumatismo, cirugía o trauma de cráneo tres semanas previas, hemorragia digestiva en el último mes, riesgo conocido de sangrado (coagulopatías).38
En estado postparo se deberá continuar el manejo con medidas de soporte ventilatorio, hemodinámico y anticoagulación en dosis plenas, así como considerar embolectomía.
Trombosis coronaria
El infarto agudo de miocardio se considera una de las principales causas de muerte súbita. El cuadro clínico clásico se presenta con dolor torácico opresivo irradiado a hombro o mandíbula, acompañado de descarga adrenérgica. El diagnóstico se realiza obteniendo electrocardiograma de 12 derivaciones, identificando elevación del segmento ST en dos o más de ellas. Por otro lado, también se puede presentar infarto agudo de miocardio sin elevación del ST en el que con elevación de marcadores cardiacos como troponina, mioglobina y/o CPK-CKMB se realizará el diagnóstico. Ecocardiográficamente, se identificará alteración en la movilidad regional de la pared afectada.39
Durante el paro cardiorrespiratorio, el ultrasonido o ecocardiograma no son de utilidad para realizar el diagnóstico. El electrocardiograma no mostrará datos debido a que no hay actividad eléctrica. Los marcadores bioquímicos serán de utilidad sólo si fueron tomados antes del colapso cardiovascular, ya que después de las compresiones cardiacas es normal encontrarlas elevadas. De cualquier manera, el manejo se centrará en continuar con maniobras de RCP de alta calidad y fármacos, ya que la trombólisis no está recomendada en caso de trombosis coronaria.8
En el estado postparo se debe realizar un electrocardiograma. En caso de que existan datos clínicos o se sospeche de infarto agudo de miocardio, el paciente deberá ingresar a hemodinámica para que se realice angioplastia coronaria percutánea, ya que se ha identificado aumento en la supervivencia realizando este procedimiento de manera temprana.24
utilidad durante el paro cardiorrespiratorio
Actualmente, las prioridades en el manejo del paro consisten en disminuir las interrupciones de las compresiones, por lo que el uso del ECO/USG durante las maniobras de RCP, es un gran reto. El operador debe tener entrenamiento especializado en reanimación para integrarse de manera efectiva al equipo y tener en cuenta la importancia de las compresiones torácicas ininterrumpidas. De esta manera, el tiempo de 10 segundos para verificar ritmo y pulso es el momento para obtener una ventana cardiaca. La vista subcostal se considera la más útil en este sentido y permite menor interrupción de compresiones. La AHA recomienda en las guías recientemente publicadas el uso del ECO/USG durante la RCP, con un nivel de evidencia clase IIb.40 El Consejo de Reanimación del Reino Unido ha diseñado un programa de entrenamiento especializado en ecocardiografía durante la RCP (Focused Echo Evaluation in Life Support, FEEL) avalado por la Sociedad Británica de Ecocardiografía. Así mismo, se han propuesto algoritmos como el CAUSE (Cardiac Arrest Ultrasound Examination), que aborda la evaluación que debe ser realizada para identificar la causa del paro e iniciar tratamiento mientras se continúan las maniobras de RCP (Figura 1).41
Conclusión
El manejo de la RCP durante asistolia y AESP se debe enfocar en la calidad de las compresiones, administración de adrenalina e identificación de la causa. El abordaje de las H y las T abarca desde el momento previo al paro, durante el paro y en los cuidados postparo. El manejo en muchos casos se puede iniciar durante las maniobras y deberá continuar hasta un abordaje definitivo en estado postparo. El ultrasonido y/o la ecocardiografía de emergencia son una gran herramienta durante la reanimación; sin embargo, nunca se deberá dar mayor importancia a obtener una imagen que a continuar con las compresiones.











 nueva página del texto (beta)
nueva página del texto (beta)