Introducción
El enorme número de casos que pueden llegar a las áreas críticas en la presente pandemia hace deseable que la selección de casos se efectúe de manera óptima. Se espera una enorme presión para los médicos ante un padecimiento nuevo, del que hay aún muchas preguntas sin resolver. Los pacientes se referirán a la UCI desde el Servicio de Urgencias, donde en general se cuenta con personal calificado y con experiencia en la identificación y manejo de la insuficiencia respiratoria aguda (IRA), y como sucede con otras patologías, otro número de pacientes provendrán de los pisos, éstos son casos identificados como graves, pero sin necesidad de ingreso a intensivos y que en muchas ocasiones serán seguidos por grupos de medicina interna y otras especialidades con menor contacto con IRA, que potencialmente podrían decidir intubar a estos pacientes siguiendo guías y protocolos, pero sin la experiencia para resolver el caso de la mejor manera. Una vez intubado, se enviará a alguna otra área hospitalaria, lo que aumentará la presión para el sistema de salud. Mediante la presentación de dos casos, se evidencia la factibilidad de brindar un manejo domiciliario si se cumplen ciertas premisas de bajo riesgo.
Casos clínicos
Caso 1
Paciente masculino de 54 años de edad sin antecedentes patológicos de interés, a excepción de diagnóstico de dislipidemia leve controlada y proteinosis alveolar 14 años antes, así como sobrepeso los últimos cuatro años. Fumó socialmente un par de años en su juventud. Visitó por razones profesionales dos estados del sur de los EE.UU., en enero de este año; después, se reunió con su familia para vacacionar por cuatro días en un tercer estado de ese país, estando todos asintomáticos. De regreso a la Ciudad de México, debutó seis días después con tos seca leve, cefalea y pocas horas después fiebre severa, que cedía parcialmente con antitérmicos e importante ataque al estado general con mialgias incapacitantes. Al segundo y tercer día de su padecimiento, se le notificó que dos personas con las que había convivido en EE. UU. dieron positivas para SARS-CoV-2, motivo por el que se le estudió, tras lo cual se encontró una neumonía de focos múltiples sin insuficiencia respiratoria, (SpO2 al 21%: 90%, FC: 92x’, con corrección al 94% con 1 LPM de O2). Se le auscultaban escasos estertores crepitantes teleinspiratorios subescapulares derechos, sin síndrome de condensación y se le observaba tranquilo, sin taquipnea y negando disnea.
El RT-PCR para este nuevo virus fue negativo, al igual que el panel de virus respiratorio por PCR, que incluyó adenovirus, coronavirus 229E, coronavirus HKU1, coronavirus NL63, coronavirus OC43, metapneumovirus humano, rinovirus, enterovirus humano, influenza A, influenza A/H1, influenza A/H1-2009, influenza A/H3, influenza B, parainfluenza virus 1, parainfluenza virus 2, parainfluenza virus 3, parainfluenza virus 4, virus sincitial respiratorio, así como las siguientes bacterias Bordetella pertussis, Chlamydophila pneumoniae y Mycoplasma pneumoniae. Antígeno urinario para Legionella e histoplasma negativos. De sus laboratorios destacan leucopenia y linfopenia progresiva, elevación del dímero-D, DHL y ferritina (Tabla 1).
Tabla 1: Resultados de laboratorio de ambos casos al momento del diagnóstico.
| Parámetros de laboratorio | |||||||
|---|---|---|---|---|---|---|---|
| Caso 1 | Caso 2 | ||||||
| Diagnóstico | Séptimo día | Catorceavo día | Veintiunavo día | Diagnóstico | Séptimo día | Veintiochoavo día | |
| Leucocitos | 4,500 | 4,000 | 3,200 | 5,900 | 6,500 | 4,100 | 7,200 |
| Linfocitos totales | 960 | 840 | 900 | 1,160 | 1,280 | 350 | 1,340 |
| Plaquetas | 230,000 | 189,000 | 230,000 | 310,000 | 532,000 | 315,000 | 697,000 |
| Nitrógeno de urea | 22 | 24 | -- | 23 | 23 | 21 | 17 |
| PCRu | 36 | 102 | 11.2 | 6.4 | 48 | 61 | 4.9 |
| PCT | 0.20 | -- | -- | 0.15 | 0.10 | 0.30 | 0.05 |
| Dímero-D | 24,000 | 33,000 | 19,000 | 1,400 | 39,000 | 27,000 | 462 |
| Ferritina | 940 | 903 | 410 | -- | 801 | 1,200 | 301 |
| DHL | 400 | -- | 280 | -- | 243 | 202 | -- |
| SARS-CoV-2 | Ausente | Presente | |||||
| Panel viral | Negativo | Influenza negativo | |||||
PCRu = proteína C reactiva ultrasensible, PCT = Procalcitonina, DHL = deshidrogenasa láctica.
Se muestran los resultados al momento del diagnóstico y de las tres a cuatro primeras semanas. En las semanas subsecuentes estos hallazgos se normalizaron de manera progresiva como reflejo de la reducción del proceso inflamatorio sistémico; sin embargo, los requerimientos de O2 suplementario pueden extenderse más de un mes.
Las imágenes radiológicas mostraron patrón de vidrio despulido bilateral periférico, que evolucionó lentamente hacia la mejoría (Figura 1).
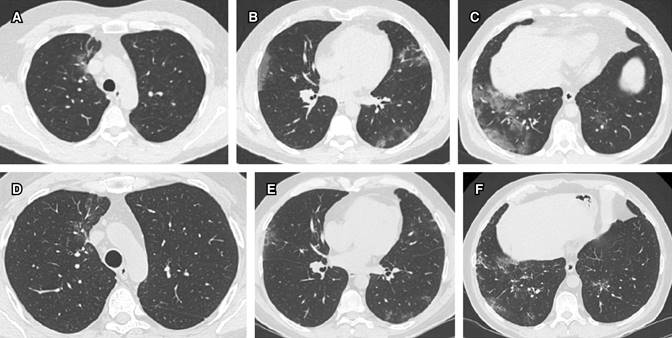
Figura 1: Evolución tomográfica del caso 1 en cortes axiales a tres niveles: A) apical, B) medio y C) basal al momento del diagnóstico, comparativamente con un control tomográfico realizado 20 días después a los mismos niveles de corte (D-F) con una obvia mejoría.
En la actualidad, el paciente se encuentra estable, asintomático respiratorio, con cierto cansancio residual, pero ya trabajando de manera parcial; todos sus contactos han permanecido asintomáticos (cinco familiares, cuatro personas del servicio y tres colaboradores directos). Sus exámenes de laboratorio se normalizaron. No se le han realizado antígenos séricos de SARS-CoV-2 todavía.
Caso 2
Paciente masculino de 57 años de edad, con sobrepeso, hiperuricemia y diabetes mellitus tipo 2 con regular manejo mediante hipoglicemiantes orales e insulina SC. Tabaquismo negativo. Tuvo contacto en su trabajo con persona diagnosticada con COVID-19 cuatro días antes de iniciar con sintomatología, la cual consistía en cefalea, conjuntivitis, rinorrea hialina leve de corta duración y odinofagia, seguida de tos seca intensa en accesos frecuentes e importante ataque al estado general, mialgias, artralgias, seguido 24 horas después de fiebre elevada, diaforesis profusa y debilidad. Se le descartó influenza y se comprobó SARS-CoV-2 mediante RT-PCR, integrándose el diagnóstico neumonía de focos múltiples con insuficiencia respiratoria (SpO2 al 21%: 79%, FC: 96x’, 90-91% con 2 LPM de O2), sin síndrome de condensación al examen físico. El síndrome febril fue intenso por una semana aproximadamente, con un promedio de dos a tres viremias al final de la primera semana de evolución. Los exámenes de laboratorio revelaron típicamente leucopenia, linfopenia importante, plaquetopenia, elevación del dímero-D, DHL y ferritina. Las tres «T’s» y el fibrinógeno descartaron coagulopatía por consumo (CID) (Tabla 1).
Sus imágenes radiológicas pueden observarse en la Figura 2 y consistieron igualmente de imágenes en vidrio despulido, en parches bilaterales y profusos, abarcando prácticamente todas las regiones del pulmón. Evolucionó sin taquipnea ni disnea. En la actualidad se encuentra estable, con mejoría importante de la tos y afebril, refiriendo fatiga y debilidad muscular particularmente en las extremidades inferiores. Uno de sus hijos resultó positivo 11 días después, con un cuadro muy leve y manifestaciones en piel.

Figura 2: Cortes tomográficos del caso 2 al séptimo día de evolución. El cuadro clínico del COVID-19 puede empeorar a partir de la segunda semana de evolución, en la cual habrá que estar particularmente atentos ante el inicio de disnea. Se aprecian cortes axiales ápico-caudales (A-C), coronales antero-posteriores (D-F) y sagitales derecha a izquierda (G-I); obsérvense los amplios infiltrados en vidrio deslustrado bilaterales generalizados, cuyo carácter periférico ha empezado a perderse.
Discusión
Existen distintas categorías de neumonía según el escenario clínico: neumonía adquirida en la comunidad (NAC), neumonía en el anciano, neumonía nosocomial (que incluye a la neumonía asociada al ventilador o NAV), neumonía en el huésped inmunocomprometido y la relacionada con fibrosis quística y otras alteraciones anatómicas. Dentro de la primera, incluimos a la NAC típica (clásica), a la atípica (no bacteriana)1 y a la neumonía por aspiración.
Sabemos que las causas de neumonía atípica son múltiples, a saber: mycoplasma (M. pneumoniae), Chlamydophila (C. psittaci, C. pneumoniae), bacterias (Legionella spp., F. tularensis, Y. pestis, B. antrhracis), hongos (Histoplasma, Blastomyces, Coccidioides, Pneumocystis), neumonitis por aspiración (estéril o por flora mixta de la vía aérea superior o boca), virus (influenza, adenovirus, virus sincicial respiratorio, parainfluenza, metapneumovirus, varicela zóster, sarampión, virus de Epstein-Barr, citomegalovirus, hantavirus, coronavirus) y rickettsias (C. burnetii).2
En el contexto de la pandemia, toda neumonía debe considerarse como probable caso de COVID-19, aislarse y manejarse en consecuencia, la gran mayoría como paciente ambulatorio (80%) y sólo los casos graves requerirán hospitalización; por lo general, en servicios generales y a cargo de personal no especializado en enfermedades pulmonares infecciosas agudas, un porcentaje menor (aproximadamente 5%) requerirá su traslado a áreas críticas por empeoramiento de la insuficiencia respiratoria, evaluada por clínica, radiología y a veces toma de gases arteriales, generalmente sólo con una oximetría de pulso. Hemos observado al inicio de la pandemia en nuestro medio la admisión de casos no justificados, probablemente por el temor acumulado por semanas en el sector médico y lo impactante de las imágenes radiológicas, entre otras, pero la optimización de recursos es prioritaria en estos momentos.
En general, en la sociedad por razones comprensibles, existe temor de ingresar a un hospital y más a una UCI al asociarlo no sólo a posibilidad de muerte, sino a sufrimiento muy vinculado con la imagen de la ventilación mecánica y a costos elevados. En particular, en el COVID-19, ha habido algunas voces en los EE. UU. que opinan que la AMV puede estar dañando a cierto tipo de pacientes con esta nueva enfermedad; las cifras reportadas de mortalidad en pacientes positivos bajo apoyo ventilatorio son inusualmente elevadas, ya que de 40 a 50% de los pacientes con SIRPA grave (80% en Nueva York) mueren estando en el ventilador y muchas veces de (y no con) insuficiencia respiratoria progresiva y falla orgánica múltiple terminal, cuando por décadas la mortalidad directa por IRA se reportó en el orden de 16% solamente y la mortalidad en UCI de la neumonía atípica se ha reportado en 11%.3 Ante esto, es factible pensar que en estos casos existe un daño asociado al ventilador particularmente amplificado que podríamos llamar «VALI-19», con conexiones deletéreas al sistema inmunológico y una exuberante respuesta inflamatoria asociada con trombosis, razón por la que hay que revisar detenidamente los criterios clásicos de intubación en pacientes con SARS-CoV-2 para hacerlos más laxos y procurar en estos casos cierto nivel de «hipoxemia permisiva», basados en lo anterior y en el hecho de que un número importante de estos enfermos no tienen la disnea habitual para este grado de afección pulmonar, al ser conectados al ventilador tienen muchas veces distensibilidades pulmonares conservadas.
Sin embargo, cambiar un paradigma dentro de la incertidumbre de una pandemia es muy complicado, nos han educado para reconocer tempranamente al SIRPA e intervenir de manera inmediata como una forma de intentar un cambio en la historia natural de la enfermedad que desde su descripción original en 1967 ha sido devastadora, aunque nunca antes como ahora. Es por ello comprensible que dentro de la intensidad de trabajo de un piso general, destinado o no específicamente para pacientes COVID-19, los jóvenes médicos residentes se aceleren para intubar a estos pacientes y solicitar su pase a intensivos, y eso es lo que hay que cambiar, iniciando por estratificar de mejor forma quién en realidad debe estar en su casa y quién en un hospital, como se ha hecho para padecimientos históricamente muy importantes;4 considero muy probable el hecho de estar eligiendo mal a quién intubar, lo que está llevando a un sobreuso de la AMV en la pandemia en todo el mundo, ante lo cual se requerirá en los pisos de personal con experiencia en el manejo de la insuficiencia respiratoria crónica y con ello me refiero a los especialistas médicos y de enfermería en enfermedades pulmonares y a los terapistas respiratorios, que poseen práctica y conocimiento para manejar pacientes a veces muy hipoxémicos que no es deseable intubar y de hecho no se intuban y salen adelante, no sin muchos interludios de inconvenientes, éste es el grupo que debe coordinar intrahospitalariamente y de manera ideal el flujo de pacientes hacia áreas críticas.
Siempre está la alternativa de la AMV no invasora y además de las puntas de O2 de alto flujo que considero de uso potencialmente peligroso, por la posibilidad de diseminar la infección en sectores importantes de los propios hospitales, afectando la operación de los mismos al contagiar al preciado personal de salud. En el artículo de revisión que se publica en este mismo número, propongo algunas precondiciones importantes si esto se quiere implementar.5
Con los casos que aquí se presentan, intento lograr una reflexión hacia la difícil e importante decisión del manejo intradomiciliario de casos de COVID-19, aunque con la cautela que el asunto amerita, ya que resulta obvio que no se puede generalizar.
Desafortunadamente, las características ideales para seleccionar estos casos pueden no encontrarse tan comúnmente en nuestro medio e incluyen de manera no exclusiva lo enlistado en la Tabla 2.
Tabla 2: Precondiciones a considerar antes de proponer el manejo ambulatorio de un paciente positivo a SARS-CoV-2.
| Factores a considerar en la valoración del manejo domiciliario de pacientes con neumonía por COVID-19 |
|---|
| • CURB-65 ≤ 2 en enfermedad temprana |
| • Paciente inteligente y cooperador* |
| • Buena red de apoyo familiar |
| • Aceptación y cultura de la enfermedad y escenario particular |
| • Plena comprensión del síntoma disnea |
| • Recursos económicos |
| • Capacidad de aislamiento total en un cuarto |
| • Disponibilidad de toma de signos vitales, SpO2 y O2 domiciliario |
| • Disponibilidad de toma de laboratorio a domicilio (y Rx) |
| • No antecedentes de ETV y capacidad para aplicarse HBPM vía SC |
| • Estrecha comunicación electrónica en tiempo real con el médico |
| • Vivienda cercana al hospital de referencia |
* El cooperar con la posición prono es fundamental. ETV = enfermedad tromboembólica venosa. HBPM = heparina de bajo peso molecular.
La labor médica lejos de disminuir en estos casos, es muy intensa y de gran responsabilidad, con videoconferencias programadas varias veces al día, reporte de signos vitales y SpO2 (con O2 y al aire ambiente, en reposo y después de moverse al baño) cada 4 a 6 horas con el líder designado de la familia, mismo que procura los cuidados de manera directa, además del propio paciente. Se recomiendan actividades de reforzamiento de medidas de asilamiento y protección personal, y un canal abierto permanentemente en caso de cambios adversos, particularmente el inicio de disnea, así como visitas presenciales ocasionales. Se demuestra, por otro lado, que en pacientes de bajo riesgo, con contexto favorable y bien seleccionados, el manejo domiciliario del COVID-19 es factible, guardando las camas hospitalarias para pacientes de mayor gravedad y evitando tal vez un número no determinado de intubaciones no indispensables, realizadas muchas veces por personal no experto, evitando así la saturación de las UCI. El Especialista en Terapia Intensiva y los médicos encargados del triage deben considerar estos argumentos. En estos casos, no se utilizó ninguna terapia farmacológica no autorizada por las agencias reguladoras (FDA, EMA, COFEPRIS), sólo paracetamol, dropropizina, enoxaparina SC a dosis profilácticas y O2 suplementario por puntas nasales; ambos recibieron oseltamivir antes de tener el resultado del RT-PCR para influenza y una dosis de azitromicina antes de recibir el resultado de la PCT; en ninguno de ellos se presentó infección bacteriana secundaria, misma que está asociada sobre todo con gérmenes nosocomiales, particularmente en el uso de AMV (que en estos casos no es menor de siete a 10 días), como tampoco presentaron sepsis u otras complicaciones. El primer caso se notificó simplemente con el diagnóstico de neumonía atípica de probable etiología viral (del tipo del SARS-CoV-2), ya que sabemos del porcentaje de resultados falsos negativos,5 mientras que el segundo correspondió sin ninguna duda a un caso de COVID-19 comprobado, ambos manejados exitosamente de manera conservadora en su domicilio, a pesar de haber tenido comorbilidad. El sistema de puntaje CURB-656 junto con otras variables continúa mostrando una invaluable utilidad.











 nueva página del texto (beta)
nueva página del texto (beta)


