Introducción
El edema macular es una causa importante de un menor resultado visual postoperatorio tras la cirugía de cataratas.1-3 Los pacientes diabéticos con retinopatía preexistente son más propensos a desarrollar edema macular tras un cirugía de cataratas que los sujetos normales o los pacientes diabéticos sin retinopatía antes de la cirugía.1,4,5
El resultado de las cirugías de cataratas está directamente asociado a la gravedad de la maculopatía antes de la cirugía.6,7
En el caso del edema macular significativo a nive clínico la fotocoagulación macular ha demostrado ser eficaz según un estudio sobre la retinopatía diabética de tratamiento temprano;8,9 no obstante, la fotocoagulación con láser tiene como objetivo evitar futuras pérdidas moderadas de la visión. Sin embargo, no puede restaurar la visión ya perdida antes del tratamiento.10
Debido a esta limitación, otras modalidades de tratamiento se han popularizado tales como los factores de crecimiento endotelial antivasculares (VEGF) intravítreos que han demostrado ser eficaces para el tratamiento de la retinopatía diabética neovascular y exudativa desde 2005; no obstante, su uso durante la cirugía requiere estudios a largo plazo.11
La inyección intravítrea de esteroides juega un papel antiinflamatorio y media la regulación a la baja de los VEGF pudiendo mejorar el edema macular refractario. No obstante, se asocia a complicaciones graves amenazantes para la visión tales como cataratas, glaucoma y endoftalmitis.12,13
El acetónido de triamcinolona subtenoniano posterior (PSTA) es una alternativa menos invasiva a la vía intravítrea y ha demostrado ser eficaz para tratar la uveítis posterior con edema macular asociado.14
Algunos estudios han informado que el PSTA, cuando se combina con la fotocoagulación macular con láser como tratamiento del edema macular diabético, ofrece mejores resultados visuales que el láser únicamente.15
Los cambios en el grosor de la mácula en respuesta al tratamiento combinado también se han descrito mediante tomografía de coherencia óptica (OCT).16
El objetivo del presente estudio es mostrar el efecto del PSTA al final de las cirugías de facoemulsificación en pacientes con edema macular preexistente previo a la cirugía y evaluar los cambios en el mapa de grosor macular después de este aborgaje combinado.
Pacientes y métodos
Se trata de un estudio de casos y controles que se llevó a cabo con la aprobación del comité científico de la Facultad de Medicina de Al-Kindy y se ajustó a los principios establecidos en la Declaración de Helsinki.
En el estudio se inscribieron 30 pacientes diabéticos con cataratas visualmente significativas que tenían previsto someterse a cirugías de cataratas en el Hospital Privado de Especialidades Oftálmicas en el período comprendido entre enero de 2020 y enero de 2021.
Los pacientes con maculopatía y sus características demográficas se muestran en la tabla 1.
Tabla 1 Carácterísticas preoperatorias de los pacientes
| Datos demográficos | Datos |
|---|---|
| Ojo/paciente | 40/30 |
| Sexo | |
| Hombre/mujer | 16/14 |
| Edad (año) | 60.2 ± 54 |
| MAVC preoperatoria Log MAR | 1.02 ± 0.12 |
| Grosor del subcampo central basal mm | 296.4 ± 80.9 |
| Grosor del anillo interior basal mm | 350.1 ± 75.5 |
| Grosor del anillo exterior basal mm | 315.6 ± 80.5 |
| PIO basal (mmHg) | 17.4 ± 2.8 |
| Antecedentes de fotocoagulación | no |
| Antecedentes de inyección de anti-VEGF durante los últimos 3 meses | 28/47 |
MAVC: mejor agudeza visual corregida, PIO: presión intraocular.
Criterios de exclusión
Los siguientes fueron criterios de exclusión:
Cirugías intraoculares previas o inflamación.
Antecedentes de glaucoma o de terapia con esteroides.
Pacientes con retinopatía proliferativa.
Pacientes con mala perfusión macular por OCT-Angio.
Complicaciones intraoperatorias tales como rotura de la cápsula posterior, lesión del iris o colocación de lente intraocular en el surco.
Antes de inscribir a los candidatos en el estudio, se les explicó el diagnóstico, pronóstico, alternativas terapéuticas disponibles y posibles beneficios e inconvenientes y se obtuvo su consentimiento informado formal.
Valoraciones preoperatorias
Todos los pacientes fueron examinados con una lámpara de hendidura para realizar exámenes completos de los segmentos anterior y posterior, presión intraocular (PIO) mediante tonometría de aplanación (AT900, Haag-Streit Diagnostics, Suiza), mejor agudeza visual corregida (MAVC), OCT y OCT-angio y microscopía especular.
OCT y OCT-angio: (Optovue Inc, Fremont, California, Estados Unidos).
Se utilizó un colirio tópico de tropicamida al 1 % para dilatar las pupilas, y el estudio de imagen se realizó 3 veces por paciente en el mismo día por el mismo técnico profesional cualificado en el uso del dispositivo Optovue-OCT.
Todas las exploraciones se realizaron lo más cerca posible de la fóvea con suficiente claridad de imagen y se tomó la imagen del punto más fino de la mácula para evitar imprecisiones en las mediciones de grosor ocasionadas por pequeñas variaciones en la posición. Sólo se consideraron adecuadas las fotografías si se podía discernir fácilmente toda la extensión y profundidad de la retina y en ausencia de cambios en el ojo o artefactos de parpadeo durante el procesamiento de las imágenes.
El subcampo central (el área circular representa el diámetro central de 1 mm situado alrededor del centro) se calculó mediante OCT. Se midió el grosor de los nueve anillos interiores y exteriores del análisis de la retinopatía diabética, así como el grosor macular general.
Cirugía de cataratas
Las cirugías de facoemulsificación fueron realizadas por un único cirujano experimentado; se realizó una incisión clara en la córnea con ayuda de un queratomo de 2,8 mm seguida de una caspulorrexis anterior curvilínea continua y cirugía de faco mediante la técnica de parada y corte (INFINITI Vision System [Alcon Laboratories, Inc]). Tras la aspiración cortical, se implantó una LIO monofocal Sensar de una pieza (Johnson and Johnson) en la bolsa procediéndose a hidratar el estroma de la incisión principal con una solución salina equilibrada hasta asegurarse de que quedaba sellada. Se administraron 200 mg en 0,2 cc de Auromox (es un vial sin conservantes, Auromox contiene 1 cc de moxifloxacino hidrocloruro 5,45 mg equivalente a 5 mg de moxifloxacina Aurolab, India) en la cámara anterior a través del puerto lateral. Su eficacia en la prevención de la endoftalmitis quedó demostrada por nuestro anterior estudio de cohorte.17 A la finalización de la cirugía se inyectó 1 cc de 40 mg de acetónido de triamcinolona (Aurocort, Aurolab company, India, una solución sin conservantes en proporción 40 mg/1 cc) en el subtenon posterior mediante abordaje temporal inferior.
Valoraciones posoperatorias
Consulta de seguimiento al cabo de 1 día, 1 semana, 1, 3 y 6 meses. En todas las consultas se realizó un examen del segmento anterior para ver la reacción de la CA mediante lámpara de hendidura. Se realizó valoró la MAVC al cabo de 1, 3 y 6 meses, y se realizó una OCT a los 3 y 6 meses. La PIO se analizó al cabo de 1 semana, 1, 3 y 6 meses mediante tonometría de aplanación.
Valoraciones sistémicas preoperatorias: glucemia en ayunas, HBA1C, perfil lipídico sérico y todo paciente con parámetros sistémicos alterados fue derivado al médico para un mejor control glucémico antes de coger cita para la cirugía.
Los investigadores principales durante la valoración preoperatoria y postoperatoria fueron el oftalmólogo y el optometrista, que no se inscribieron en el estudio.
Análisis estadístico
Se utilizó el software Minitab 16 para el análisis de los datos, que se expresaron como media ± DE. Los datos basales preoperatorios frente a los correspondientes datos postoperatorios se compararon mediante la prueba t para muestras pareadas. La comparativa de > 2 medias se realizó mediante la fórmula estadística ANOVA unidireccional. Los resultados se consideraron significativos desde el punto de vista estadístico con valores p < 0.05.
Resultados
Cuarenta ojos de 30 pacientes, con una media de edad de 60 ± 4.5, 16 eran varones y 14 mujeres. Durante el seguimiento:
Examen del segmento anterior
Inflamación moderada del segmento anterior (+2) en cinco ojos en la consulta de seguimiento al cabo de 1 semana, la patología se resolvió prescribiendo trometamina ketorolaco tópica al 0.5 % 4 veces al día y tropicamida al 1 % 3 veces al día durante 2 semanas.
Cambios en la MAVC: La MAVC media pasó de 1.02 ± 1.12 Log MAR basal a 0.58 ± 0.01 (p = 0.0001) y 0.56 ± 0.02 (p = 0,0001),en las consultas de seguimiento realizadas al cabo de 1 y 3 meses. Y a los 6 meses 0.42 ± 0.1 (p = 0.002).
Cambios en la PIO: no se observaron subidas significativas de la PIO desde el punto de vista estadístico con respecto a los valores basales (p = 0.62). Dos pacientes desarrollan subidas significativas de la PIO (> 10 mmHg). En uno de ellos, el ojo contralateral tiene una cirugía de cataratas complicada con glaucoma de ángulo abierto secundario. El otro paciente no tenía antecedentes de una PIO alta en ninguno de los dos ojos. La PIO de ambos pacientes se controló con colirios tópicos para reducción de la PIO.
Cambios maculares en la OCT
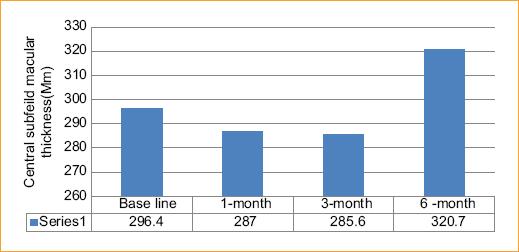
Grosor del subcampo central: El grosor macular medio del subcampo central (CSMT) preoperatorio fue de 296.4 ± 80.9, pero mejoró hasta 287.8 ± 91.3 al cabo de 1 mes, a pesar de que el resultado no es significativo desde le punto de vista estadístico (p = 0.06), pero sí tiene importancia clínica. A los 3 meses, era de 285,6 ± 76.2 (p = 0.62), de nuevo sin importancia significativa desde le punto de vista estadístico con respecto al resultado inicial (p = 0.178). A los 6 meses era de 320.7 ± 74.5, en este caso, sí con una diferencia significativa con respecto a los valores basales (p = 0.001) Figura 1.
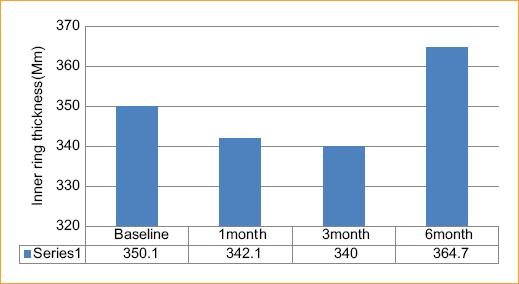
Grosor del anillo interior: El grosor medio basal del anillo interior fue de 350.1 ± 75.5. En la consulta celebrada al cabo de 1 mes, pasó a ser 342.1 ± 85.9. A los 3 meses, fue de 340.7 ± 65.9. Si comparamos los resultados posoperatorios con el grosor del anillo interior basal mediante ANOVA unidireccional, no se observa una mejora significativa desde le punto de vista estadístico (p = 0.09). A los 6 meses, no osbtante, fue de 364.7 ± 78.35 detectándose un deterioro significativo (p = 0.008) Figura 2.
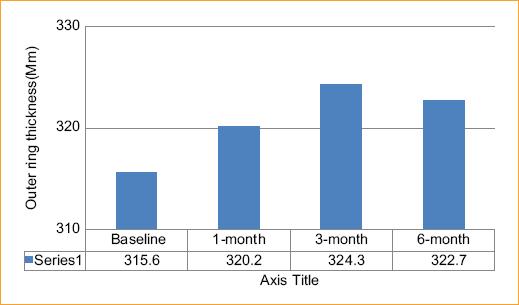
Grosor del anillo exterior: El grosor medio basal fue de 315.6 ± 80.5. Al cabo de 1 mes, 320.2 ± 83.4, al cabo de 3 meses, 324.3 ± 65.7 y al cabo de 6 meses, 322.7 ± 119.7.
No se observaron diferencias significativa desde le punto de vista estadístico según el ANOVA unidireccional (p = 0.74) Figura 3.
Discusión
El edema macular es la causa más común de pérdida de agudeza visual en pacientes diabéticos. En lo referente a la cuestión de ausencia de retinopatía, el hecho de si la cirugía de cataratas acelera o no el avance de la retinopatía sigue siendo objeto de debate.17-21
Algunos autores no comunicaron cambios significativos en la retinopatía,18,21 si bien otros informaron de un empeoramiento significativo del edema macular en ojos con edema macular preexistente antes de la operación.1,4,5 La diferencia en sus resultados podría deberse a los diferentes criterios de avance de la retinopatía, a factores de confusión tales como el control de la glucemia y al tipo de cirugía empleada, sea esta complicada o no.
En el presente estudio, los grosores medios del subcampo central y del anillo interior 1 mes después de la facoemulsificación y el PSTA se mantuvieron estables y no mostraron deterioro del grosor. De hecho, 9 ojos mostraron mejoras estadísticas con respecto al grosor del subcampo central basal. El grosor macular se mantuvo 3 meses después de la cirugía mientras que el efecto de la triamcinolona como prevención del deterioro al cabo de 3 meses ha remitido cuando 20 ojos precisaron AVEGF (AVASTIN), para 10 ojos utilizamos fotocoagulación láser focal bajo guiardo OCT-A puesto que hicieron rechazo a las inyecciones intravítreas (entre ellos los que respondieron a los esteroides). Cinco ojos se mantuvieron estables, mientras que en los otros 5 utilizamos una dosis distinta de PSTA y trometamina ketorolaco tópica al 0,5 % 4 veces al día durante 1 mes.
Nuestros resultados son comparables a los de Lodhi et al.,22 en lo que respecta al efecto de la inyección de PSTA en su ensayo controlado, en el que se incluyeron 18 ojos con retinopatía diabética que recibieron PSTA. No obstante, el tamaño de su muestra es pequeño y prescribieron colirios de esteroides tópicos durante 6 semanas tras la intervención, mientras que en nuestros pacientes aplicamos un abordaje sin gotas para eliminar todos los factores de confusión que pudieran afectar los resultados de nuestro estudio. Además, utilizamos la OCT para analizar mejor los cambios acaecidos tanto en el subcampo central como en los anillos interior y exterior.
Kim et al.23 informaron que el cambio medio en el grosor macular central (GMC) al cabo de 1 mes es mayor en el grupo de control que en el grupo de PSTA. Esto refleja las posibles causas del deterioro de la maculopatía un mes después de la cirugía de cataratas como son la rotura de la barrera hematorretiniana y el aumento de la inflamación en pacientes diabéticos tras una operación de cataratas. Tras una facoemulsificación sin complicaciones, se produce una elevación de los niveles de VEGF, factor de crecimiento hepatocitario, IL1 y factores derivados del epitelio pigmentario, que tardan hasta 1 mes en volver a sus niveles iniciales,24 lo cual podría explicar el empeoramiento de la retinopatía que se observa 1 mes después de la operación de cataratas.
Ahmadabadi et al.25 informaron que la inyección intravítrea de acetónido de triamcinolona tras facoemulsificación en pacientes diabéticos redujo la cantidad de grosor del punto central y la aparición de edema macular cistoide. Los aborgajes intravítreos conllevan riesgo de cataratas, glaucoma y endoftalmitis. Nuestro aborgaje es seguro, menos invasivo y eficaz en la prevención del deterioro hasta 3 meses después de la cirugía. A pesar de los efectos secundarios mencionados tales como perforación del globo ocular (poco frecuente), escleritis, oclusión de la arteria central de la retina, blefaroptosis e infección, no se documentó ninguna de estas complicaciones.
Chew et al.26 informaron que la AT peribulbar anterior se asoció a un mayor riesgo de PIO elevada y desarrollo de cataratas comparado con el PSTA. Esto concuerda con nuestros resultados, que no muestran una elevación significativa desde le punto de vista estadístico de la PIO un mes después del PSTA.
En cuanto a los cambios en la MAVC: la mejora de la MAVC experimentada tras la facoemulsificación y el PSTA fue significativa y se asoció a la extracción de la catarata y al efecto de la triamcinolona que evita el avance de la retinopatía que sobreviene, principalmente, 1 mes después de la cirugía de cataratas. La mejora se mantuvo durante 3 meses si bien el descenso significativo observado a los 6 meses se asoció, principalmente, al avance de la retinopatía. Los resultados actuales coinciden con los resultados visuales comunicados por Hegazy et al.27 y por Lodhi et al.22
En cuanto al efecto antiinflamatorio del PSTA, la reacción de la cámara anterior fue comparable a la de pacientes tratados con esteroides tópicos, lo cual viene a avalar el aborgaje sin gotas después de la facoemulsificación y aquí ampliamos el límite de nuestro anterior estudio de cohorte,17 cuando excluimos a pacientes diabéticos con retinopatía de los aborgajes sin gotas. Por lo tanto, informamos de la eficacia de la prevención de la inflamación posoperatoria y de la seguridad del PSTA con respecto a la posibilidad de una subida de la PIO.











 nueva página del texto (beta)
nueva página del texto (beta)